Clear Sky Science · pl
Obliczeniowa identyfikacja fitozwiązków Terminalia arjuna jako potencjalnych inhibitorów 3α-HSD3
Dlaczego to badanie ma znaczenie
Rak piersi jest najczęstszym nowotworem u kobiet, a wiele guzów rozwija się pod wpływem hormonów. W tym badaniu postawiono aktualne pytanie: czy naturalne substancje z tradycyjnego leczniczego drzewa Terminalia arjuna można przekształcić w nowoczesne kandydaty na leki, które łagodnie „wyciszą” kluczowy enzym przetwarzający hormony powiązany z wzrostem guza? Zamiast testów na zwierzętach, badacze zastosowali zaawansowane symulacje komputerowe, szukając związków roślinnych, które mogłyby w przyszłości uzupełniać lub poprawiać istniejące terapie hormonalne.
Hormony, pojedynczy enzym i wzrost guza
W niektórych rakach piersi, zwłaszcza w powszechnie badanym typie MCF-7, wzrost jest silnie napędzany przez żeński hormon estrogen. Zazwyczaj androgeny (często kojarzone z hormonami męskimi) mogą przeciwdziałać efektom estrogenu. Enzym będący w centrum tego badania, określany jako 3α-HSD3, pomaga przekształcać silny androgen w formy słabsze. Gdy 3α-HSD3 jest nadmiernie aktywny, odbiera to ochronne działanie androgenów i pozostawia środowisko zdominowane przez estrogen, które sprzyja podziałom komórek nowotworowych i odporności na leczenie. Zablokowanie tego enzymu mogłoby zatem przywrócić równowagę hormonalną hamującą wzrost raka.
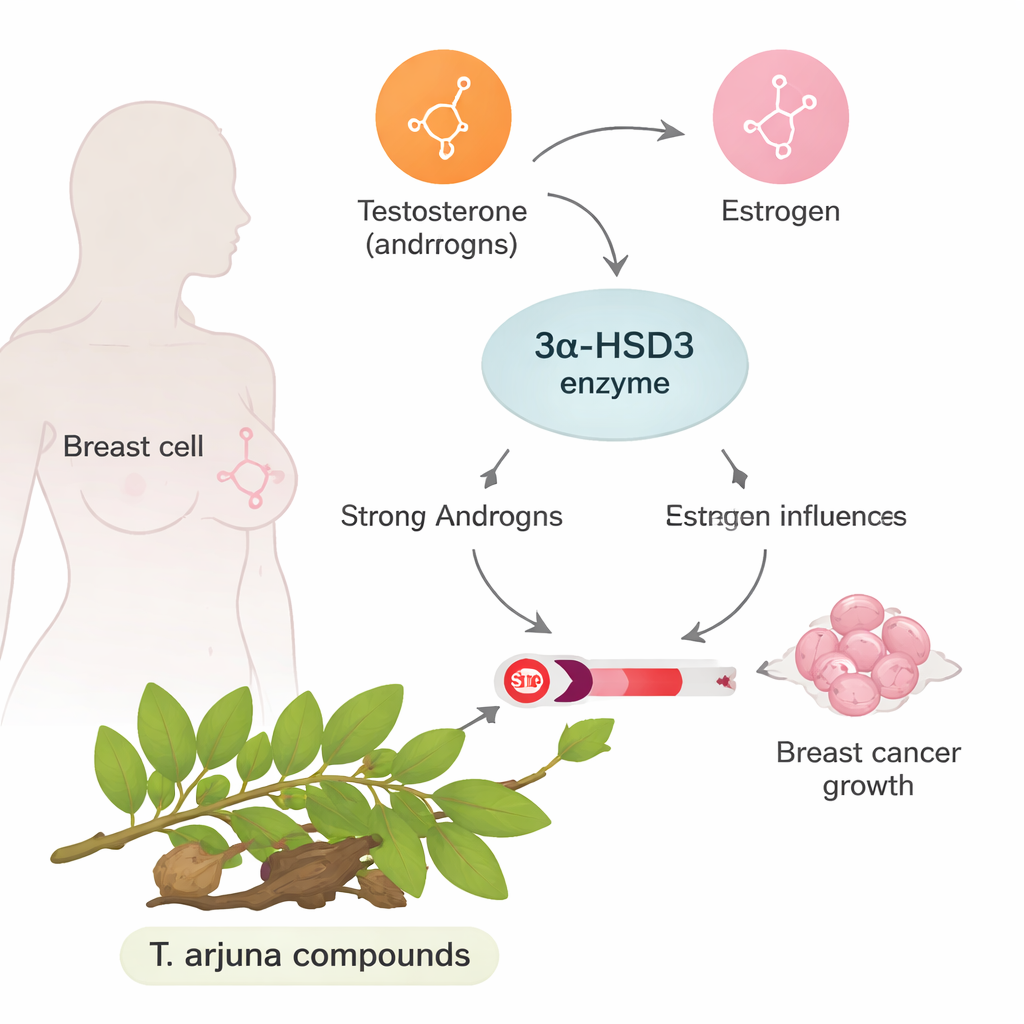
Obietnica tradycyjnego drzewa leczniczego
Terminalia arjuna to drzewo od dawna stosowane w medycynie tradycyjnej Azji Południowej, zwłaszcza dla zdrowia serca. Kora i inne części drzewa zawierają wiele związków roślinnych o zgłaszanych właściwościach przeciwutleniających i przeciwnowotworowych. Do tej pory żadnego z nich nie badano szczegółowo pod kątem działania na 3α-HSD3. Autorzy wybrali dziewięć dobrze znanych molekuł z tego drzewa, w tym flawonoidy i garbniki, na podstawie wcześniejszych doniesień o efektach przeciwnowotworowych i ochronnych. Zamiast od razu przechodzić do badań na zwierzętach lub pacjentach, najpierw użyli zestawu narzędzi komputerowo wspomaganego projektowania leków, aby odpowiedzieć na pytanie: które z tych naturalnych molekuł najprawdopodobniej dopasują się do enzymu i go zablokują, zachowają się jak realne leki w organizmie i unikną oczywistej toksyczności?
Symulowanie spotkania molekuł roślinnych z celem
Zespół rozpoczął od trójwymiarowej struktury ludzkiego 3α-HSD3, uprzednio rozwiązanej metodą krystalografii rentgenowskiej, i sprawdził jej jakość za pomocą standardowych testów strukturalnych. Następnie zbudowano i cyfrowo „zrelaksowano” kształty każdej molekuły roślinnej, aby odzwierciedlić realistyczne formy, jakie przyjmują w organizmie. Kolejnym krokiem było wirtualne dokowanie: komputer próbował wielu sposobów umieszczenia każdej molekuły w kieszeni aktywnej enzymu i oceniał, jak ciasno i korzystnie się wiązała. Kilka związków z Terminalia wykazało silne przewidywane wiązanie, często lepsze niż znany syntetyczny inhibitor odniesienia. Szczególnie wyróżniły się cztery: luteolina, leucocyjanidyna, kwas galusowy i kwas elagowy. Nie tylko przewidywano, że silnie się wiążą, ale także że tworzą wielokrotne wiązania wodorowe i inne stabilizujące kontakty z kluczowymi aminokwasami kontrolującymi aktywność enzymu.
Testowanie stabilności, zachowania i bezpieczeństwa in silico
Dokowanie daje migawkę; badacze następnie sprawdzili, czy kompleksy te pozostaną stabilne w czasie w wodnym, przypominającym ciało środowisku. Przeprowadzili 100-nanosekundowe symulacje dynamiki molekularnej — w praktyce filmy fizyczne atomów poruszających się w temperaturze ciała. Miary drgań białka i ligandów wykazały, że cztery molekuły roślinne pozostały mocno osadzone w kieszeni enzymu, często stabilizując ją bardziej niż lek kontrolny. Dodatkowe obliczenia oszacowały energie wiązania i potwierdziły, że luteolina, leucocyjanidyna i kwas galusowy w szczególności tworzą silne, korzystne interakcje. Równoległe modele komputerowe przewidziały, że wszystkie cztery kandydaty powinny być stosunkowo dobrze wchłanialne przez jelito, dobrze dystrybuować się w tkankach, unikać istotnych problemów z enzymami wątrobowymi i wykazywać niskie prawdopodobieństwo działania genotoksycznego lub uszkodzeń narządów przy dawkach terapeutycznych.
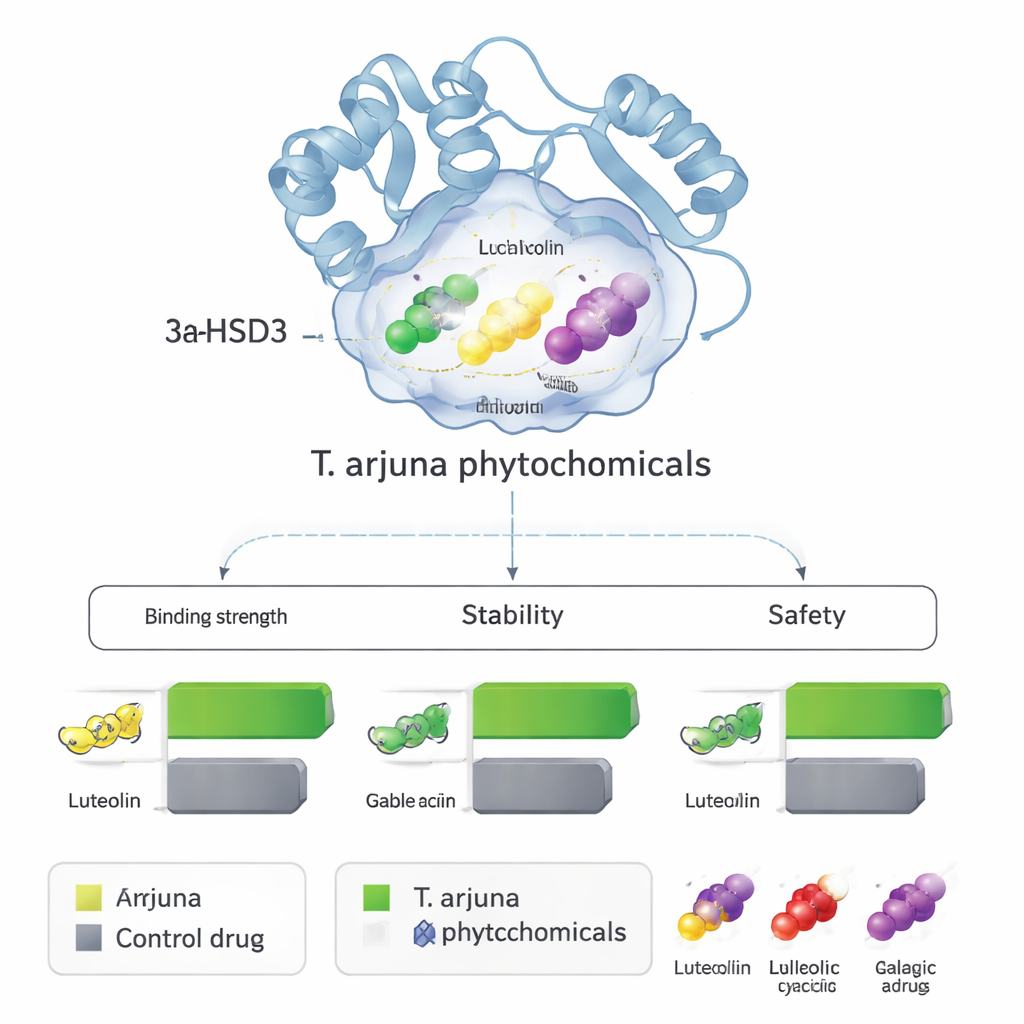
Od przewidywań komputerowych do przyszłych terapii
Dla osoby niezaznajomionej z tematem kluczowe przesłanie jest takie, że praca ta nie twierdzi, iż odkryto nowy lek, ale dostarcza skoncentrowanej krótkiej listy obiecujących związków naturalnych. Luteolina, leucocyjanidyna, kwas galusowy i kwas elagowy z Terminalia arjuna wydają się, na podstawie wielu niezależnych testów komputerowych, wiązać się z 3α-HSD3 i potencjalnie go blokować — enzymem, który przyczynia się do powstawania środowiska bogatego w estrogeny w komórkach raka piersi wrażliwych na hormony. Na papierze wyglądają również jak substancje mające cechy leku i stosunkowo bezpieczne. Kolejne niezbędne kroki to eksperymenty laboratoryjne, aby sprawdzić, czy te przewidywania się potwierdzą: czy związki te rzeczywiście hamują enzym w probówkach i czy realnie ograniczają wzrost komórek raka piersi bez szkody dla zdrowych tkanek? Jeśli tak, mogą posłużyć do projektowania ulepszonych pochodnych lub zainspirować nowe terapie skojarzone łączące tradycyjną wiedzę roślinną z nowoczesną nauką molekularną.
Cytowanie: Al Mashud, M.A., Rahman, M.A., Kumer, A. et al. Computational identification of Terminalia arjuna phytochemicals as potential 3α-HSD3 inhibitors. Sci Rep 16, 8045 (2026). https://doi.org/10.1038/s41598-026-37558-z
Słowa kluczowe: hormony raka piersi, Terminalia arjuna, naturalne inhibitory enzymów, komputerowo wspomagane projektowanie leków, luteolina kwas galusowy