Clear Sky Science · pl
Hybrydowe nowe ramy uczenia głębokiego do klasyfikacji choroby Parkinsona
Dlaczego to ma znaczenie dla pacjentów i rodzin
Choroba Parkinsona często zaczyna się od subtelnych zmian — spowolnienia ruchów, cichszego głosu lub słabego drżenia — które łatwo pomylić z normalnym procesem starzenia. W momencie, kiedy diagnoza staje się pewna, wiele uszkodzeń mózgu już miało miejsce. W tym badaniu przedstawiono komputerowe podejście, które analizuje skany mózgu, by wykrywać chorobę Parkinsona z bardzo wysoką dokładnością, nawet gdy objawy są jeszcze łagodne. Jeśli narzędzia tego typu będą godne zaufania i szeroko stosowane, mogą pomóc lekarzom w szybszym rozpoznaniu, wcześniejszym rozpoczęciu leczenia oraz dać pacjentom i rodzinom więcej czasu na planowanie.
Wgląd w mózg za pomocą inteligentnych skanów
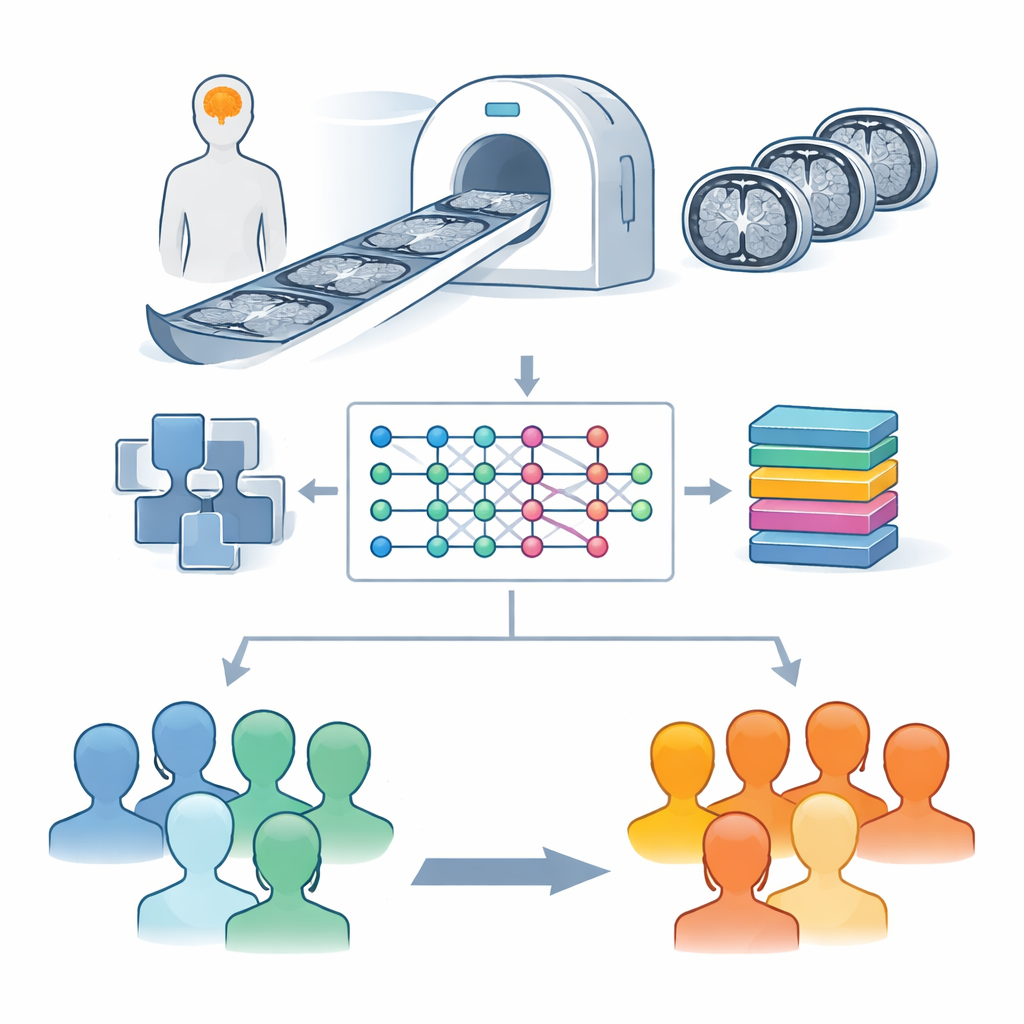
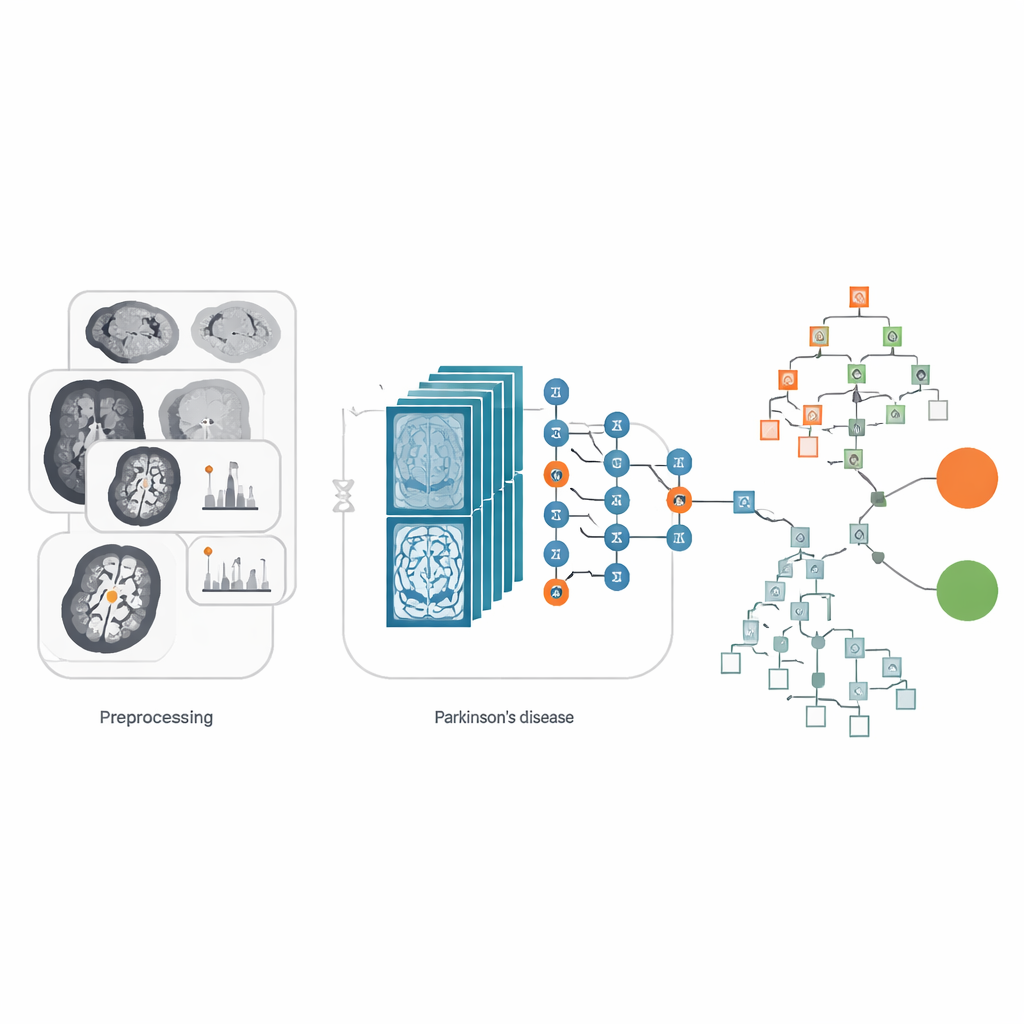
Naukowcy skupili się na obrazowaniu metodą rezonansu magnetycznego (MRI), badaniu powszechnym w szpitalach, które nie wiąże się z promieniowaniem. Wykorzystali dużą publiczną bazę obrazów mózgu z inicjatywy Parkinson’s Progression Markers Initiative, zawierającą skany osób z chorobą Parkinsona oraz zdrowych ochotników. Zamiast analizować cały trójwymiarowy obraz naraz, zespół pracował na przekrojach — „plastrach” mózgu, szczególnie w rejonie śródmózgowia, gdzie znajdują się komórki produkujące dopaminę. Komórki te są kluczowe dla płynności ruchu, a ich utrata jest znakiem charakterystycznym choroby Parkinsona. Aby ułatwić komputerowi „zauważenie” słabych struktur, obrazy najpierw przeszły staranną korektę standaryzującą jasność oraz wzmacniającą kontrast w istotnych obszarach.
Nauczanie modelu hybrydowego rozpoznawania wzorców
W centrum badania znajduje się system hybrydowy łączący dwie silne metody współczesnych technologii. Pierwszą jest sieć głębokiego uczenia EfficientNetB0, pierwotnie zaprojektowana do ogólnych zadań rozpoznawania obrazów. Tu działa jak wytrenowane oko, skanując każdy plaster mózgu i wydobywając subtelne wzorce kształtu i tekstury, które mogą różnić mózgi zdrowe od tych dotkniętych chorobą Parkinsona. Drugą jest metoda podejmowania decyzji znana jako XGBoost, która świetnie radzi sobie z wytyczaniem ostrych granic między kategoriami, gdy dysponuje informatywnymi cechami. W prostych słowach, EfficientNetB0 kondensuje każdy przekrój MRI do zwartego podpisu cech, a XGBoost wykorzystuje te podpisy, by zdecydować, czy skan należy do osoby zdrowej, czy chorej na Parkinsona, oraz czy obrazy pochodzą z konkretnego ustawienia MRI.
Równoważenie ograniczonych i niejednorodnych danych
Jednym z największych praktycznych problemów w medycznym AI jest to, że dane często są zarówno nieliczne, jak i niezrównoważone: może być znacznie więcej skanów od pacjentów niż od zdrowych ochotników lub odwrotnie. Tutaj zespół rozpoczął od skanów 77 osób zdrowych i 223 osób z Parkinsonem, co jest umiarkowaną liczbą dla uczenia głębokiego. Aby uniknąć uczenia systemu ukierunkowanego na jedną klasę, powiększyli zbiór obrazów w kontrolowany sposób. Każdy oryginalny przekrój mózgu został obrócony lub odbity, by odzwierciedlić małe różnice w ustawieniu głowy podczas rzeczywistych badań. Zastosowali też technikę wzmocnienia kontrastu zwaną CLAHE, która uwydatnia drobne detale bez przesadnego wzmacniania szumu. Takie ostrożne „rozciągnięcie” zestawu danych wygenerowało ponad 26 000 obrazów, dając modelowi wystarczającą różnorodność do nauki solidnych wzorców i zmniejszając ryzyko dopasowania do specyficznych cech oryginalnych skanów.
Jak dobrze działa system?
Aby ocenić niezawodność, badacze porównali kilka wersji swojego podejścia. Testowali trzy popularne sieci obrazowe — VGG16, ResNet50 i EfficientNetB0 — w trzech trybach: użyte „tak jak są”, dostrojone oraz połączone z etapem decyzyjnym XGBoost. W tych zestawieniach konfiguracje hybrydowe konsekwentnie wypadały najlepiej. Zwycięska konfiguracja, EfficientNetB0 plus XGBoost, poprawnie sklasyfikowała skany w 99,02 procent przypadków na zestawie testowym. Dobrze poradziła sobie ze wszystkimi czterema kategoriami: zdrowi i Parkinson, każda z obrazami z użyciem i bez użycia ustawienia MRI znanego jako FLAIR. Miary skupiające się na przypadkach przeoczonych i fałszywych alarmach, takie jak recall i F1-score, również były bardzo wysokie, co sugeruje, że narzędzie nie polega na wymianie jednego typu błędu na inny. Co ważne, model pozostał też efektywny pod względem czasu obliczeń, co czyni go bardziej realistycznym do zastosowań w zatłoczonych warunkach klinicznych.
Co to może znaczyć w praktyce klinicznej
Chociaż żaden system komputerowy nie zastąpi doświadczonego neurologa, praca ta pokazuje, że starannie zaprojektowany model hybrydowy może pełnić rolę potężnego asystenta. Szybko przeglądając rutynowe obrazy MRI w poszukiwaniu subtelnych oznak choroby Parkinsona, takie narzędzia mogłyby wskazywać pacjentów wymagających bliższej kontroli znacznie wcześniej, zanim objawy staną się oczywiste. Autorzy zastrzegają, że ich rozwiązanie wymaga jeszcze testów na większych i bardziej zróżnicowanych grupach pacjentów oraz w przyszłości połączenia z innymi informacjami, takimi jak testy ruchowe czy markery we krwi. Mimo to wyniki sugerują, że inteligentne oprogramowanie oparte na istniejących skanach szpitalnych mogłoby stać się szybkim, niskokosztowym i szeroko wdrażalnym sprzymierzeńcem we wczesnym wykrywaniu choroby Parkinsona.
Cytowanie: Desai, S., Vora, M., Shah, S. et al. Hybrid deep learning novel framework for classification of parkinson’s disease. Sci Rep 16, 9143 (2026). https://doi.org/10.1038/s41598-026-37553-4
Słowa kluczowe: Choroba Parkinsona, rezonans magnetyczny mózgu, uczenie głębokie, obrazowanie medyczne, wczesna diagnoza