Clear Sky Science · pl
Podejście z rozdzieloną ligazą biotynową ujawnia białka związane z oligomeryczną alfa-synukleiną podczas agregacji
Dlaczego skupiska białek w mózgu mają znaczenie
W chorobie Parkinsona i schorzeniach pokrewnych białko mózgowe zwykle pomocne, zwane alfa‑synukleiną, może zlepić się w lepkie depozyty znane jako ciała Lewy’ego. Te złogi pojawiają się na dziesięciolecia przed objawami i stanowią cechę rozpoznawczą widoczną w badaniu pośmiertnym, a mimo to wciąż nie wiemy, które inne białka przyczyniają się do przejścia alfa‑synukleiny ze stanu nieszkodliwego do formy agregującej. Badanie wykorzystuje sprytny molekularny „znacznik bliskości”, by zmapować, które białka znajdują się blisko alfa‑synukleiny, gdy przechodzi ona od pojedynczych cząsteczek do drobnych skupisk, dostarczając nowych wskazówek o tym, jak zaczyna się choroba i które szlaki mogą być celem spowolnienia lub zapobiegania jej rozwojowi.
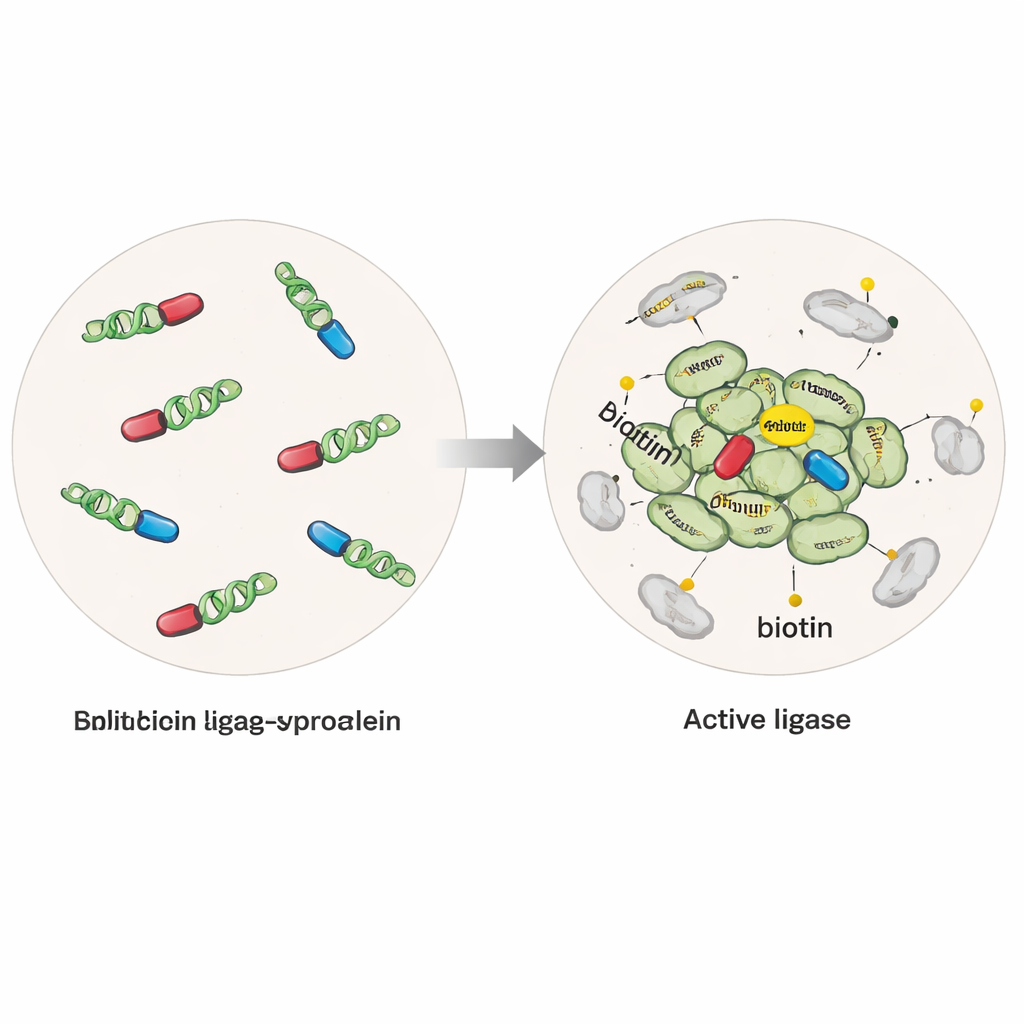
Molekularny „znacznik”, który oświetla sąsiadów
Naukowcy zaprojektowali komórki ludzkie produkujące alfa‑synukleinę złączoną z zmodyfikowaną enzymatyczną domeną, która może przyłączyć niewielką cząsteczkę biotyny do każdego białka w odległości kilku miliardowych części metra. W jednej wersji enzym był nienaruszony i aktywny zawsze, gdy obecna była alfa‑synukleina, znakując białka wokół pojedynczych cząsteczek i skupisk. W drugiej, bardziej selektywnej „rozdzielonej” wersji, enzym został przecięty na dwie nieaktywne połówki, z których każda była przyłączona do oddzielnej cząsteczki alfa‑synukleiny. Dopiero gdy cząsteczki alfa‑synukleiny łączyły się w multimery lub oligomery, połówki łączyły się ponownie w aktywny enzym, włączając znakowanie specyficznie wokół tych wczesnych agregatów. Dodając do komórek oczyszczone fibryle alfa‑synukleiny, zespół mógł też wymusić agregację przypominającą chorobową i porównać stany normalne z patologicznymi.
Budowanie mapy pobliskich białek
Po odczekaniu czasu potrzebnego na znakowanie zespół wyłapał wszystkie białka oznaczone biotyną i zidentyfikował je za pomocą spektrometrii mas, techniki, która z dużą precyzją waży i liczy białka. We wszystkich warunkach wykryto 1 277 odrębnych białek, a po starannym przefiltrowaniu zawężono listę do 581, które najprawdopodobniej rzeczywiście znajdowały się blisko alfa‑synukleiny. Porównując systemy z nienaruszonym i rozdzielonym enzymem, mogli rozróżnić białka kojarzące się głównie z pojedynczymi cząsteczkami od tych preferujących multimery. Porównali też komórki z dodanymi fibrylami i bez nich, aby zobaczyć, jak lokalne środowisko białkowe alfa‑synukleiny zmienia się po wyzwoleniu agregacji.
Kluczowe szlaki komórkowe wciągane do skupisk
Uzyskany szkic interaktomu wskazuje na kilka głównych motywów biologicznych. W warunkach normalnych multimerowa alfa‑synukleina znajdowała się blisko wielu białek zaangażowanych w transport błonowy i enzymów modyfikujących białka — zgodnie z przypuszczalną rolą w pomaganiu neuronom w zarządzaniu pęcherzykami synaptycznymi i utrzymaniu kontroli jakości białek. Kilka enzymów dodających grupy fosforanowe, w tym kinazy PAK4, RIPK2 i MAP4K4, było wzbogaconych przy zdrowych multimerach, ale wydawały się tracić kontakt po utworzeniu agregatów, co sugeruje, że zaburzenie tych relacji może sprzyjać formom białka związanym z chorobą. Zespół wykrył też białka związane z sygnalizacją insulinopodobnego czynnika wzrostu, co potwierdza kliniczne powiązania między insulinoopornością a chorobą Parkinsona, oraz stwierdził, że agregacja rekrutuje białka uczestniczące w usuwaniu uszkodzonych białek, takie jak rodzina chaperonów 14‑3‑3 i określone składniki szlaków degradacyjnych komórki.
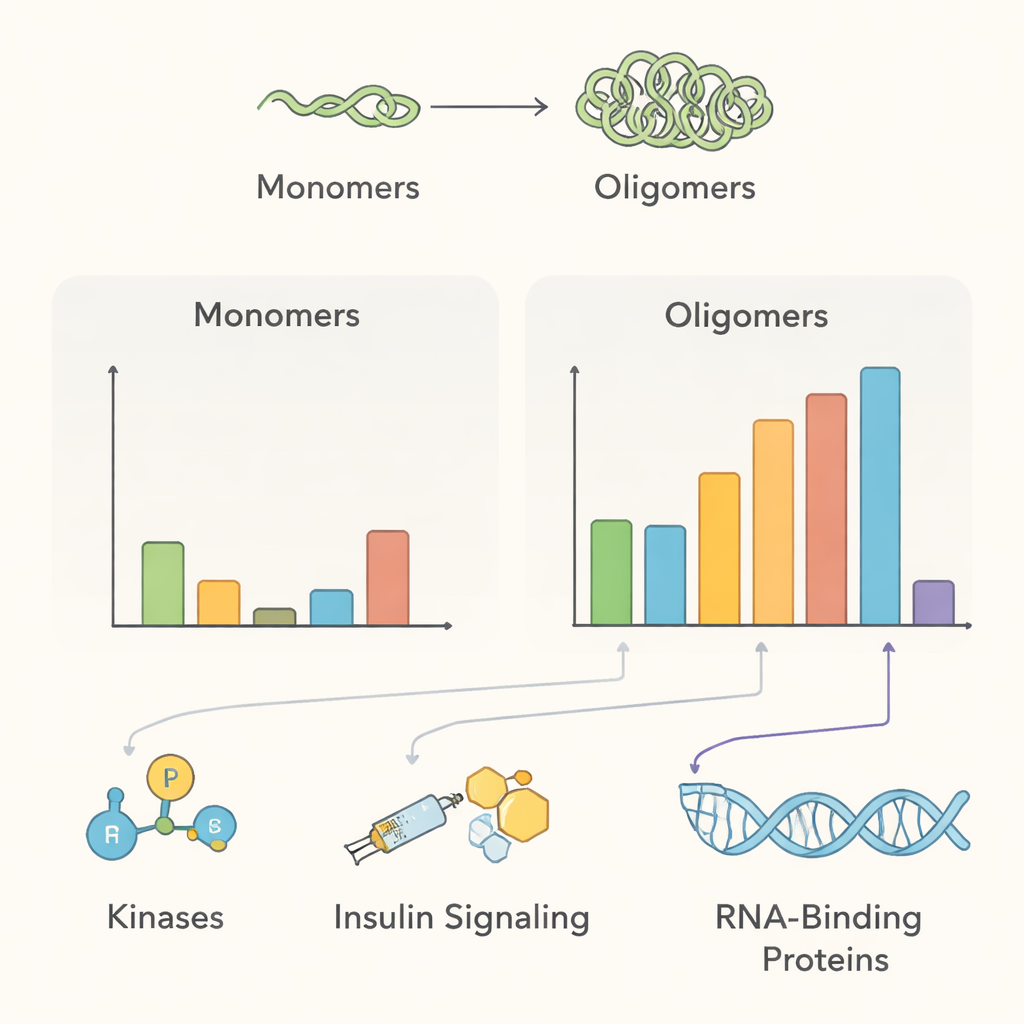
Niespodziewane mosty do innych chorób mózgu
Ponad chorobą Parkinsona dane uwypuklają zaskakujące powiązanie z stwardnieniem zanikowym bocznym (ALS) i otępieniem czołowo‑skroniowym (FTD). Białko wiążące RNA o nazwie FUS, które w tych schorzeniach ulega zmylokalizowaniu i agregacji, pojawiało się blisko multimerowej alfa‑synukleiny zarówno w warunkach normalnych, jak i napędzanych agregacją. Inne białka związane z RNA również zmieniały swoją bliskość w miarę agregacji alfa‑synukleiny. Odkrycia te sugerują możliwość, że małe zespoły alfa‑synukleiny mogą zatrzymywać białka zajmujące się RNA w niewłaściwym miejscu w komórkach, potencjalnie łącząc biologię chorób z ciałami Lewy’ego z mechanizmami ALS i FTD, choć bezpośrednie fizyczne interakcje wciąż wymagają potwierdzenia.
Co to oznacza dla rozumienia choroby
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że ta praca dostarcza wstępnej „listy kontaktów” białek towarzyszących alfa‑synukleinie, gdy przechodzi ona z roli normalnego pomocnika do szkodliwego skupiska. Badanie sugeruje, że utrata niektórych ochronnych relacji — na przykład z określonymi kinazami czy enzymami kontroli jakości — może być równie istotna jak pozyskanie nowych toksycznych partnerów. Choć eksperymenty przeprowadzono w uproszczonym modelu komórkowym i nie dowodzą jeszcze związku przyczynowo‑skutkowego, wskazują konkretne kandydatury i szlaki do dalszych badań w neuronach i tkance mózgowej. W dłuższej perspektywie mapowanie tych zmieniających się sąsiedztw białkowych mogłoby ukierunkować strategie przywracania ochronnych interakcji, wspierania sygnalizacji związanej z insuliną lub zapobiegania uchwyceniu białek wiążących RNA, co potencjalnie spowolniłoby przejście od subtelnych zmian molekularnych do pełnoobjawowych chorób związanych z ciałami Lewy’ego.
Cytowanie: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Słowa kluczowe: alfa-synukleina, choroba ciał Lewy’ego, agregacja białek, proximity proteomics, choroba Parkinsona