Clear Sky Science · pl
Kowalencyjne unieruchamianie peroksydazy Lepidium draba na chitozanem pokrytych nanocząstkach magnetycznych i jej zastosowanie w biosensing'u glukozy
Dlaczego drobne magnesy mają znaczenie dla poziomu cukru we krwi
Utrzymanie poziomu glukozy pod kontrolą jest kluczowe przy zarządzaniu cukrzycą i zapobieganiu długoterminowym uszkodzeniom serca, nerek, oczu i nerwów. Dzisiejsze testy glukozy działają dobrze, ale enzymy w nich używane bywają kruche, mają krótką żywotność i trudno je ponownie wykorzystać, co podnosi koszty i generuje odpady. W tym badaniu zbadano sprytne rozwiązanie, które może uczynić enzym roślinny bardziej odpornym i trwalszym przez zamocowanie go na mikroskopijnych magnetycznych kulkach, otwierając drogę do szybszych, bardziej niezawodnych i potencjalnie tańszych testów glukozy.
Roślinny pomocnik inspirowany chrzanem
Wiele testów medycznych opiera się na enzymach — białkach przyspieszających reakcje chemiczne. Powszechnie stosowaną „robotą” w laboratoriach diagnostycznych jest peroksydaza z chrzanu, używana do zamiany niewidocznych zmian chemicznych w wyraźne zmiany koloru widoczne gołym okiem. Naukowcy pracowali z bliskim krewnym tego enzymu, peroksydazą Lepidium draba, produkowaną w bakteriach, aby umożliwić wytwarzanie w dużych ilościach. Samodzielnie ten wolny enzym jest wydajny, ale delikatny: traci aktywność pod wpływem ciepła, podczas przechowywania i przy wielokrotnym użyciu, co ogranicza jego zastosowanie w czujnikach przemysłowych i zestawach klinicznych.
Przekształcanie enzymów w magnetyczne narzędzia
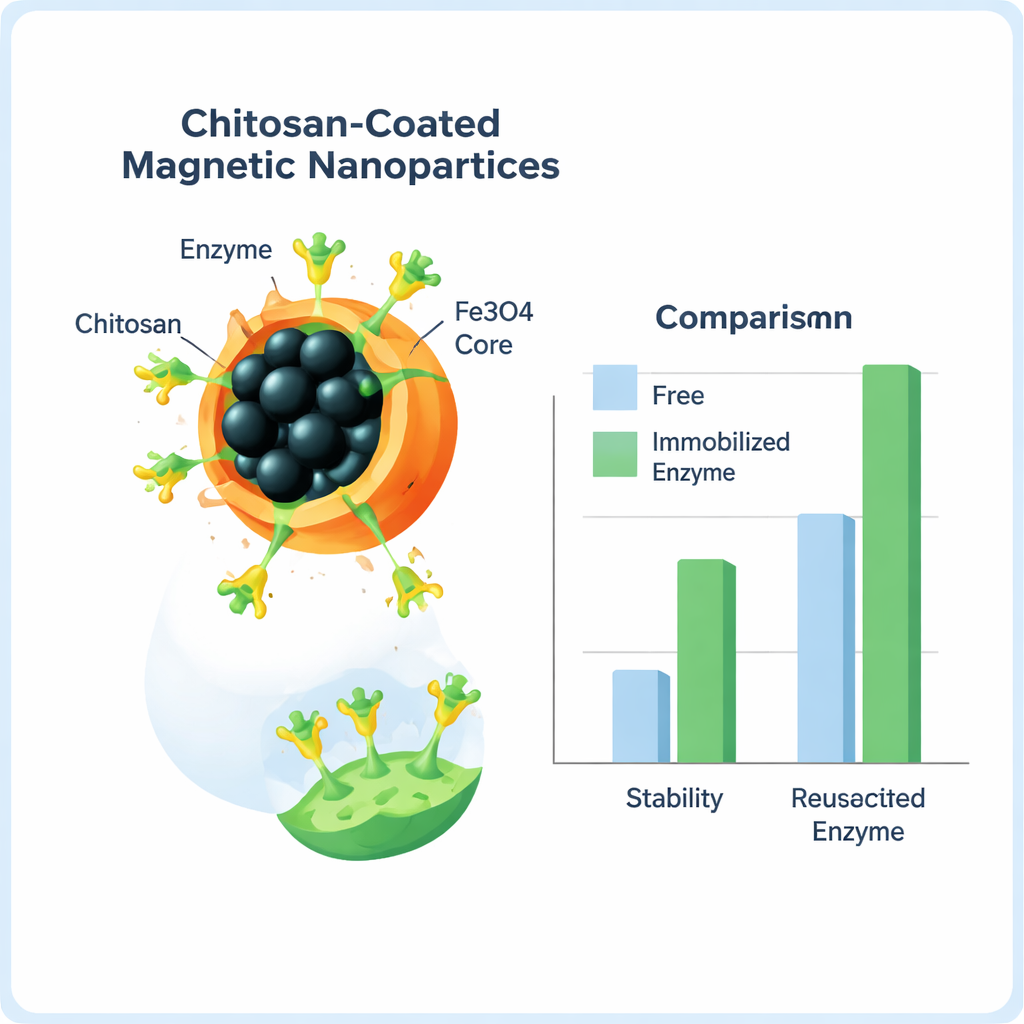
Aby chronić enzym i móc go ponownie użyć, zespół przyłączył go do nanocząstek tlenku żelaza — maleńkich ziarenek materiału magnetycznego — powleczonych naturalnym polimerem zwanym chitozanem, pozyskiwanym ze skorup skorupiaków. Chitozan zapewnia miękką, biokompatybilną powłokę pełną chemicznych „uchwytów”, które mogą wiązać enzymy. Przy użyciu małocząsteczkowego środka sieciującego, glutaraldehydu, utworzono silne wiązania kowalencyjne między enzymem a powlekanymi cząstkami. Naukowcy następnie dopracowali ilość użytego środka sieciującego, czas reakcji i ilość nośnika, wybierając warunki dające najlepszą równowagę między ilością zaadsorbowanego enzymu a zachowaniem jego aktywności.
Sprawdzanie struktury, wytrzymałości i trwałości
Po unieruchomieniu zespół potwierdził, że enzym rzeczywiście osadził się na cząstkach, stosując kilka narzędzi strukturalnych odczytujących wibracje wiązań, wzory krystaliczne i kształt powierzchni. Co ważniejsze dla zastosowań praktycznych, unieruchomiony enzym zachowywał się lepiej niż jego wolna forma. Lepiej wiązał swój barwiący substrat i przekształcał go w produktów barwny znacznie efektywniej — w niektórych testach aż do 11-krotnie wyższa efektywność katalityczna. Enzym związany tolerował też szerszy zakres kwasowości, utrzymywał wyższą aktywność w przydatnym zakresie temperatur i dłużej wytrzymywał ogrzewanie w 50 °C. Jego półokres rozpadu w tej temperaturze się więcej niż podwoił, a po dwóch miesiącach przechowywania w lodówce zachował mniej więcej dwukrotnie więcej aktywności niż enzym wolny. Dzięki magnetycznym cząstkom można było je wyciągnąć z roztworu magnesem i użyć ponownie; nawet po 11 cyklach reakcji pozostało około 40% początkowej aktywności.
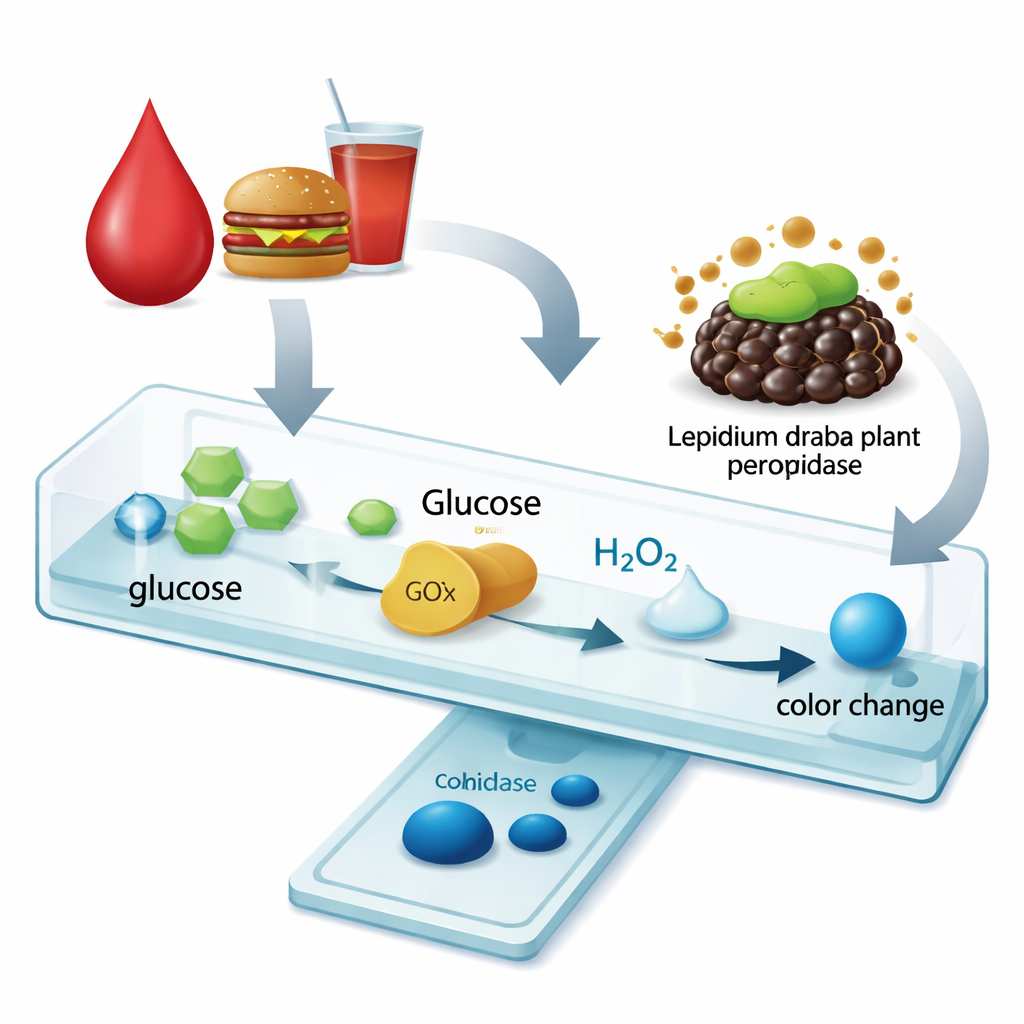
Wyraźniejsza zmiana barwy w testach na glukozę
Aby sprawdzić, czy ten bardziej trwały enzym rzeczywiście poprawia praktyczny test, badacze zbudowali prosty test kolorymetryczny glukozy. Najpierw standardowy enzym oksydaza glukozowa przekształca glukozę w nadtlenek wodoru. Następnie peroksydaza Lepidium draba, w formie wolnej lub unieruchomionej na magnetycznych kulkach z chitozanem, wykorzystuje ten nadtlenek do przekształcenia bezbarwnego barwnika w intensywnie niebieski. W przypadku formy unieruchomionej użyteczny zakres pomiarowy dla glukozy znacznie się poszerzył — z 0,1–1 mmol/l dla enzymu wolnego do 0,1–10 mmol/l po unieruchomieniu. Jednocześnie czas reakcji potrzebny do testu skurczył się do około jednej trzeciej, podczas gdy minimalny wykrywalny poziom glukozy pozostał bardzo niski i klinicznie istotny.
Co to oznacza dla codziennego zdrowia
Poprzez zakotwiczenie enzymu roślinnego na chitozanem pokrytych nanocząstkach magnetycznych autorzy stworzyli solidny, wielokrotnego użytku i wysoce czuły element czujnika kolorymetrycznego glukozy. Dla laika oznacza to, że przyszłe paski testowe, zestawy laboratoryjne, a nawet inteligentne opakowania żywności mogą stać się bardziej stabilne, dokładniejsze w szerszym zakresie stężeń cukru i potencjalnie tańsze, ponieważ aktywny enzym można odzyskać i użyć ponownie. Chociaż potrzebne są dalsze prace, aby zwiększyć ładowność enzymu na cząstkach i rozszerzyć podejście na inne markery krwi, takie jak cholesterol czy mocznik, badanie pokazuje, jak nanomateriały i naturalne polimery mogą współdziałać, by przekształcić znane narzędzia biochemiczne w bardziej wytrzymałe, czystsze i wszechstronne systemy diagnostyczne.
Cytowanie: Sepahi-Baghan, M., Asoodeh, A. & Riahi-Madvar, A. Covalent immobilization of Lepidium draba peroxidase on chitosan-coated magnetic nanoparticles and its application in glucose biosensing. Sci Rep 16, 7035 (2026). https://doi.org/10.1038/s41598-026-37542-7
Słowa kluczowe: biosensor glukozy, unieruchamianie enzymów, nanocząstki magnetyczne, detekcja kolorymetryczna, peroksydaza