Clear Sky Science · pl
TIPE2 pełni rolę korzystnego biomarkera prognostycznego i hamuje rozwój raka dróg żółciowych poprzez oddziaływanie na transport integryny αvβ6 zależny od RAC1
Dlaczego ten rzadki nowotwór dróg żółciowych ma znaczenie
Cholangiocarcinoma, czyli rak dróg żółciowych wewnątrz i wokół wątroby, jest rzadki, lecz wyniszczający. Większość pacjentów trafia do rozpoznania w zaawansowanym stadium, zabieg chirurgiczny jest rzadko możliwy, a przeżycie pięcioletnie dotyczy mniej niż jednej na dwadzieścia osób. Lekarzom pilnie potrzeba lepszych narzędzi do przewidywania, którzy pacjenci rokować będą gorzej, oraz nowych podejść terapeutycznych. W tym badaniu odkryto cząsteczkę nazwaną TIPE2, która zarówno pomaga prognozować wyniki, jak i wydaje się hamować wzrost i rozsiew tego nowotworu.
Wbudowany hamulec, który zanika
TIPE2 to białko najlepiej znane z działania uspokajającego układ odpornościowy, zapobiegając nadmiernym reakcjom zapalnym. Autorzy zastanawiali się, czy może ono pełnić także funkcję naturalnego hamulca w komórkach dróg żółciowych, które przekształcają się w komórki nowotworowe. Zbadali próbki guzów od dużej grupy 218 pacjentów po operacji z powodu cholangiocarcinoma oraz drugiej, niezależnej grupy 95 chorych. Przy użyciu immunohistochemii — metody barwienia pokazującej poziom określonego białka w tkance — zmierzyli poziomy TIPE2 w guzach i przylegającej niezmienionej tkance dróg żółciowych.
Mniej TIPE2, bardziej agresywne guzy
We wszystkich obu grupach pacjentów TIPE2 było konsekwentnie niższe w tkance nowotworowej niż w normalnych przewodach żółciowych. Co więcej, im mniej TIPE2 występowało w guzie, tym częściej był on bardziej zaawansowany i agresywny. Niski poziom TIPE2 wiązał się z większymi guzami, zajęciem pobliskich węzłów chłonnych, naciekaniem naczyń krwionośnych oraz wyższym ogólnym stadium choroby. Kiedy zespół obserwował pacjentów w czasie, osoby z niskim TIPE2 umierały wcześniej niż pacjenci, których guzy wykazywały wyższe jego ilości. Analizy statystyczne wykazały, że TIPE2 jest niezależnym predyktorem przeżycia, nawet po uwzględnieniu standardowych miar, takich jak rozmiar guza i status węzłów chłonnych.
Przekształcenie biomarkera w narzędzie kliniczne
Aby ich ustalenia miały praktyczne zastosowanie przy łóżku chorego, badacze zbudowali „nomogram” — wizualne narzędzie punktacji łączące kilka czynników ryzyka w jedną prognozę. W tym wykresie rozmiar guza, zajęcie węzłów chłonnych, naciekanie naczyń oraz poziom TIPE2 każdego pacjenta są przeliczane na punkty szacujące prawdopodobieństwo przeżycia po jednym, trzech i pięciu latach od operacji. Model działał lepiej niż sam konwencjonalny system TNM, co sugeruje, że dodanie barwienia TIPE2 do rutynowych opisów patologicznych mogłoby poprawić zdolność lekarzy do informowania pacjentów i wyboru dalszego postępowania.
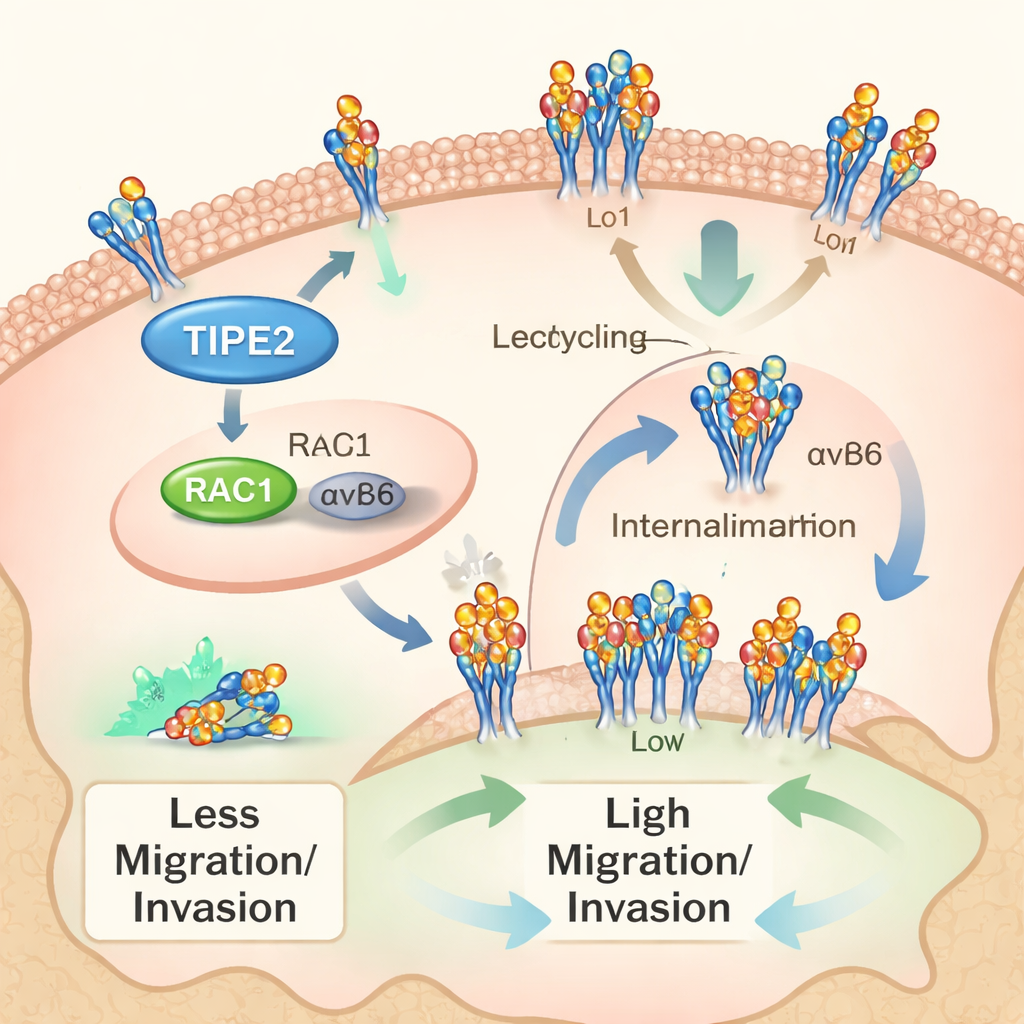
Jak TIPE2 powstrzymuje komórki nowotworowe
Ponad aspektem prognostycznym, zespół badał, jak TIPE2 wpływa na zachowanie komórek nowotworowych. W eksperymentach laboratoryjnych na ludzkich liniach komórkowych cholangiocarcinoma sztuczne obniżenie TIPE2 powodowało szybszy wzrost komórek oraz zwiększoną zdolność do przemieszczania się i inwazji przez sztuczne membrany. Zwiększenie poziomu TIPE2 miało efekt odwrotny — spowalniało podziały komórek i osłabiało ich zdolność do migracji i penetrowania barier. U myszy wszczepionych komórkami raka dróg żółciowych dostarczanie dodatkowego TIPE2 bezpośrednio do guzów zmniejszało ich rozmiar i masę, co pokazuje, że TIPE2 hamuje wzrost guza zarówno in vivo, jak i in vitro.
Problem z ruchem na powierzchni komórki
Badanie skoncentrowało się na innym graczu — integrynie αvβ6, cząsteczce adhezyjnej na powierzchni komórek, która pomaga komórkom nowotworowym przyczepiać się i przebudowywać otoczenie, sprzyjając inwazji i rozsiewowi. Badacze wcześniej wykazali, że αvβ6 jest obficie obecna i patologiczna w cholangiocarcinoma. Tutaj skupili się na „transportowaniu” αvβ6 — jej ciągłej internalizacji do wnętrza komórki i recyklingu z powrotem na powierzchnię. Za pomocą biochemicznych testów śledzących wykazali, że ten proces przemieszczania jest aktywny w komórkach raka dróg żółciowych i że blokowanie internalizacji hamuje wzrost i inwazyjność komórek. Odkryli, że TIPE2 zaburza zarówno internalizację, jak i recykling αvβ6, zmniejszając liczbę i ruchliwość tych cząsteczek na powierzchni komórki.
Kluczowy molekularny przełącznik: RAC1
Powiązując te elementy, istotną rolę pełni RAC1, mały molekularny przełącznik kontrolujący ruch komórek i przemieszczanie białek błonowych. Autorzy pokazali, że hamowanie RAC1 spowalnia transport αvβ6, podobnie jak robi to TIPE2. Wcześniejsze prace ujawniły, że TIPE2 może wiązać RAC1 i hamować jego aktywność. Modelowanie komputerowe w tym badaniu zasugerowało fizyczne kontakty między TIPE2, RAC1 i ogonem integryny αvβ6. Kiedy zespół użył zmienionej formy TIPE2, która nie może prawidłowo wchodzić w interakcję z RAC1, jej zdolność do spowolnienia wzrostu i inwazji komórek nowotworowych w dużej mierze zniknęła. Podobnie, gdy komórki były wstępnie traktowane lekiem blokującym RAC1, dodanie dodatkowego TIPE2 przynosiło znacznie mniejszą korzyść. Razem te wyniki wspierają ścieżkę, w której TIPE2 ujarzmia RAC1, co z kolei redukuje transport αvβ6 i agresywne zachowanie komórek cholangiocarcinoma.
Co to znaczy dla pacjentów
Dla osób niebędących specjalistami przekaz jest dwojaki. Po pierwsze, barwienie TIPE2 w próbkach guza mogłoby dać lekarzom jaśniejszy obraz tego, jak niebezpieczny jest dany rak dróg żółciowych, poprawiając prognozowanie ponad obecne systemy stagingowe. Po drugie, samo TIPE2 oraz szlak RAC1–αvβ6, który ono reguluje, wskazują nowe kierunki terapeutyczne: zwiększenie aktywności TIPE2 lub bezpośrednie celowanie w RAC1 bądź αvβ6 może pomóc spowolnić ten zwykle śmiertelny nowotwór. Choć terapie takie będą wymagać dalszych badań i testów klinicznych, praca ta wyznacza obiecującą drogę do bardziej precyzyjnej i skutecznej opieki nad pacjentami z cholangiocarcinoma.
Cytowanie: Wang, S., Jia, W., Sun, Y. et al. TIPE2 serves as a favorable prognostic biomarker and suppresses cholangiocarcinoma progression by targeting RAC1-mediated integrin αvβ6 trafficking. Sci Rep 16, 6638 (2026). https://doi.org/10.1038/s41598-026-37540-9
Słowa kluczowe: cholangiocarcinoma, TIPE2, biomarker, integrin αvβ6, RAC1