Clear Sky Science · pl
Interakcja impulsowego pola elektromagnetycznego niskiej częstotliwości (PEMF) z mitochondriami
Łagodne pola i elektrownie komórkowe
Terapia impulsowym polem elektromagnetycznym (PEMF) jest już stosowana w klinikach w celu wspomagania zrostu kości, łagodzenia bólu stawów i przyspieszania rekonwalescencji po operacjach. Nadal jednak nie rozumiemy w pełni, w jaki sposób te łagodne, niskoczęstotliwościowe pola działają w naszych organizmach. W badaniu postawiono proste, lecz istotne pytanie: czy sygnały PEMF bezpośrednio wpływają na mitochondria — maleńkie elektrownie komórek wytwarzające większość naszej energii — i jeśli tak, to w jaki sposób?
Dlaczego mitochondria mają znaczenie dla codziennego zdrowia
Mitochondria przekształcają pożywienie i tlen w cząsteczkę ATP, uniwersalną „walutę energetyczną” komórek. Kiedy mitochondria zawodzą, tkanki goją się wolniej, mięśnie szybciej się męczą, a choroby związane z zaburzeniami metabolizmu mogą się pogorszyć. Ponieważ wcześniejsze badania sugerowały, że zabiegi PEMF poprawiają metabolizm energetyczny i wspierają naprawę tkanek, autorzy skoncentrowali się na tym, czy określone urządzenie PEMF może wyregulować aktywność mitochondriów. Użyli dobrze zdefiniowanego sygnału magnetycznego: krótkich, milisekundowych impulsów fali sinusoidalnej o częstotliwości 30 kHz i niskiej energii wejściowej, stosowanych do komórek mięśniowych w hodowli, tkanek szczurzych oraz do oczyszczonych mitochondriów.
Uważne spojrzenie do wnętrza żywych komórek
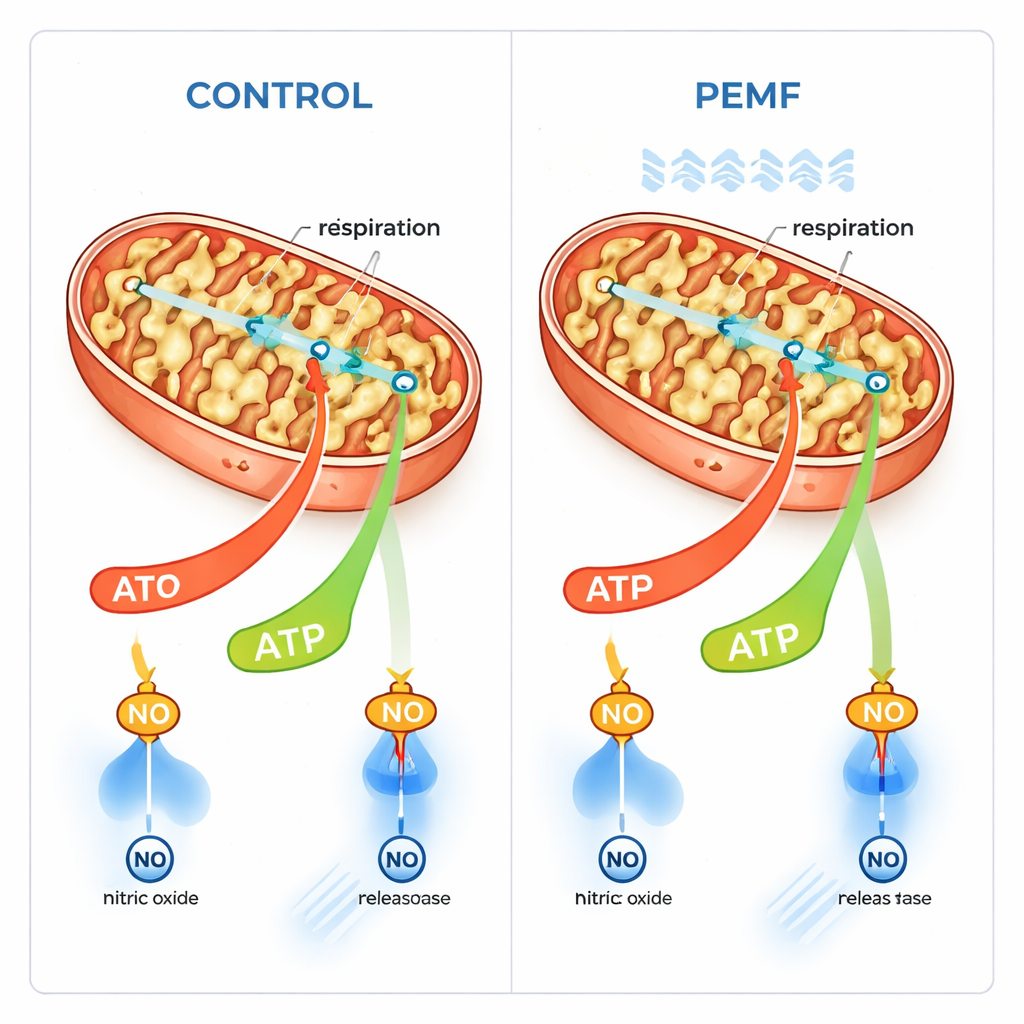
W ludzkich komórkach mięśniowych hodowanych w laboratorium zespół zmierzył trzy kluczowe wskaźniki po ekspozycji na PEMF: potencjał elektryczny przez wewnętrzną błonę mitochondrialną (rodzaj maleńkiej baterii), poziomy reaktywnych form tlenu (wysokie poziomy mogą być szkodliwe) oraz tlenek azotu, gaz mogący tymczasowo blokować oddychanie mitochondriów. Około 90 minut po zabiegu potencjał błonowy mitochondriów był nieznacznie niższy, podczas gdy poziomy tlenku azotu były zmniejszone; reaktywne formy tlenu nie wzrosły. Niewielki spadek potencjału błonowego może oznaczać uszkodzenie lub intensywniejszą produkcję ATP. Ponieważ komórki nie wykazywały oznak stresu, autorzy przypuszczali, że mitochondria po prostu pracowały nieco szybciej i zużywały zgromadzony potencjał przez wewnętrzną błonę.
Testowanie, jak mitochondria „oddychają”
Aby sprawdzić ten pomysł bardziej bezpośrednio, badacze delikatnie naruszyli zewnętrzną błonę komórkową, tak by precyzyjnie dostarczać mitochondriom różne paliwa i mierzyć zużycie tlenu. Konsekwentnie obserwowali tendencję do zwiększonego oddychania związanego z produkcją ATP po ekspozycji na PEMF, zwłaszcza gdy obecny był glutaminian — powszechne paliwo mitochondrialne. Analiza statystyczna wielu próbek sugerowała, że kombinacja ekspozycji na PEMF i wyboru paliwa istotnie kształtowała tempo zużycia tlenu przez mitochondria. Co ważne, nie stwierdzono oznak, że PEMF szkodziły komórkom lub ich mitochondriom. Zamiast tego pola wydawały się selektywnie pobudzać tryb oddechowy „sprzężony”, w którym zużycie tlenu jest ściśle powiązane z wytwarzaniem ATP, bez zwiększania marnotrawnego, niesprzężonego spalania paliwa.
Zapalenie, tlenek azotu i niespodzianka od niebieskiego światła
Ponieważ tlenek azotu może gromadzić się w czasie zapalenia i blokować kluczowy etap mitochondrialnego „oddychania”, zespół zapytał, czy PEMF może pomóc mitochondriom odzyskać sprawność po takim zahamowaniu. Dodali chemiczny donor tlenku azotu do homogenatów mięśniowych i wątrobowych oraz do izolowanych mitochondriów wątroby, co silnie spowolniło oddychanie. W tych warunkach PEMF nie przywróciły funkcji mitochondrialnej, nawet gdy mitochondria były silnie skoncentrowane. Aby sprawdzić, czy blokada jest w ogóle odwracalna, naśladowali znaną metodę i naświetlili światłem niebieskim mitochondria zahamowane przez tlenek azotu — światło to częściowo usunęło tlenek azotu z miejsca wiązania i częściowo przywróciło oddychanie, potwierdzając, że system może się zregenerować. PEMF nie dawały jednak dodatkowej korzyści. Pokazało to, że pozytywne efekty PEMF nie wynikają z usuwania tlenku azotu w warunkach podobnych do zapalnych.
Bramy błonowe i przepływ energii
Korzystając z analogii między komórkami a obwodami elektrycznymi, autorzy sugerują, że PEMF mogą działać głównie na biologiczne błony. Mitochondria otacza błona zewnętrzna zawierająca kluczowy białkowy „węzeł bramowy” o nazwie VDAC, który pozwala związkom związanym z energią przechodzić do wnętrza i na zewnątrz. W przeciwieństwie do bardzo wysokiego napięcia wewnętrznej błony, zewnętrzna błona ma mniejsze, łatwiej podatne na wpływy napięcie. Autorzy proponują, że PEMF subtelnie zmienia to napięcie zewnętrzne, przesuwając częstość otwarć bramek VDAC i w ten sposób ułatwiając przepływ paliwa i zużytego ATP przez błonę. To naturalnie zwiększałoby sprzężony, produkujący ATP tryb oddychania bez zmiany maksymalnej wydajności samego łańcucha transportu elektronów.
Co to oznacza dla przyszłych terapii
Podsumowując, badanie nie znajduje dowodów, że tego typu PEMF są szkodliwe dla mitochondriów. Wręcz przeciwnie — PEMF łagodnie wzmacniają tę część mitochondrialnego oddechu, która produkuje ATP, pozostawiając niezmienioną maksymalną pojemność oddechową i stres oksydacyjny. Nie przywracają jednak mitochondriów zablokowanych przez wysoki poziom tlenku azotu, co sugeruje, że ich korzyści w tkankach zapalnych muszą wynikać z innych mechanizmów. Dla pacjentów i klinicystów wyniki te wspierają ideę, że starannie dobrane pola elektromagnetyczne mogą skłonić „elektrownie” komórkowe do bardziej efektywnego, produkującego energię stanu — oferując wiarygodne, mechanistyczne wyjaśnienie niektórych efektów leczniczych obserwowanych przy naprawie kości, leczeniu ran i rekonwalescencji po operacjach.
Cytowanie: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Słowa kluczowe: terapia impulsowym polem elektromagnetycznym, mitochondria, energia komórkowa, tlenek azotu, produkcja ATP