Clear Sky Science · pl
Weryfikacja nowego biomarkera genomowego skaliowalności komórek macierzystych mezenchymalnych i implikacje statusu genotypu dla fenotypów starzenia komórkowego
Dlaczego hodowla komórek macierzystych staje się trudniejsza z czasem
Komórki macierzyste z dorosłej szpiku kostnego są podstawą wielu eksperymentalnych terapii — od naprawy uszkodzonych kości po tłumienie stanów zapalnych. Jest jednak haczyk: by leczyć pacjenta, laboratoria muszą namnażać te komórki poza organizmem, a im dłużej są one ekspandowane, tym wolniej się dzielą i zaczynają zachowywać się jak komórki „zestarzałe”. W badaniu zbadano, dlaczego komórki niektórych osób starzeją się wolniej w hodowli i czy mały brak fragmentu DNA może pomóc naukowcom wybrać najbardziej odporne komórki do przyszłych terapii.
Brakujący gen, który zmienia zasady
Naukowcy skupili się na genie o nazwie GSTT1, który pomaga komórkom detoksykować szkodliwe cząsteczki powstające podczas normalnego metabolizmu i stresu. Co zaskakujące, znaczna część populacji całkowicie nie ma tego genu — są „GSTT1 null”. Wcześniejsze badania sugerowały, że komórki macierzyste ze szpiku od takich osób mogą szybciej rosnąć i zachowywać dłuższe chroniące chromosomy czapeczki, zwane telomerami. W tym projekcie zespół przebadał komórki od sześciu zdrowych dawców, podzielił je na grupy GSTT1‑dodatnie i GSTT1‑null, a następnie śledził zachowanie komórek podczas wielu cykli namnażania i po ekspozycji na promieniowanie rentgenowskie, silny czynnik wywołujący starzenie komórkowe.
Szybko rosnące komórki odporne na sygnały starzenia
Gdy naukowcy obserwowali liczbę komórek przez kilka dni, komórki GSTT1‑null mnożyły się szybciej we wczesnych pasażach niż komórki z obecnym genem. Przy bardzo długiej ekspansji tempo wzrostu w grupach stało się bardziej podobne, ale wczesna przewaga była wyraźna. Aby zbadać starzenie bezpośrednio, zespół użył klasycznego barwienia, które barwi komórki senescentne, czyli „zestarzałe”, na niebiesko. Po wielu podziałach, a także po naświetleniu, hodowle GSTT1‑null konsekwentnie zawierały mniej niebieskich, senescentnych komórek niż hodowle GSTT1‑dodatnie. Co ważne, różnica ta nie wynikała z wolniejszego skracania telomerów ani z wyższej aktywności enzymu utrzymującego telomery (hTERT); oba wskaźniki wyglądały podobnie niezależnie od statusu GSTT1, co sugeruje działanie innego mechanizmu.
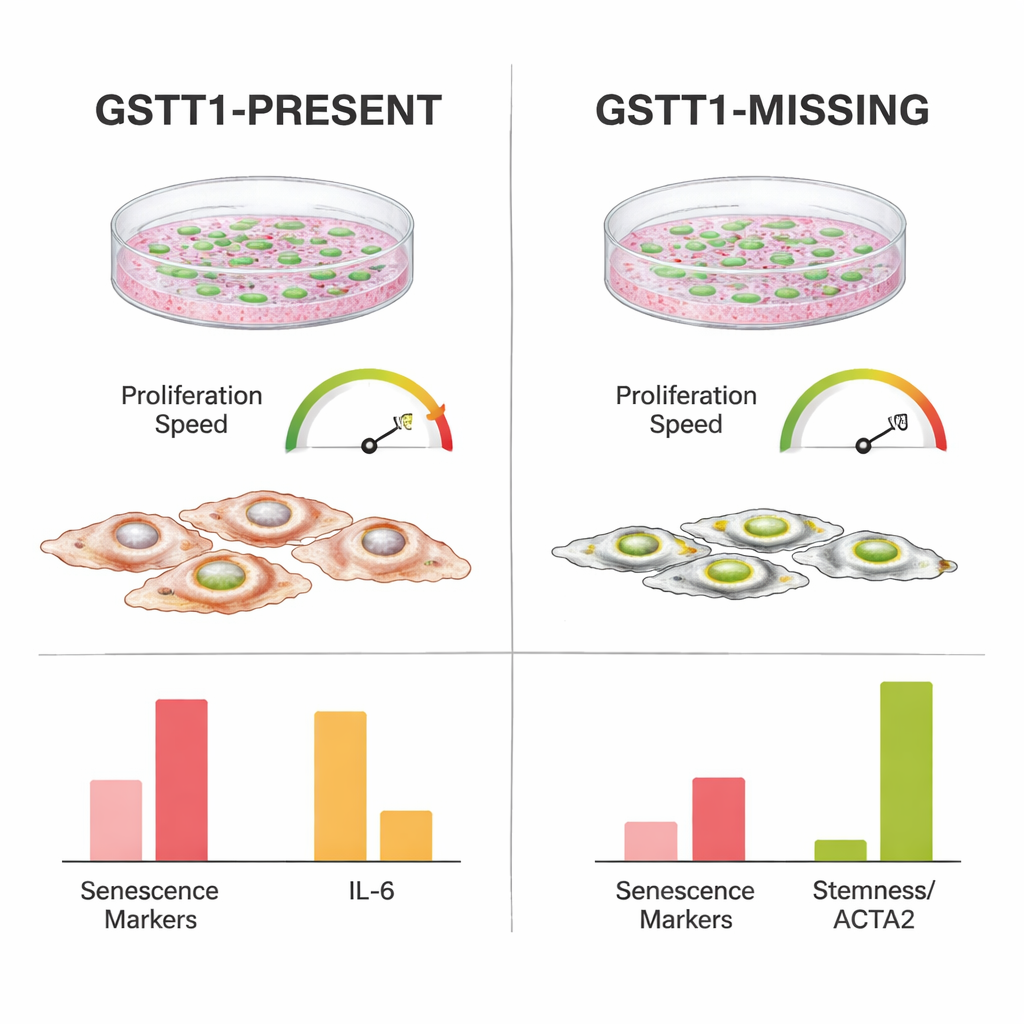
Mniejszy stres i zapalenie w hodowli
Aby zrozumieć, co czyni komórki GSTT1‑null bardziej odpornymi, badacze zmierzyli aktywność genów powiązanych z zatrzymaniem cyklu komórkowego, uszkodzeniem DNA i tzw. fenotypem wydzielniczym związanym z senescencją — koktajlem sygnałów zapalnych i stresowych uwalnianych przez starzejące się komórki. Komórki z obecnym GSTT1 wykazywały wyższe poziomy kluczowych sygnałów „stop”, takich jak p21 i p14, szczególnie w późniejszych pasażach i po naświetleniu. Silniej zwiększały też ekspresję IL‑6, silnej cząsteczki zapalnej, oraz innych genów związanych ze stresem niż komórki GSTT1‑null. W przeciwieństwie do tego, komórki macierzyste GSTT1‑null utrzymywały niższe poziomy tych markerów starzenia i zapalenia, jednocześnie zachowując wyższe poziomy ACTA2 i TWIST1 — genów związanych z integralnością strukturalną i cechami macierzystymi. Co istotne, obie grupy genotypowe zachowały podobną zdolność do różnicowania w kierunku komórek kostnych i tłuszczowych, co oznacza, że efekt ochronny nie wynikał po prostu z utraty normalnej funkcji komórek macierzystych.
Co to może znaczyć dla przyszłych terapii komórkowych
Wyniki sugerują, że komórki macierzyste ze szpiku pozbawione GSTT1 są częściowo chronione przed typowym zużyciem wynikającym z ekspansji w laboratorium i napromieniania. Rośną szybciej na początku, gromadzą mniej jawnie zestarzałych komórek i utrzymują mniej zapalny profil, mimo że ich chromosomy skracają się w podobnym tempie. Dla firm i klinik produkujących duże ilości komórek macierzystych status GSTT1‑null mógłby służyć jako praktyczny marker genetyczny do identyfikacji dawców, których komórki lepiej tolerują ekspansję, co potencjalnie prowadzi do bardziej spójnych i silniejszych terapii. Oczywiście badanie objęło niewielką grupę dawców i warunki hodowli niekliniczne, więc potrzebne są większe, starannie kontrolowane badania. Mimo to praca podkreśla, jak jedna odziedziczona różnica może przesunąć równowagę między młodzieńczym a starzejącym się zachowaniem komórek macierzystych hodowanych dla medycyny regeneracyjnej.
Cytowanie: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Słowa kluczowe: komórki macierzyste mezenchymalne, starzenie komórkowe, biomarkery, produkcja terapii komórkowych, polimorfizm GSTT1