Clear Sky Science · pl
Klinicznie zastosowalny i uogólnialny model głębokiego uczenia dla guzów przedniego śródpiersia w obrazach TK z wielu placówek
Dlaczego wykrywanie rzadkich guzów klatki piersiowej ma znaczenie
Większość z nas nigdy nie usłyszy w przychodni określenia „guz przedniego śródpiersia”, właśnie dlatego że te zmiany — często dotyczące grasicy przed sercem — są rzadkie. Gdy się jednak pojawią, trudno je rozpoznać, a jeszcze trudniej precyzyjnie zmierzyć na skanach TK; zadania te zwykle wymagają specjalistów z dużych ośrodków onkologicznych. Badanie to sprawdza, czy starannie wytrenowany system sztucznej inteligencji (SI) może pomóc lekarzom w wielu szpitalach wiarygodnie wykrywać i obrysowywać te trudne do zauważenia guzy na rutynowych obrazach TK, co potencjalnie poprawi diagnostykę i planowanie leczenia u pacjentów, którzy inaczej mogliby zostać przeoczeni.
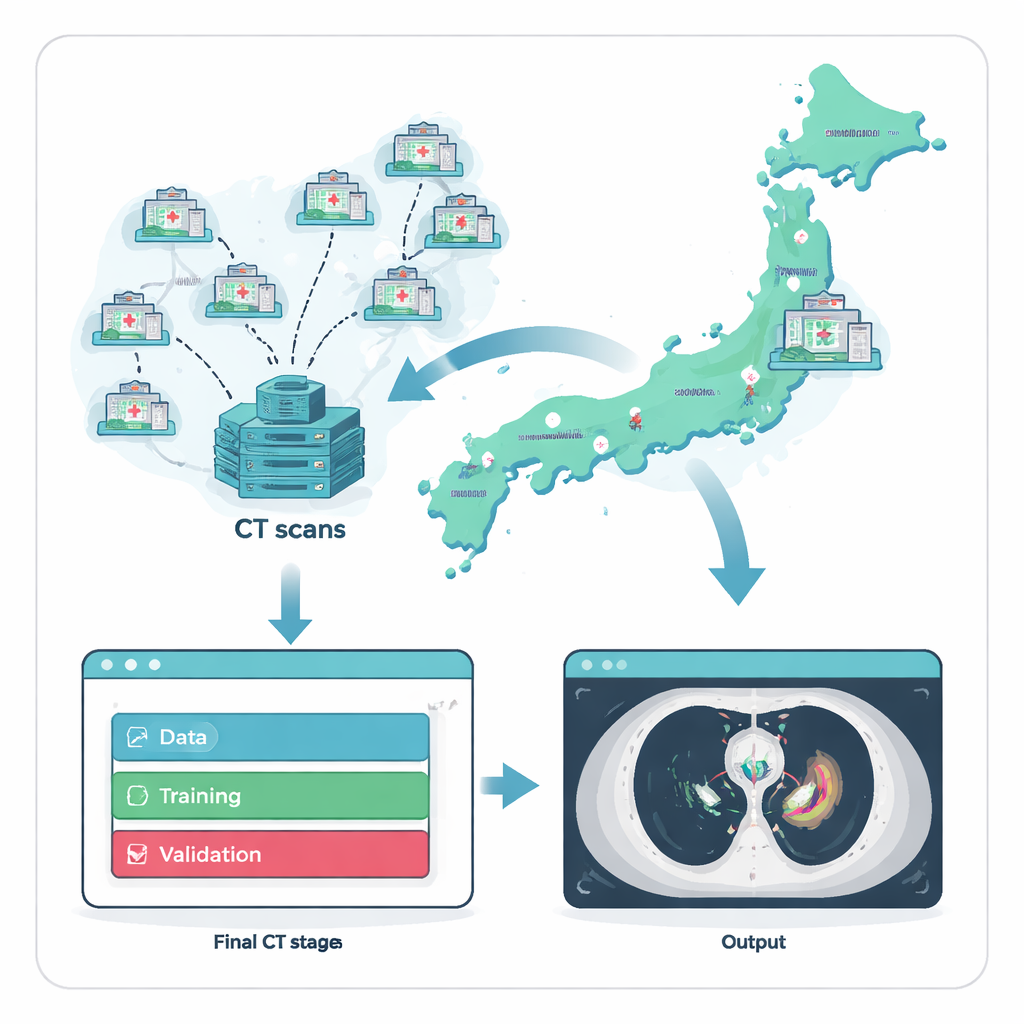
Zbieranie rzadkich przypadków z całego kraju
Ponieważ guzy przedniego śródpiersia są nieczęste, pierwszą przeszkodą jest po prostu znalezienie wystarczającej liczby przykładów do wytrenowania SI. Badacze poradzili sobie z tym, współpracując z Narodowym Centrum Onkologii w Japonii oraz 135 szpitalami odsyłającymi z całego kraju. W ciągu dwóch dekad zgromadzili 711 skanów TK klatki piersiowej, każdy od innego dorosłego pacjenta, u którego rozpoznanie guza potwierdzono mikroskopowo. Aby zapewnić uczciwy i realistyczny test, dane podzielono na trzy grupy: dużą do treningu, mniejszą do dopracowania i całkowicie oddzielny zewnętrzny zestaw testowy składający się z 164 skanów pochodzących z 121 szpitali, które nie dostarczyły żadnych obrazów do treningu. Takie rygorystyczne rozdzielenie odtwarza sytuację, gdy system zostaje wdrożony w nowych szpitalach, których nigdy wcześniej „nie widział”.
Przekształcanie skanów w wiarygodny materiał uczący
Model SI jest tyle wart, ile przykłady, na których się uczy, dlatego zespół włożył dużo pracy w profesjonalne oznaczanie danych. Dla każdego skanu TK specjaliści odrysowali dokładne granice guzów w przedniej części klatki piersiowej. Chirurg klatki piersiowej lub technik radiologii wykonał wstępne obrysowanie, które następnie sprawdzili dwaj doświadczeni radiolodzy diagnostyczni. Wszelkie niezgodności rozstrzygano przez dyskusję, tworząc wysokiej jakości odniesienie odzwierciedlające interpretację ekspertów w praktyce. Korzystając z komercyjnej platformy no-code do AI, klinicyści — bez pisania kodu komputerowego — zbudowali i wytrenowali trójwymiarowy model naśladujący te eksperckie obrysowania, co pozwoliło personelowi medycznemu bezpośrednio kierować procesem rozwoju.
Jak SI widzi guzy w trzech wymiarach
Rdzeń systemu stanowi trójwymiarowa wersja architektury sieci neuronowej znanej jako U-Net, zaprojektowana do analizowania całych wolumenów TK zamiast pojedynczych przekrojów. Przyjmuje stos obrazów klatki piersiowej i dla każdego małego elementu objętości przewiduje, czy należy on do guza czy do tkanki prawidłowej, efektywnie malując 3D maskę na guzie. Podczas treningu model był wystawiany na losowe rotacje, skalowanie i przycinanie obrazów, aby stał się odporny na niewielkie różnice w pozycji pacjenta i ustawieniach aparatu. Badacze następnie mierzyli, jak blisko przewidywane przez model obszary guzów pokrywają się z rysunkami ekspertów, używając standardowych miar nakładania, które premiują zarówno dokładne wyznaczenie granic, jak i pełne objęcie objętości guza.
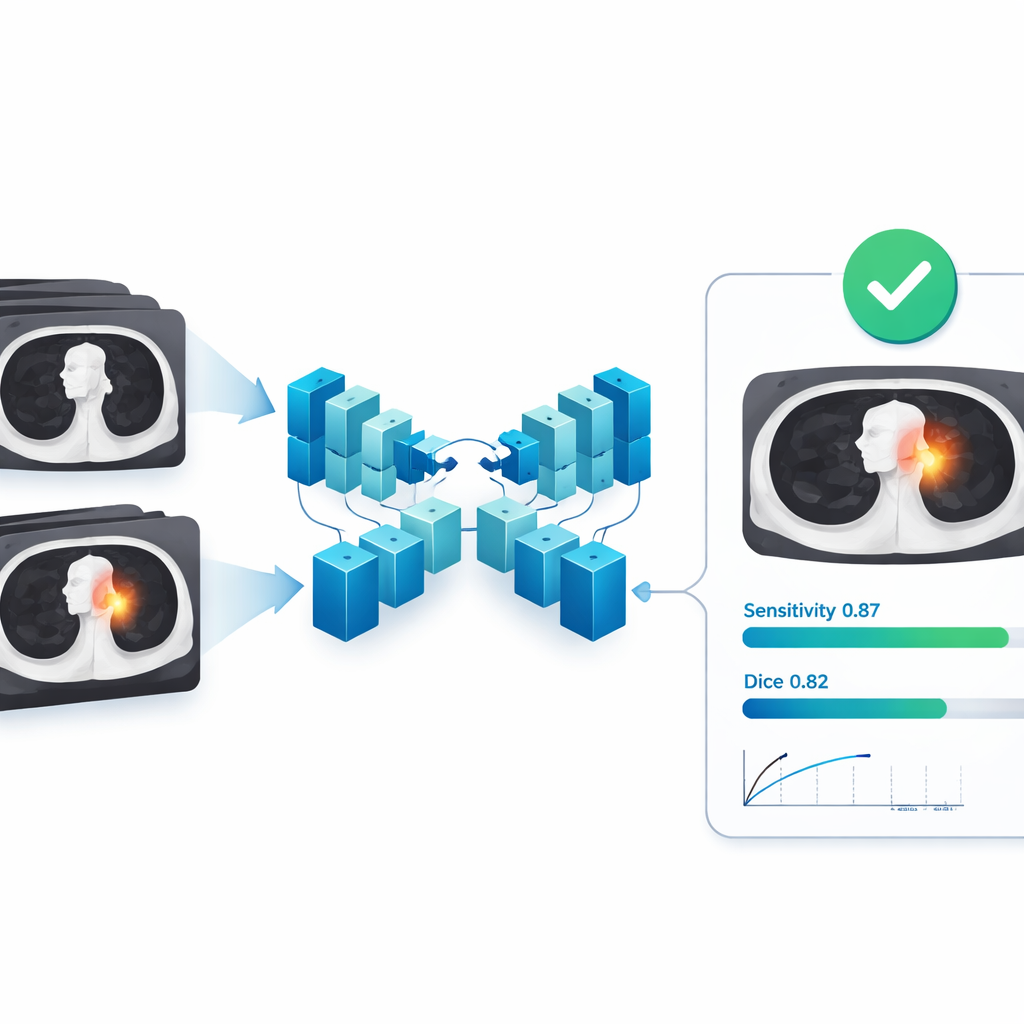
Wyniki w wielu szpitalach i dla różnych typów guzów
W zewnętrznym zestawie testowym pochodzącym z 121 niezależnych szpitali model SI wykazał silną zgodność z eksperckimi segmentacjami. Średnio jego wskaźnik nakładania (Dice) wyniósł 0,82, a powiązany miernik Intersection over Union 0,72; precyzja i czułość były w przybliżeniu na poziomie 0,82–0,85, co oznacza, że model rzadko błędnie oznaczał tkankę prawidłową jako guz i skutecznie obejmował większość tkanki guzowej. Co ważne, wyniki te utrzymywały się niezależnie od producenta tomografu, rozmiaru guza i jego typu, co sugeruje, że system radzi sobie z różnorodnością spotykaną w klinikach. Oceniany również jako wykrywacz — pytany po prostu, czy w ogóle znajdzie każde ognisko — model osiągnął czułość około 0,87 nawet przy rygorystycznej regule dopasowania, przy mniej niż jednej fałszywej alarmie na skan w średniej, profil atrakcyjny zwłaszcza do wsparcia badań przesiewowych w onkologii.
Gdzie system pomaga, a gdzie ludzie pozostają kluczowi
Bliższa analiza sukcesów i porażek ujawniła wyraźny wzorzec: SI najlepiej radziła sobie z większymi guzami, a miała trudności z bardzo małymi lub słabo widocznymi zmianami, które częściowo pomijała lub myliła z pobliskimi strukturami normalnymi, takimi jak naczynia krwionośne czy nagromadzenia płynu. Zgodne jest to z codziennym doświadczeniem w radiologii, gdzie drobne lub niskokontrastowe zmiany najłatwiej przeoczyć. Autorzy argumentują, że narzędzie najlepiej stosować w trybie „człowiek w pętli” (human-in-the-loop). Może służyć jako efektywny pierwszy czytelnik, który oznacza prawdopodobne guzy i obrysowuje ich granice, dostarczając gotowe objętości do zadań takich jak planowanie leczenia czy zabiegu, podczas gdy radiolodzy skupiają uwagę na ponownej weryfikacji małych, subtelnych lub niejednoznacznych obszarów.
Co to oznacza dla pacjentów i przyszłych narzędzi
Dla laika zasadnicze przesłanie jest takie, że system SI wytrenowany na rzadkiej, lecz poważnej grupie guzów klatki piersiowej może wiarygodnie pomagać lekarzom w znajdowaniu i obrysowywaniu tych nowotworów na skanach TK, nawet w szpitalach, które nigdy nie dostarczyły danych do treningu. Dzięki dostarczaniu dokładnych trójwymiarowych map guzów i utrzymywaniu niskiego poziomu fałszywych alarmów model może przyspieszyć diagnostykę, wspierać precyzyjniejsze planowanie radioterapii i zabiegów chirurgicznych oraz stanowić dodatkową sieć bezpieczeństwa przeciwko przeoczonym ogniskom. Jednocześnie praca podkreśla, że SI nie zastąpi fachowego osądu — zwłaszcza w przypadku najmniejszych i najsłabszych zmian — lecz jest obiecującym asystentem, który zyskuje na wartości, gdy łączy się ekspertów, dane obrazowe i łatwe w użyciu platformy AI.
Cytowanie: Takemura, C., Miyake, M., Kobayashi, K. et al. A clinically applicable and generalizable deep learning model for anterior mediastinal tumors in CT images across multiple institutions. Sci Rep 16, 6774 (2026). https://doi.org/10.1038/s41598-026-37504-z
Słowa kluczowe: guzy przedniego śródpiersia, głębokie uczenie w obrazowaniu TK, segmentacja obrazów medycznych, wsparcie diagnostyki nowotworowej, sztuczna inteligencja w radiologii