Clear Sky Science · pl
Wyjątkowo selektywne blokowanie czujnika napięcia kanałów NaV1.5 przez Mg-protoporfirynę zaburza migrację komórek nowotworowych
Barwnik roślinny wskazuje nową strategię przeciwnowotworową
Nasze serca i guzy mogą mieć zaskakującą wspólną słabość: specjalny rodzaj elektrycznych wrót w błonie komórkowej zwany NaV1.5. Badanie pokazuje, że naturalny krewny budulców chlorofilu u roślin, magnez‑protoporfiryna IX (MgPpIX), potrafi zamknąć te wrota z niezwykłą precyzją. W efekcie wyraźnie spowalnia ruch niektórych komórek nowotworowych — co sugeruje, że cząsteczka inspirowana chemią fotosyntezy mogłaby pomóc okiełznać przerzuty bez silnego zakłócania funkcji mózgu czy mięśni.
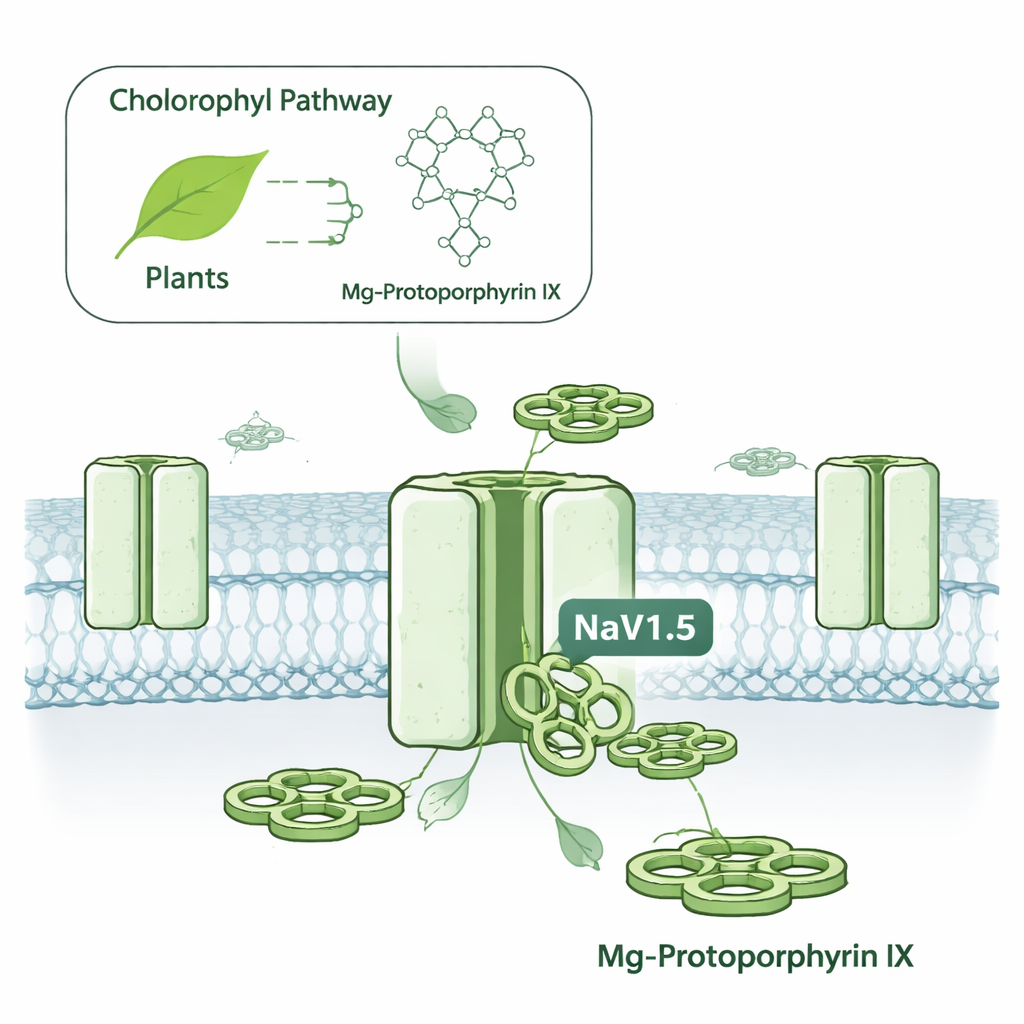
Ukryty elektryczny przełącznik w komórkach nowotworowych
Komórki używają napięciowo zależnych kanałów sodowych jako maleńkich drzwi, które otwierają się i zamykają, by przepuszczać naładowane cząstki, generując sygnały elektryczne. NaV1.5 jest najlepiej znany z roli w skurczach serca, gdzie pomaga wywołać każdy skurcz. Ten sam kanał występuje jednak także w kilku nowotworach, w tym w guzach piersi i jelita grubego, gdzie jego aktywność powiązano ze zwiększoną zdolnością komórek do przemieszczania się i naciekania. Celowanie w NaV1.5 było trudne, ponieważ większość leków na kanały sodowe uderza też w pokrewne kanały w nerwach i mięśniach szkieletowych, niosąc ryzyko działań niepożądanych, takich jak drgawki, drętwienie czy osłabienie mięśni. Autorzy postanowili sprawdzić, czy jakiekolwiek małe cząsteczki potrafią wyróżnić NaV1.5 spośród jego krewnych z dużo większą selektywnością.
Bloker zainspirowany rośliną o rekordowej precyzji
Zespół przebadał rodzinę pierścieniowych cząsteczek zwanych metalowymi protoporfirynami, które przypominają rdzenie hemu we krwi i chlorofilu u roślin, lecz zawierają różne jądrowe atomy metalu. Gdy zastosowali różne wersje do ludzkich kanałów NaV1.5 wytworzonych w hodowlach komórkowych, jedna substancja wyróżniła się: MgPpIX. Redukowała prąd elektryczny przepływający przez NaV1.5 o około 99% w stężeniach nanomolowych, czyli w przybliżeniu 100 razy silniej niż odpowiednik zawierający żelazo (hemina). Inne wersje metaliczne, na przykład z niklem czy miedzią, były praktycznie nieaktywne. Co istotne, MgPpIX nie wpływała w tych samych dawkach na kilka innych typów ludzkich kanałów sodowych (używanych w mózgu, nerwach obwodowych i mięśniach szkieletowych), co czyni jej selektywność jedną z najostrzejszych odnotowanych dla tej rodziny kanałów.
Jak cząsteczka blokuje maleńką dźwignię napięciową
Aby zrozumieć tę niezwykłą precyzję, badacze połączyli modyfikacje genetyczne z symulacjami komputerowymi. Kanały sodowe składają się z czterech powtarzających się części, z których każda zawiera „czujnik napięcia”, przemieszczający się, gdy zmienia się potencjał błonowy. Poprzez zamianę pojedynczych aminokwasów między NaV1.5 a jej niewrażliwymi krewnymi, zespół przypisał działanie MgPpIX do czujnika napięcia w drugiej domenie, a zwłaszcza do dwóch reszt wystawionych na zewnątrz komórki. Symulacje dynamiki molekularnej w realistycznym środowisku błonowym zasugerowały, że MgPpIX układa się przy tym czujniku, gdy znajduje się on w pozycji spoczynkowej, „w dół”. Dodatnio naładowane jądro metalu MgPpIX przyciąga ujemnie naładowany łańcuch boczny w kanale, podczas gdy płaski pierścień wchodzi w interakcje z otaczającymi lipidami. To wiązanie wydaje się blokować czujnik napięcia, uniemożliwiając jego przesunięcie do aktywnej pozycji „w górę” i utrzymując kanał zamknięty. Co interesujące, silne depolaryzacje — jak te podczas bicia serca — mogą tymczasowo wypychać cząsteczkę, zachowanie opisane przez autorów jako „odwrotna zależność od użycia”.
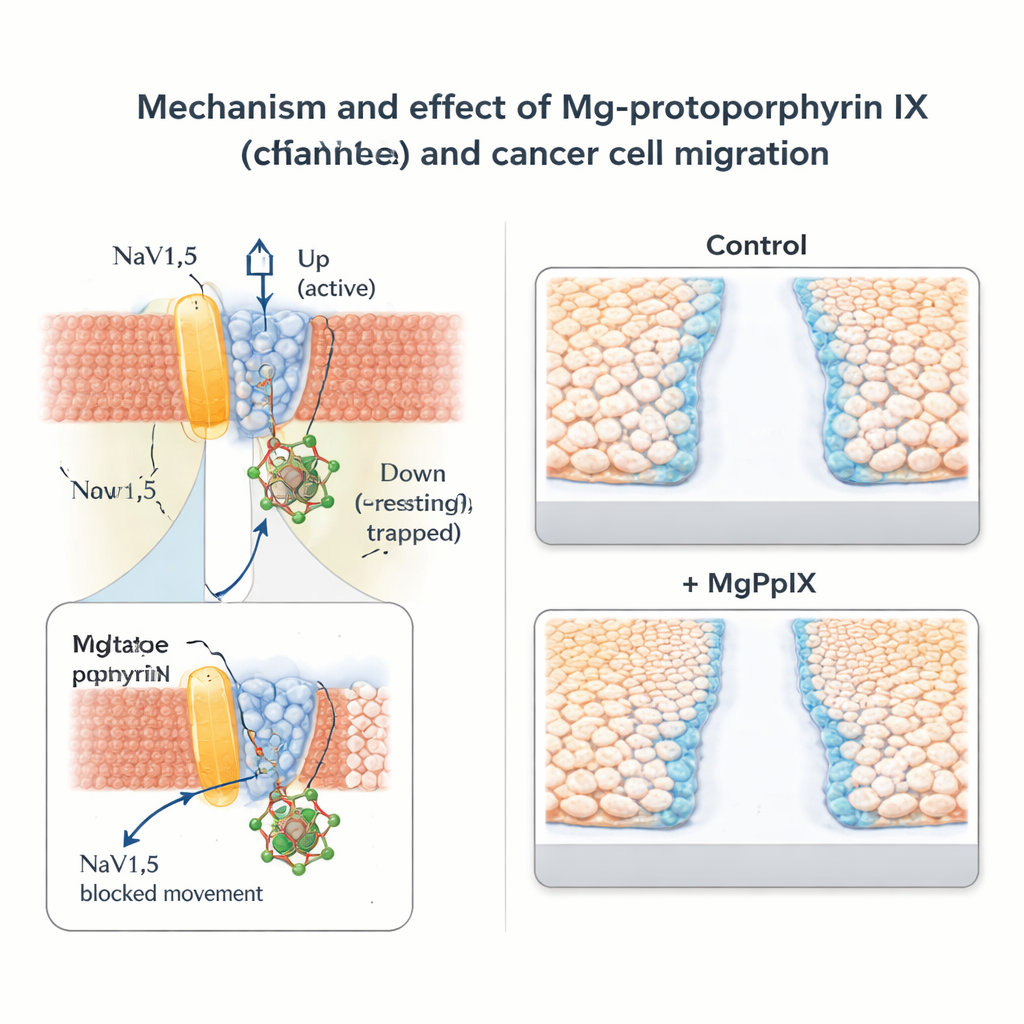
Spowalnianie ruchu komórek nowotworowych bez szerokiego blokowania nerwów
Zespół następnie zbadał, co ta molekularna blokada oznacza dla zachowania nowotworu. W liniach komórkowych raka piersi (MDA-MB-231) i raka jelita grubego (SW-480), które naturalnie ekspresjonują NaV1.5, MgPpIX dramatycznie zmniejszyła prądy sodowe i spowolniła migrację komórek w standardowych testach „zarysowania” i transwell. Im silniej dana protoporfiryna metalu blokowała NaV1.5, tym bardziej hamowała ruch komórek, co wzmacnia związek między aktywnością kanału a motoryką. Dla odmiany linie komórkowe nowotworowe pozbawione NaV1.5 nie reagowały na MgPpIX ani elektrycznie, ani w testach migracji, co wspiera tezę, że efekt jest wysoce specyficzny, a nie ogólnotoksyczny. W porównaniu z klasyczną toksyną na kanały sodowe, tetrodotoksyną, MgPpIX osiągnęła silniejsze zahamowanie migracji przy znacznie niższych stężeniach.
Obietnica i ostrożność wobec przyszłych leków antymetastatycznych
Dla osoby nietechnicznej główne przesłanie jest takie, że badacze znaleźli związek związany z roślinami, który działa jak precyzyjny zacisk na kanał typu sercowego, wykorzystywany przez niektóre nowotwory. Zatrzymując maleńką dźwignię napięciową kanału w pozycji spoczynkowej, MgPpIX może silnie ograniczyć ruchliwość komórek nowotworowych w laboratorium, oszczędzając przy tym inne kanały sodowe kluczowe dla czucia i ruchu. Ponieważ szybka aktywność elektryczna serca może częściowo znosić ten blok, może istnieć okno bezpieczeństwa, w którym komórki nowotworowe są hamowane bardziej niż komórki serca. Chociaż sama MgPpIX może nie być od razu gotowa jako lek, jej unikatowe miejsce wiązania i mechanizm działania dają potężny plan działania do projektowania przyszłych leków mających powstrzymać rozprzestrzenianie się raka przez ukierunkowanie NaV1.5 z bezprecedensową selektywnością.
Cytowanie: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Słowa kluczowe: kanały sodowe, Nav1.5, migracja komórek nowotworowych, cząsteczki pochodne chlorofilu, ukierunkowane leki na kanały jonowe