Clear Sky Science · pl
Efekty terapeutyczne IGF-2 w NMOSD przez hamowanie apoptozy astrocytów poprzez modulację szlaku sygnałowego IGF-1R/PI3K/AKT
Ochrona mózgu w mało znanej chorobie autoimmunologicznej
Spektrum zaburzeń neuromyelitis optica, czyli NMOSD, to rzadka, lecz wyniszczająca choroba autoimmunologiczna atakująca nerwy wzrokowe i rdzeń kręgowy, często pozostawiająca pacjentów z ślepotą, porażeniem lub poważnymi zaburzeniami poznawczymi. Obecne leki głównie tłumią układ odpornościowy, są kosztowne i nie chronią bezpośrednio komórek mózgu przed uszkodzeniem. W badaniu sprawdzono, czy naturalna krążąca w krwi cząsteczka związana ze wzrostem, nazwana IGF‑2, może chronić komórki mózgu przed urazem w NMOSD i stanowić nową opcję terapeutyczną.
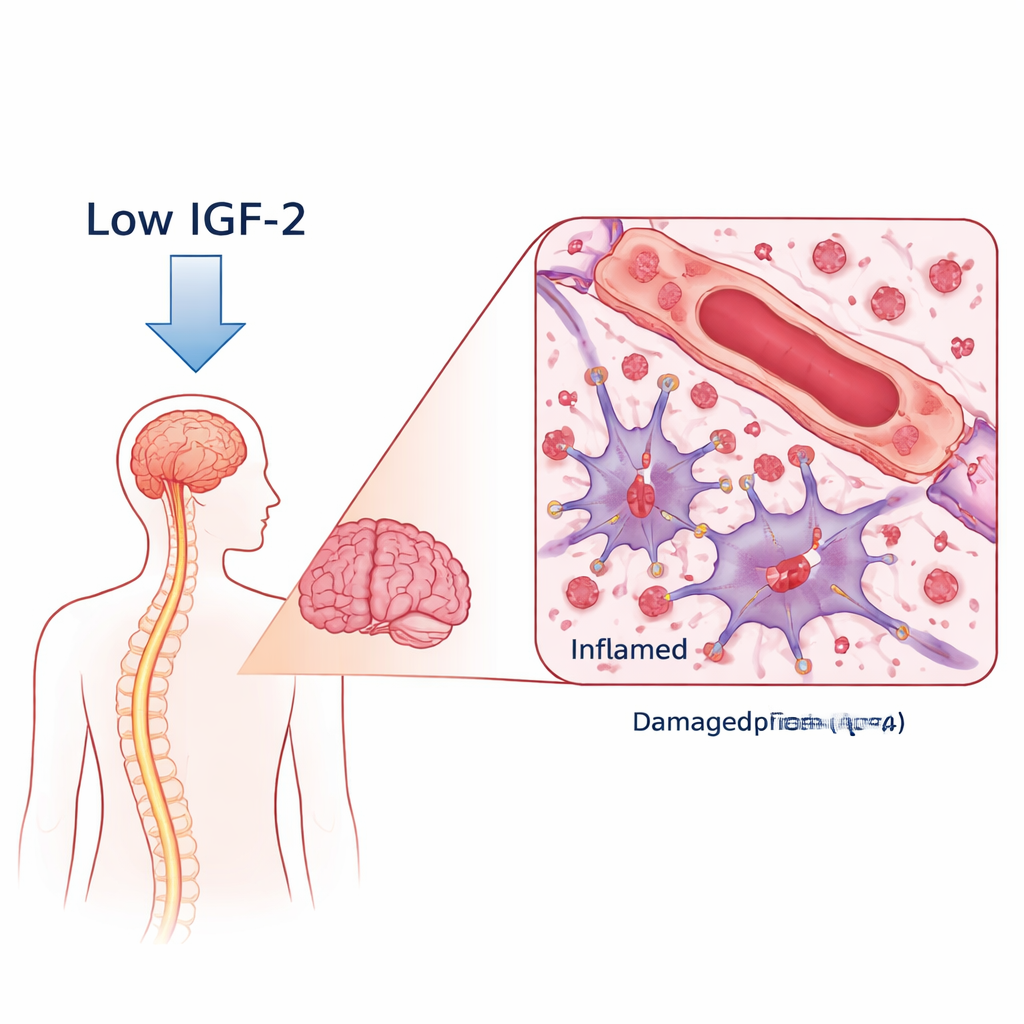
Szkodliwe przeciwciało i brakujący czynnik ochronny
W NMOSD organizm wytwarza przeciwciała przeciwko białku kanału wodnego zwanemu AQP4, znajdującemu się na gwiaździstych komórkach wsparcia mózgu — astrocytach. Gdy te przeciwciała się wiążą, wywołują ataki immunologiczne, które uszkadzają astrocyty, pozbawiają osłonki mielinowej włókna nerwowe i mogą szkodzić neuronom. Naukowcy porównali krew kobiet z NMOSD z obecnością przeciwciał przeciw AQP4 do zdrowych ochotniczek. W szerokim przeglądzie białek stwierdzili, że poziomy IGF‑2 były znacznie obniżone u pacjentek z NMOSD, podczas gdy dwa białka wiążące IGF, które mogą unieruchamiać IGF‑2, były podwyższone. Co istotne, pacjentki z najniższym IGF‑2 miały tendencję do większej niesprawności oraz słabszych wyników w testach myślenia i pamięci, łącząc tę cząsteczkę z ciężkością choroby i funkcjami poznawczymi.
Standardowe leczenie przywraca IGF-2
Wiele pacjentek z NMOSD otrzymuje rituximab — lek usuwający komórki B produkujące przeciwciała. Zespół zmierzył białka we krwi przed i po terapii rituximabem. Po leczeniu poziomy IGF‑2 wzrosły, a białka wiążące spadły, zbliżając się do wzorca obserwowanego u zdrowych osób. Sugeruje to, że uspokojenie układu odpornościowego może pozwolić organizmowi przywrócić niektóre własne czynniki ochronne. Chociaż rituximab nie jest zaprojektowany do działania na IGF‑2, zmiana w tej cząsteczce sugeruje, że może być częścią odpowiedzi naprawczej organizmu, a monitorowanie IGF‑2 mogłoby pomóc śledzić stan pacjentek w czasie.
Testowanie IGF-2 w mysiej wersji choroby
Aby sprawdzić, czy IGF‑2 może robić coś więcej niż wskazywać ciężkość choroby, naukowcy sięgnęli po model myszy. Wstrzyknęli do mózgów myszy ludzkie przeciwciała przeciw AQP4 i ludzki dopełniacz, co odtworzyło kluczowe cechy NMOSD: utratę AQP4 na astrocytach, zapalenie, uszkodzenie mieliny i osłabienie kończyn. Inna grupa myszy otrzymała najpierw niepatogenny wirus powodujący, że komórki mózgu wytwarzały dodatkowe IGF‑2. Myszy z podwyższonym IGF‑2 traciły mniej wagi, miały łagodniejsze zaburzenia ruchowe oraz mniejsze ubytki mieliny i zapalenie w tkance mózgu i rdzenia kręgowego. Standardowe leczenie rituximabem także pomagało, ale nadekspresja IGF‑2 zdawała się chronić tkankę mózgową bardziej bezpośrednio, sugerując rolę neuroprotekcyjną, a nie wyłącznie immunosupresyjną.
Jak IGF-2 łagodzi śmierć komórek i zapalenie
Zespół następnie badał astrocyty w hodowlach narażone na przeciwciała NMOSD. Zazwyczaj te przeciwciała obniżały poziomy kluczowego receptora IGF‑1R i tłumiły podporowy szlak bezpieczeństwa znany jako PI3K/AKT, jednocześnie włączając białka „samozniszczenia” i sygnały zapalne. Kiedy badacze wymusili w astrocytach produkcję większej ilości IGF‑2, ten ochronny szlak znów się aktywował, markery śmierci komórkowej spadły, a komórki uwalniały mniej cząsteczek zapalnych, takich jak IL‑1β, IL‑6 i TNF‑α. Zablokowanie receptora IGF‑1R częściowo cofnęło te korzyści, pokazując, że IGF‑2 działa głównie przez aktywację łańcucha IGF‑1R/PI3K/AKT we wnętrzu astrocytów. U żywych myszy zwiększenie IGF‑2 także zmniejszyło aktywację mikrogleju — strażników immunologicznych mózgu — i obniżyło sygnały zapalne we krwi.
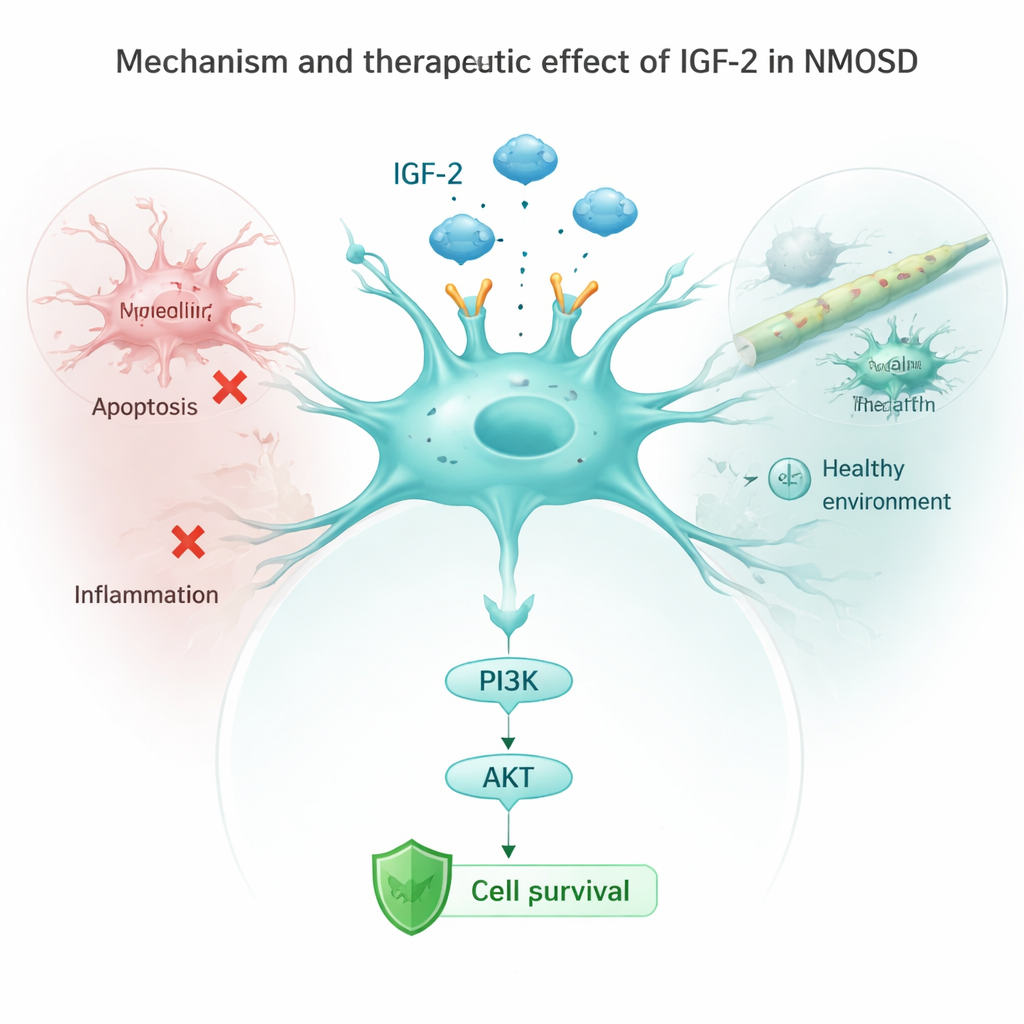
Co to może znaczyć dla pacjentów
Podsumowując, wyniki te sugerują, że niski poziom IGF‑2 jest zarówno sygnałem ostrzegawczym, jak i utraconą szansą w NMOSD. Pacjenci z mniejszą ilością IGF‑2 mają zwykle większą niepełnosprawność i gorsze funkcje poznawcze, podczas gdy przywrócenie lub zwiększenie IGF‑2 w modelach eksperymentalnych pomaga przetrwać astrocytom, zmniejsza zapalenie mózgu i ogranicza uszkodzenie nerwów. Choć praca jest wstępna i oparta na niewielkiej liczbie pacjentów oraz badaniach na zwierzętach, wskazuje na IGF‑2 jako obiecujący cel przyszłych terapii, które mogłyby nie tylko osłabić atak immunologiczny, lecz również bezpośrednio chronić wrażliwe komórki mózgu.
Cytowanie: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Słowa kluczowe: neuromyelitis optica, astrocyty, IGF-2, neurozapalenie, neuroprotekcja