Clear Sky Science · pl
Integracja toksykologii sieciowej, uczenia maszynowego i symulacji dynamiki molekularnej w celu ujawnienia podwójnych mechanizmów działania tanshinonu IIA w TNBC i kardiotoksyczności wywołanej doksorubicyną
Dlaczego te badania są ważne dla pacjentów
Doksorubicyna jest podstawowym lekiem w leczeniu raka piersi, ale ma poważny minus: może uszkadzać serce, czasem lata po zakończeniu terapii. Równocześnie potrójnie ujemny rak piersi — trudna do leczenia postać pozbawiona typowych celów hormonalnych i czynników wzrostu — nadal wymaga lepszych terapii. Badanie to bada, czy tanshinon IIA, związek wyizolowany z tradycyjnego chińskiego zioła Salvia miltiorrhiza, mógłby zarówno chronić serce przed toksycznością doksorubicyny, jak i pomagać w zwalczaniu agresywnych nowotworów piersi, potencjalnie czyniąc chemioterapię bezpieczniejszą i skuteczniejszą.
Jeden związek, dwa duże problemy
Doksorubicyna uratowała niezliczone życia, ale jej korzyści ogranicza kardiotoksyczność zależna od dawki: powyżej określonej dawki całkowitej ryzyko niewydolności serca gwałtownie rośnie. Klinicyści często muszą dokonywać trudnego wyboru między kontrolą nowotworu a ochroną serca. Wcześniejsze badania laboratoryjne sugerowały, że tanshinon IIA może wzmacniać antyoksydacyjne mechanizmy obronne w komórkach serca i bezpośrednio zabijać komórki nowotworowe, lecz molekularne podstawy tych efektów nie były jasne. Autorzy postanowili systematycznie odwzorować, w jaki sposób jeden związek mógłby zmniejszać uszkodzenia serca, a jednocześnie atakować potrójnie ujemny rak piersi, budując pomost między medycyną tradycyjną a nowoczesną onkologią precyzyjną. 
Kopanie w dużych zbiorach danych biologicznych w poszukiwaniu ochrony serca
Aby zrozumieć ochronę serca, zespół najpierw zgromadził tysiące genów powiązanych z kardiotoksycznością z kilku dużych baz danych i połączył je z poznanymi białkowymi celami doksorubicyny i tanshinonu IIA. Wyłoniło się trzynaście celów „nakładających się” — białek powiązanych z uszkodzeniem serca, oddziałujących z doksorubicyną i potencjalnie modulowanych przez tanshinon IIA. Na podstawie map interakcji białko–białko badacze zawęzili listę do sześciu kluczowych uczestników, w tym CCND1 (regulator cyklu komórkowego), APAF1 (inicjator zaprogramowanej śmierci komórkowej), AR (receptor androgenowy), TERT (istotny dla utrzymania telomerów), MMP2 (enzym przebudowy tkanki) i NQO1 (enzym antyoksydacyjny). Dokowanie komputerowe i symulacje dynamiki molekularnej sugerowały, że zarówno doksorubicyna, jak i tanshinon IIA mogą silnie wiązać się z tymi białkami, lecz kompleksy z tanshinonem IIA bywają częściej bardziej stabilne i termodynamicznie korzystne, co sugeruje, że związek ziołowy może przekierowywać lub łagodzić szkodliwe sygnały doksorubicyny w sercu.
Odkrywanie, jak celuje w agresywne guzy piersi
Po stronie nowotworowej badacze skupili się na zestawach danych ekspresji genów potrójnie ujemnego raka piersi. Porównali próbki guza z normalną tkanką piersi, aby znaleźć setki genów nieprawidłowo włączonych lub wyłączonych. Następnie użyli techniki zwanej ważoną analizą sieci współekspresji genów, aby zidentyfikować grupy genów najsilniej powiązane z fenotypem potrójnie ujemnym. Przecinając te geny z przewidywanymi celami tanshinonu IIA, wyekstrahowali krótką listę kandydatów i zastosowali trzy niezależne metody uczenia maszynowego, aby sprawdzić, które geny najlepiej odróżniają tkankę guza od normalnej i mają największe znaczenie kliniczne. Zbieżne dowody wskazały jeden wyróżniający się cel: EZH2, gen uczestniczący w pakowaniu DNA i często nadaktywowany w agresywnych nowotworach.
Łączenie biologii guza i układu odpornościowego
Aby zrozumieć, dlaczego EZH2 ma znaczenie u pacjentów, zespół przeanalizował duże bazy danych nowotworowych. Stwierdzili, że EZH2 jest wyraźnie bardziej aktywny w inwazyjnych guzach piersi niż w normalnej tkance piersi. Chociaż jego ekspresja nie korelowała jednoznacznie z całkowitym przeżyciem we wszystkich przypadkach raka piersi, była silnie związana z cechami mikrośrodowiska immunologicznego guza. Wyższy poziom EZH2 korelował z większą infiltracją kilku typów komórek odpornościowych — takich jak komórki B i T — oraz ze zwiększoną ekspresją cząsteczek zarówno pobudzających, jak i hamujących odpowiedź immunologiczną, w tym dobrze znanych białek punktów kontrolnych, takich jak CTLA‑4 i LAG‑3. Te wzorce sugerują, że EZH2 znajduje się na skrzyżowaniu między wzrostem guza a kontrolą immunologiczną, i że lek taki jak tanshinon IIA, wpływając na EZH2, mógłby pomóc przekształcić sposób, w jaki układ odpornościowy rozpoznaje i atakuje potrójnie ujemny rak piersi. 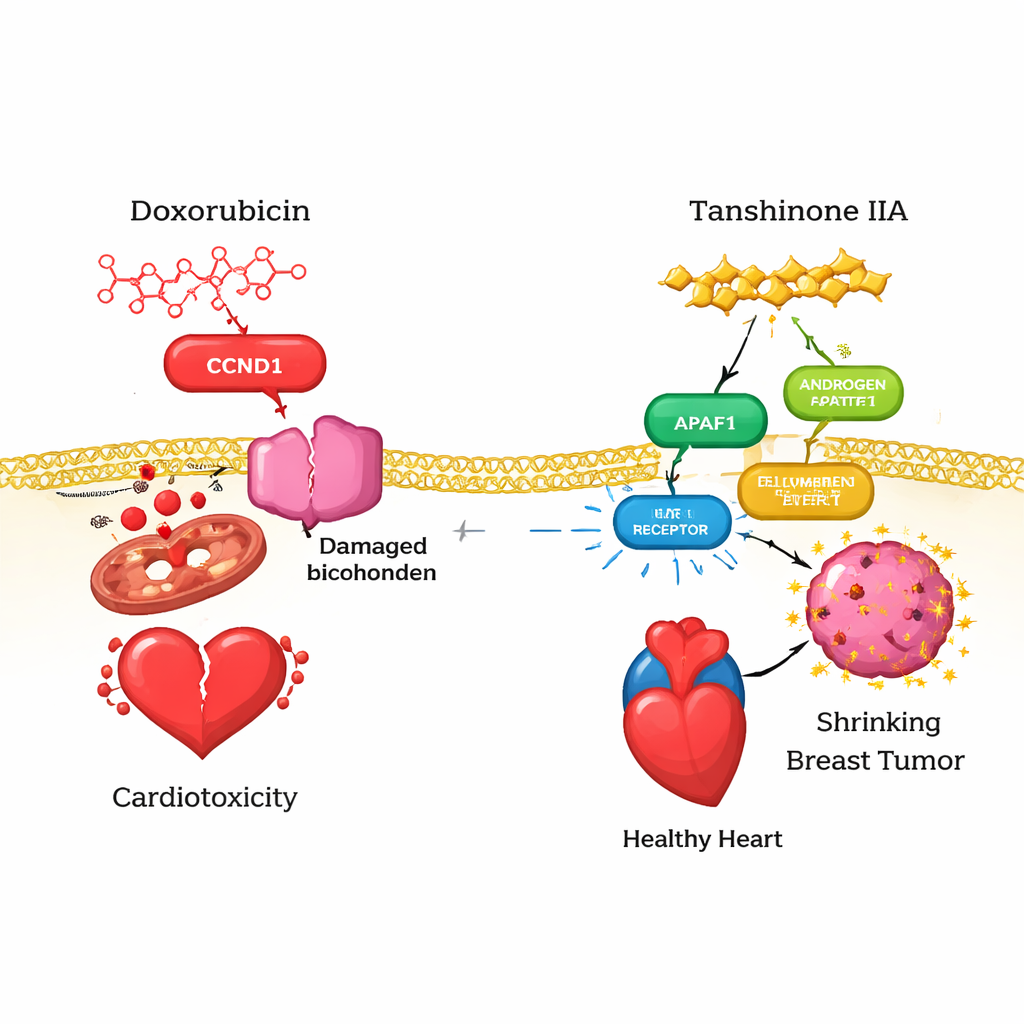
Co to może znaczyć dla przyszłego leczenia
Mówiąc wprost, praca ta proponuje, że tanshinon IIA mógłby pełnić podwójną rolę w opiece nad rakiem piersi: działać jak „chemiczna tarcza”, która zmniejsza uszkodzenia serca związane z doksorubicyną poprzez stabilizację kluczowych białek chroniących serce, oraz jednocześnie jako celowany środek przeciw potrójnie ujemnemu rakowi piersi poprzez wpływ na EZH2 i powiązane ścieżki immunologiczne. Wyniki opierają się na analizach komputerowych i statystycznych, a nie na badaniach na zwierzętach czy ludziach, więc stanowią wczesny plan działania, a nie gotową terapię. Mimo to dostarczają szczegółowej mapy molekularnej do projektowania terapii skojarzonych, które zachowują ratującą życie skuteczność doksorubicyny przy jednoczesnym ograniczeniu jej długoterminowego ryzyka — oraz do przetłumaczenia tradycyjnego składnika ziołowego na nowoczesny, oparty na mechanizmach dodatek do leczenia raka.
Cytowanie: Wu, B., Lan, Xh., Chen, Xq. et al. Integrating network toxicology, machine learning, and molecular dynamics simulations to reveal tanshinone iia’s dual mechanisms in TNBC and doxorubicin-induced cardiotoxicity. Sci Rep 16, 6861 (2026). https://doi.org/10.1038/s41598-026-37428-8
Słowa kluczowe: tanshinon IIA, kardiotoksyczność doksorubicyny, potrójnie ujemny rak piersi, EZH2, farmakologia sieciowa