Clear Sky Science · pl
Ocena metabolomiczna ujawnia wyczerpanie aminokwasów i metabolitów energetycznych w mięśniach szkieletowych po niedokrwiennym ostrym uszkodzeniu nerek u myszy
Dlaczego uszkodzone nerki mogą osłabiać mięśnie
Osoby z nagłą niewydolnością nerek często zauważają objaw, który wydaje się niezwiązany z badaniami moczu czy krwi: mięśnie stają się słabe, a regeneracja przebiega powoli. To badanie stawia proste, ale istotne pytanie — co rzeczywiście dzieje się w zapasach paliwa i budulca mięśni, gdy nerki zostaną nagle uszkodzone? Na podstawie szczegółowego chemicznego przeglądu mięśni myszy autorzy pokazują, że ostre uszkodzenie nerek wywołuje ogólnoustrojowy odpływ kluczowych substancji odżywczych i cząsteczek energetycznych, pozostawiając mięśnie szkieletowe w stanie wyczerpania i deficytu energetycznego.
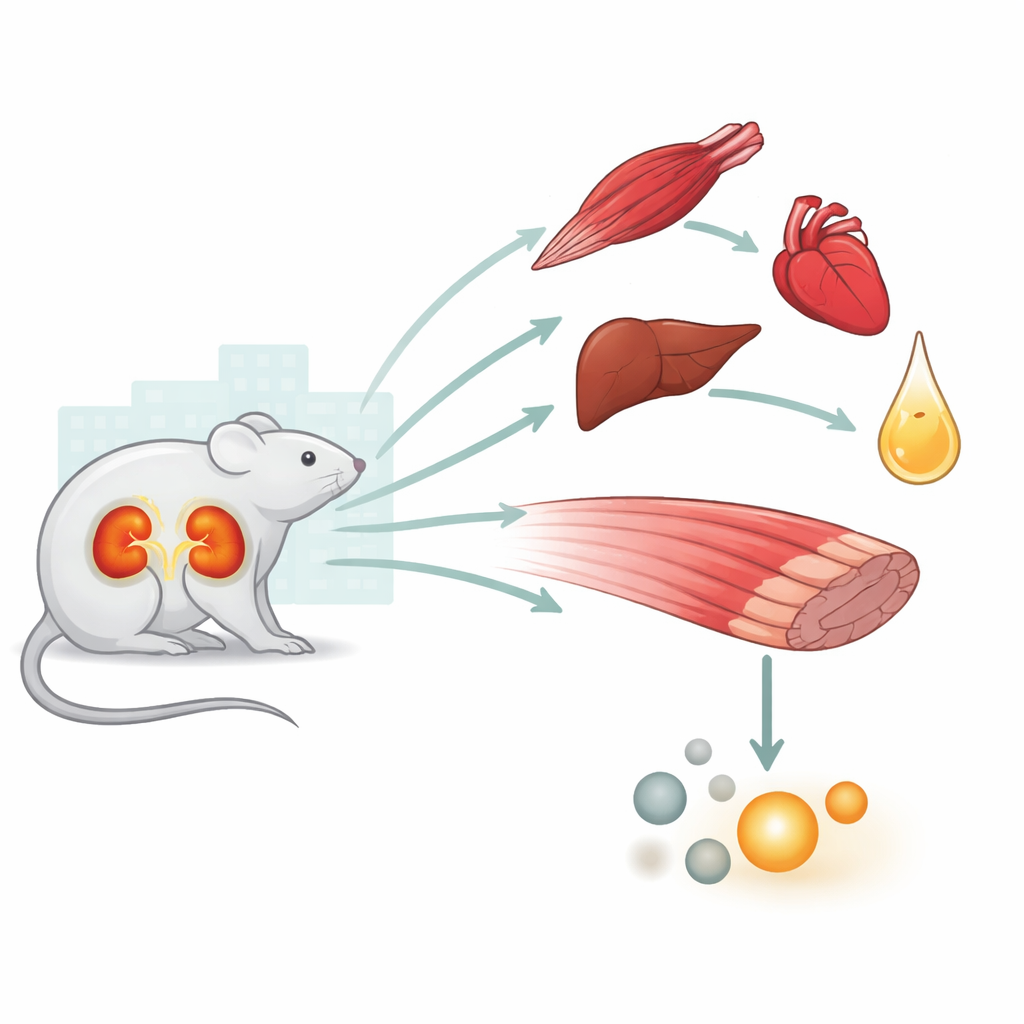
Kryzys całego organizmu, nie tylko problem nerek
Ostre uszkodzenie nerek (AKI) jest powszechne u hospitalizowanych i krytycznie chorych pacjentów i wiąże się ze zwiększonym ryzykiem śmierci. Lekarze od dawna obserwują, że AKI zachowuje się jak stan ogólnoustrojowego stresu, wpływając na serce, płuca, wątrobę, mózg i mięśnie. Wcześniejsze prace tej grupy wykazały, że po przejściowym zahamowaniu przepływu krwi do nerek u myszy serce, wątroba, płuca i same nerki wykazywały chemiczne oznaki deficytu energetycznego i stresu oksydacyjnego. Na tej podstawie obecne badanie koncentruje się na mięśniach szkieletowych, będących ważnym rezerwuarem węglowodanów i aminokwasów, z którego organizm korzysta w stanie ciężkiego stresu.
Jak przeprowadzono badanie u myszy
Naukowcy wywołali niedokrwienne AKI u młodych dorosłych samców myszy przez krótkie zaciskanie obu dopływów krwi do nerek, a następnie przywrócenie przepływu. Porównywano te zwierzęta z grupą operowaną pozorowanie (sham) oraz z całkowicie nieoperowanymi kontrolami. Po 24 i 72 godzinach pobrano kluczowy mięsień nogi (gastrocnemius) i zastosowano nieukierunkowane podejście metabolomiczne — ultrasensytywne skanowanie chemiczne — aby zmierzyć 175 małych cząsteczek, w tym aminokwasy, przeciwutleniacze i związki związane z energią. Zastosowano metody statystyczne i rozpoznawania wzorców, by ustalić, które molekuły zmieniły się najbardziej i jak różniła się chemia mięśni między grupami.
Zapas paliwa mięśni i przeciwutleniacze maleją
Najbardziej uderzające zmiany pojawiły się 24 godziny po uszkodzeniu nerek. Około dwóch piątych wszystkich wykrytych metabolitów uległo zmianie, a ogólny wzorzec był czytelny: wiele kluczowych związków w mięśniach było zredukowanych w porównaniu z zabiegiem pozorowanym. Zarówno egzogenne, jak i endogenne aminokwasy, takie jak alanina, walina, lizyna, metionina i tyrozyna, spadły, podobnie jak kilka związków cyklu mocznikowego (arginina, cytrulina, ornityna, argininosuccynian), które pomagają w gospodarowaniu azotem i wspierają produkcję kreatyny. Główny wewnątrzkomórkowy przeciwutleniacz, glutation, oraz jego składniki budulcowe (w tym metionina i dipeptyd cysteina‑glicyna) również były zmniejszone, co wskazuje na nasilony stres oksydacyjny. Związki związane z energią, w tym kreatyna i pośrednie produkty centralnych szlaków energetycznych, miały tendencję spadkową, sugerując, że mięsień poświęca własne rezerwy, aby wspierać resztę organizmu.
Łączenie mięśni z innymi narządami
Aby zobaczyć szerszy obraz, zespół porównał dane z mięśni z wcześniej zebranymi profilami metabolomicznymi z nerek, wątroby, serca i osocza krwi w tym samym punkcie czasowym 24 godzin. We wszystkich tych miejscach powtarzały się pewne motywy: szerokie wyczerpanie glutationu i jego prekursorów, niższy poziom alaniny oraz konsekwentne zaburzenia chemii związanej z argininą i cyklem mocznikowym. Równocześnie niektóre produkty rozpadu, takie jak allantoin (marker stresu oksydacyjnego), wzrosły w wielu narządach i we krwi. Kreatyna i jej wysokomolekularna forma energii, fosfokreatyna, były względnie podwyższone w wątrobie, nerkach i krwi, nawet gdy arginina i aminokwasy malały w mięśniach i osoczu, co sugeruje, że mięśnie szkieletowe mogą eksportować substraty, by inne organy — a szczególnie uszkodzone nerki — mogły utrzymać produkcję energii w warunkach stresu.
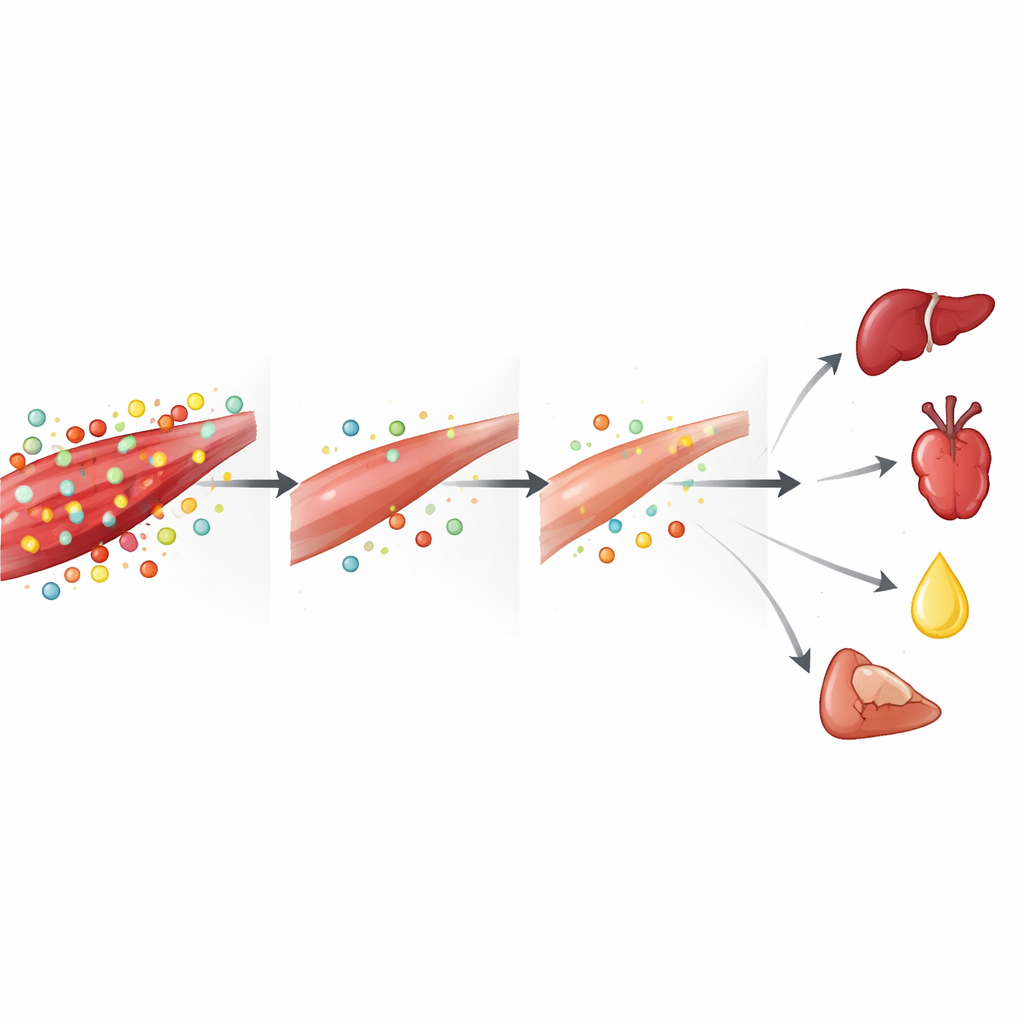
Co to oznacza dla pacjentów i przyszłych terapii
Mówiąc prostymi słowami, badanie opisuje AKI jako metaboliczne „wypłacenie” środków przez organizm: mięśnie szkieletowe rozkładają swoje zapasy białka i przeciwutleniaczy, by pomóc zasilać i chronić narządy życiowe, pozostawiając same mięśnie pozbawione paliwa i obrony. To pomaga wyjaśnić, dlaczego osoby z ciężkim uszkodzeniem nerek są podatne na zanik mięśni, osłabienie i słabą regenerację funkcjonalną. Wskazuje też na możliwość, że celowane wsparcie żywieniowe — w szczególności aminokwasy i związki wzmacniające systemy glutationu oraz kreatyna‑fosfokreatyna — mogłoby kiedyś pomóc chronić zarówno nerki, jak i mięśnie podczas ostrej choroby. Choć te ustalenia pochodzą od myszy i opierają się na chemicznych migawkach zamiast bezpośredniego śledzenia przepływów, dostarczają szczegółowej mapy tego, jak chemia mięśni jest zaburzona przez uszkodzenie nerek i wskazują nowe strategie zachowania siły i poprawy wyników, gdy nerki zawodzą nagle.
Cytowanie: Li, A.S., Baker, P.R., Park, S. et al. Metabolomic assessment reveals depletion of amino acids and energy metabolites in skeletal muscle after ischemic acute kidney injury in mice. Sci Rep 16, 8823 (2026). https://doi.org/10.1038/s41598-026-37424-y
Słowa kluczowe: ostre uszkodzenie nerek, metabolizm mięśni szkieletowych, wyczerpanie aminokwasów, stres oksydacyjny, metabolomika