Clear Sky Science · pl
Analiza skurczowej czynności serca u myszy z wyłączonym genem PERM1 przy użyciu dużych kohort zwierząt
Dlaczego małe mysie serca mają znaczenie dla zdrowia ludzi
Niewydolność serca często opisuje się jako zmęczoną pompę, jednak to, co sprawia, że serce jest słabe, jest zaskakująco złożone. W tym badaniu naukowcy wykorzystali wyjątkowo dużą grupę myszy, aby zadać konkretne pytanie: czy wyłączenie pojedynczego genu o nazwie PERM1, znanego z roli w produkcji energii w komórkach serca, zmienia także siłę skurczu serca? Poprzez staranne badanie serc ponad 170 myszy wykazali, że ten gen subtelnie przekształca serce i obniża jego siłę pompowania, podczas gdy zwierzęta z zewnątrz pozostają w dużej mierze zdrowe. Ich odkrycia pomagają rozstrzygnąć debatę w tej dziedzinie i proponują wskazówki do projektowania lepszych eksperymentów kardiologicznych w przyszłości.
Gen łączący wykorzystanie paliwa ze skurczem serca
PERM1 został po raz pierwszy zidentyfikowany jako przełącznik zwiększający produkcję energii w komórkach mięśniowych, w tym w sercu. Wcześniejsze badania wykazały, że poziomy PERM1 spadają w niewydolnych sercach u myszy i u ludzi, co sugerowało, że niski poziom PERM1 może przyczyniać się do osłabionych skurczów. Jednak prace na myszach pozbawionych PERM1 — zmodyfikowanych tak, by brakowało im tego genu — dały sprzeczne odpowiedzi, czy ich serca rzeczywiście pompują słabiej. Ponieważ PERM1 jest rozważany jako potencjalny cel terapii niewydolności serca, autorzy postanowili przetestować jego wpływ na funkcję serca przy użyciu wystarczającej liczby zwierząt i rygorystycznej analizy statystycznej, by uzyskać jednoznaczną odpowiedź tak/nie.
Przegląd małych serc przy dużej liczbie zwierząt
Zespół zebrał dane z echokardiogramów — tej samej techniki ultrasonograficznej stosowanej w klinikach kardiologicznych — ze wszystkich myszy z wyłączonym genem PERM1 oraz od zdrowych rodzeństw używanych w ich laboratorium w ciągu 18 miesięcy. To retrospektywne zbieranie danych zaowocowało 84 myszami normalnymi (dzikiego typu) i 88 myszami z wyłączeniem genu, co daje próbę znacznie większą niż zwykle w badaniach serca u myszy. Z obrazów ultradźwiękowych zmierzono standardowe wskaźniki funkcji lewej komory, głównej jamy pompującej. Kluczowym parametrem była frakcja wyrzutu, czyli procent krwi wyrzucanej przy każdym skurczu, wraz z powiązanymi miarami, takimi jak zmniejszenie średnicy komory przy skurczu, grubość ścian oraz całkowita objętość krwi pompowana na minutę.
Słabszy skurcz, większa jama, podobny wyrzut
Wyniki pokazują spójny wzorzec. Średnio frakcja wyrzutu spadła z około 65% u myszy normalnych do 54% u myszy z brakiem PERM1, różnica wystarczająco duża, by miała znaczenie kliniczne u ludzi i poparta bardzo mocnymi danymi statystycznymi. Inne miary skurczu, takie jak skrócenie frakcyjne i pogrubienie ściany, również się obniżyły. Jednocześnie lewe komory myszy bez PERM1 były wyraźnie większe, szczególnie pod koniec skurczu, co wskazuje, że w komorze pozostawało więcej krwi. Pomimo słabszego skurczu, całkowita objętość krwi pompowana na minutę spadła tylko nieznacznie — o około 6% — ponieważ powiększone jamy mogły pomieścić więcej krwi na początku. Innymi słowy, serce częściowo kompensowało słabszy skurcz przez rozciągnięcie głównej komory.
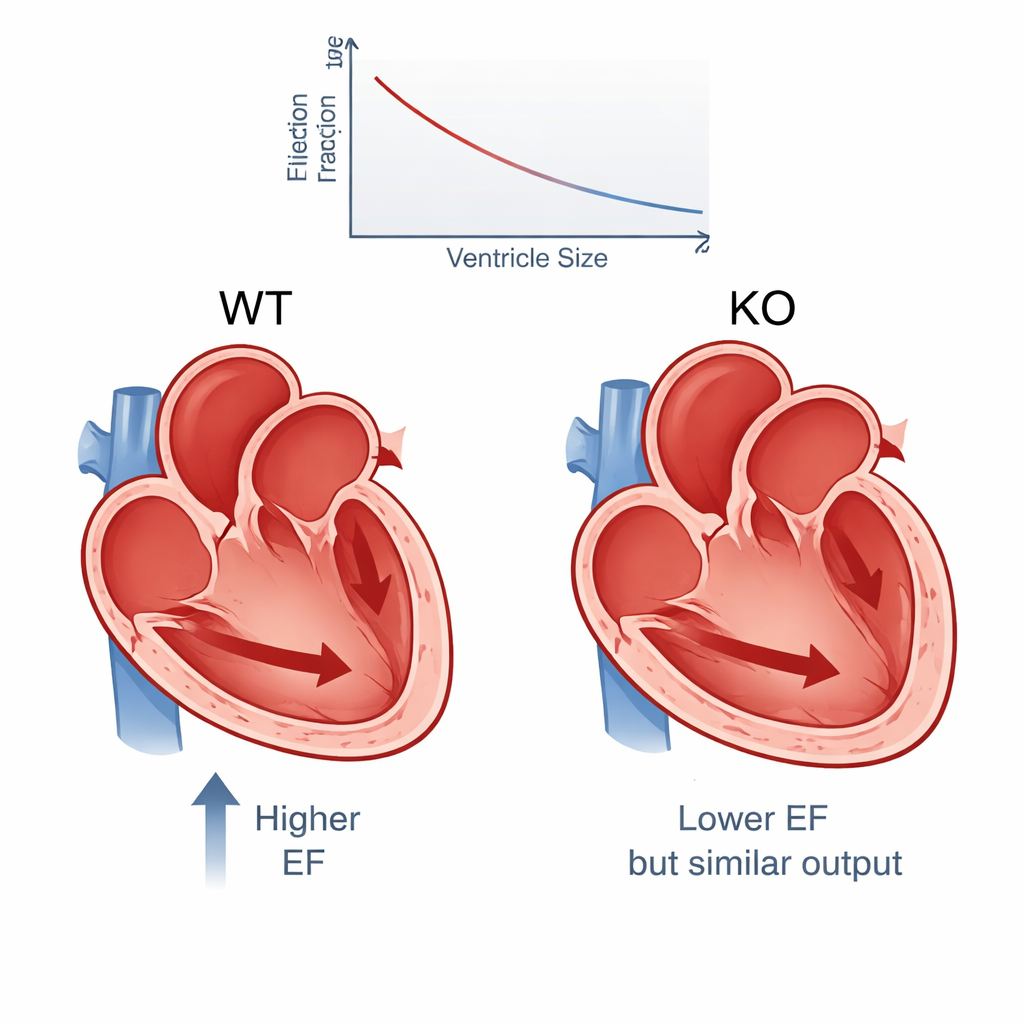
Ukryta różnorodność w „identycznych” sercach
Dzięki tak dużej liczbie zwierząt badacze mogli spojrzeć poza średnie i zbadać, jak poszczególne serca się różnią. Nawet wśród genetycznie identycznych, zdrowych myszy zaobserwowali zaskakująco szerokie rozrzuty wartości frakcji wyrzutu. Wyłączenie PERM1 przesunęło całą dystrybucję w dół — więcej serc o niższej sile pompowania — ale nie poszerzyło samego rozrzutu. Około 7% myszy z wyłączonym genem miało frakcję wyrzutu poniżej 40%, poziom uznawany u ludzi za niewydolność serca z obniżoną frakcją wyrzutu, a mimo to te myszy nadal utrzymywały niemal normalny wyrzut krwi. Analizy statystyczne wykazały, że płeć, wiek i masa ciała wyjaśniały tylko małą część zmienności; większość różnic prawdopodobnie wynika z trudniejszych do zmierzenia czynników biologicznych, takich jak subtelne wpływy środowiskowe lub zmiany epigenetyczne.
Co to oznacza dla przyszłych badań nad sercem
Aby pomóc innym naukowcom w projektowaniu lepszych eksperymentów, autorzy wykorzystali swoje duże dane do obliczenia, ile zwierząt zwykle potrzeba, by wykryć istotne zmiany w poszczególnych parametrach serca. Stwierdzili, że skromne rozmiary grup, często stosowane w tej dziedzinie, łatwo mogą przeoczyć rzeczywiste, choć umiarkowane efekty, zwłaszcza dla subtelnych miar, takich jak objętość wyrzutowa czy rzut serca. Ogólnie badanie silnie wskazuje, że utrata PERM1 powoduje specyficzne przebudowanie serca — większe jamy, słabsze skurcze — zamiast całkowitej niewydolności, a to przebudowanie jest częściowo zrównoważone zmianami strukturalnymi, które pomagają zachować przepływ krwi. Dla laików wniosek jest taki, że pojedynczy gen regulujący energię może przesunąć serce do nowego trybu pracy — takiego, który z zewnątrz wygląda zdrowo, ale kryje subtelne zmiany w budowie pompy i w tym, jak ciężko ona pracuje.
Cytowanie: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Słowa kluczowe: niewydolność serca, kurczliwość serca, energetyka mitochondriów, modele mysie, echokardiografia