Clear Sky Science · pl
Mutacja GJB2 c.109G > A aktywująca szlak mitochondrialnej apoptozy za pośrednictwem IFI27 prowadzący do dziedzicznej niesyndromowej głuchoty
Dlaczego maleńkie komórki ucha mają znaczenie dla przyszłości dzieci
Utrata słuchu obecna od urodzenia dotyka miliony dzieci na całym świecie, często kształtując sposób, w jaki uczą się mówić, radzą sobie w szkole i nawiązują relacje z innymi. Jednym z najczęstszych genetycznych czynników jest gen GJB2, ale lekarze nie w pełni rozumieli, w jaki sposób zmiany w tym genie uszkadzają ucho wewnętrzne. W tym badaniu wykorzystano danio pręgowane oraz komórki ludzkie, aby prześledzić łańcuch zdarzeń od pojedynczej zmiany DNA w GJB2 do śmierci delikatnych komórek odbierających dźwięk, i wskazać nową cząsteczkę, IFI27, jako potencjalny cel przyszłych terapii.
Częsta zmiana genu stojąca za cichą dziecięcą głuchotą
Badacze zaczęli od przesiewu próbek krwi od 1 199 dzieci z podejrzeniem dziedzicznej utraty słuchu w prowincji Fujian w Chinach. Skoncentrowali się na kilku dobrze znanych genach związanych z głuchotą i stwierdzili, że zmiany w GJB2 dominowały — stanowiły 85% wszystkich wykrytych mutacji. Wśród nich najczęstsza była konkretna zmiana nazywana c.109G>A (znana też jako p.Val37Ile). Ten wariant jest stosunkowo często spotykany w populacji ogólnej, a jednocześnie znacznie wzbogacony wśród osób z ubytkiem słuchu, co sugeruje, że odgrywa istotną rolę w niesyndromowej utracie słuchu — problemie słuchowym występującym bez innych dolegliwości.
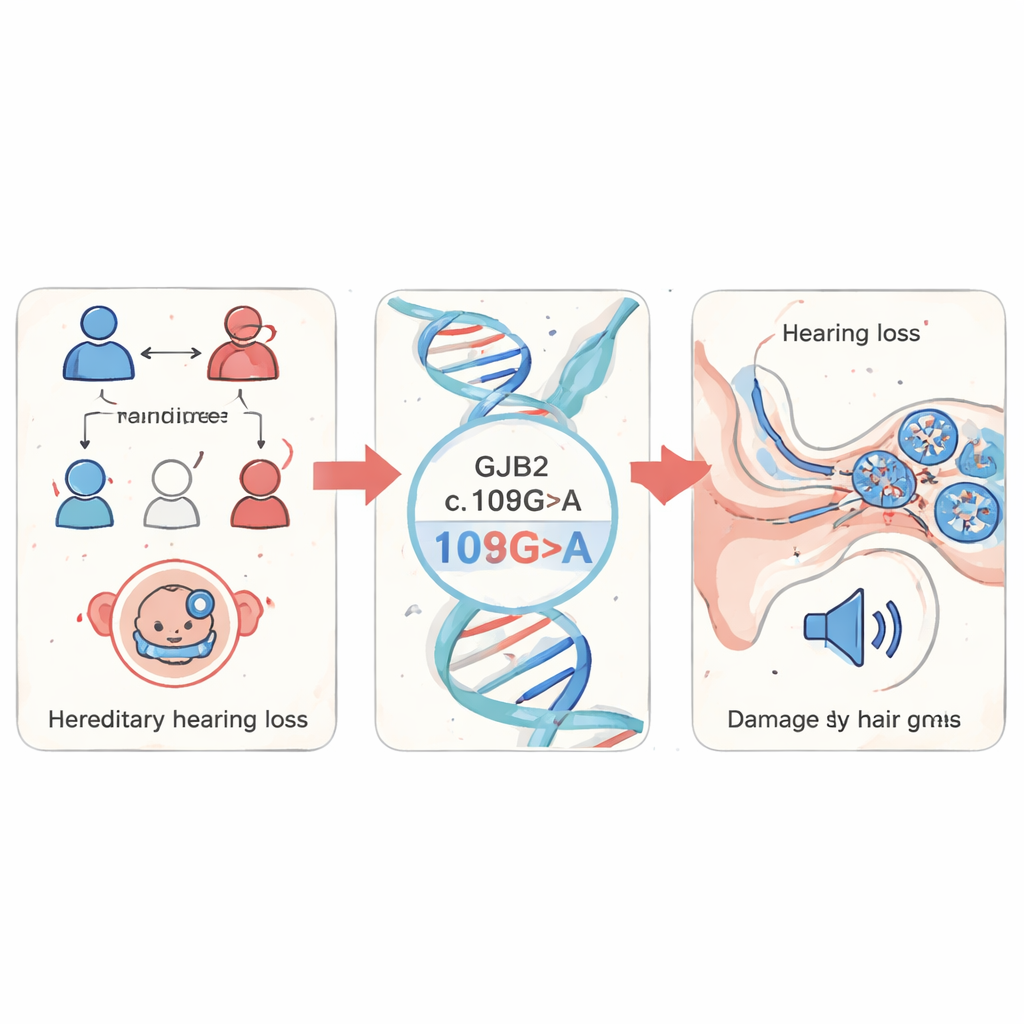
Śledząc uszkodzenia w przezroczystej rybie
Aby zobaczyć, co robi ta mutacja w żywym organizmie, zespół zwrócił się ku danio pręgowanemu, małej rybce słodkowodnej, której zarodki są przezroczyste i która dzieli wiele genów oraz struktur ucha z ludźmi. Zamodelowali zarodki tak, aby produkowały albo normalne ludzkie GJB2, albo mutant c.109G>A, a także zastosowali podejście „knockdown”, by zmniejszyć ekspresję własnego genu gjb2 ryby. Zarodki z wariantem lub z obniżonym poziomem genu wykazywały opóźniony wzrost, zakrzywione ogony i obrzęki wokół serca — objawy zaburzonego rozwoju. Co najistotniejsze, ich ucho wewnętrzne było wyraźnie nieprawidłowe: kluczowe struktury zwane otolitami były mniejsze i bardziej rozstawione, a wypełniony płynem obszar przypominający ślimak był zmniejszony. Gdy naukowcy dodali z powrotem normalne GJB2 obok mutanta, wiele z tych zmian strukturalnych uległo poprawie, co wskazuje, że sama mutacja powodowała defekty.
Od uszkodzonych uszu do gorszego zachowania słuchowego
Ponieważ słuch zależy od maleńkich „komórek włosowych”, które przekształcają drgania dźwięku w sygnały nerwowe, zespół wybarwił te komórki w danio. Ryby z mutacją GJB2 lub po knockdownie miały znacznie mniej komórek włosowych zarówno w uchu wewnętrznym, jak i na powierzchni ciała, gdzie danio też wyczuwają ruch wody. Następnie badacze przetestowali reakcje ryb na dźwięk. Używając zautomatyzowanego systemu śledzenia, mierzyli, jak daleko i jak szybko pięciodniowe larwy pływały po krótkich impulsach dźwiękowych. Ryby normalne i z dziką (wild-type) wersją GJB2 reagowały, pływając dalej i szybciej, natomiast ryby z mutacją i po knockdownie niewiele zmieniały zachowanie, co wskazywało na upośledzenie słuchu. Ponownie — dodanie normalnego GJB2 częściowo przywracało zarówno liczbę komórek włosowych, jak i ruch zależny od dźwięku.
Ścieżka zabijająca wewnątrz „elektrowni” komórki
Aby zrozumieć, co działo się wewnątrz komórek, naukowcy użyli sekwencjonowania RNA, porównując aktywność genów pomiędzy normalnymi danio a tymi z obniżonym poziomem gjb2. Zestaw genów powiązanych z „mitochondrialną ścieżką apoptozy” — drogą samozniszczenia skoncentrowaną w elektrowniach komórkowych — był mocno aktywowany. W szczególności wyróżniały się liczne członkinie rodziny IFI27, obok dobrze znanych uczestników śmierci komórkowej, takich jak Bax, cytochrom c, Apaf1 i kaspazy. Dalsze eksperymenty w ludzkich komórkach HEK293 potwierdziły wzorzec: komórki z mutantem GJB2 wytwarzały więcej reaktywnych form tlenu (ROS, forma stresu oksydacyjnego), uwalniały więcej cytochromu c z mitochondriów i uruchamiały białka apoptozy, co skutkowało zwiększoną śmiercią komórek. Gdy badacze wyciszyli IFI27 w komórkach niosących mutant, poziomy ROS spadły, sygnały śmierci osłabły, a mniej komórek przeszło apoptozę.
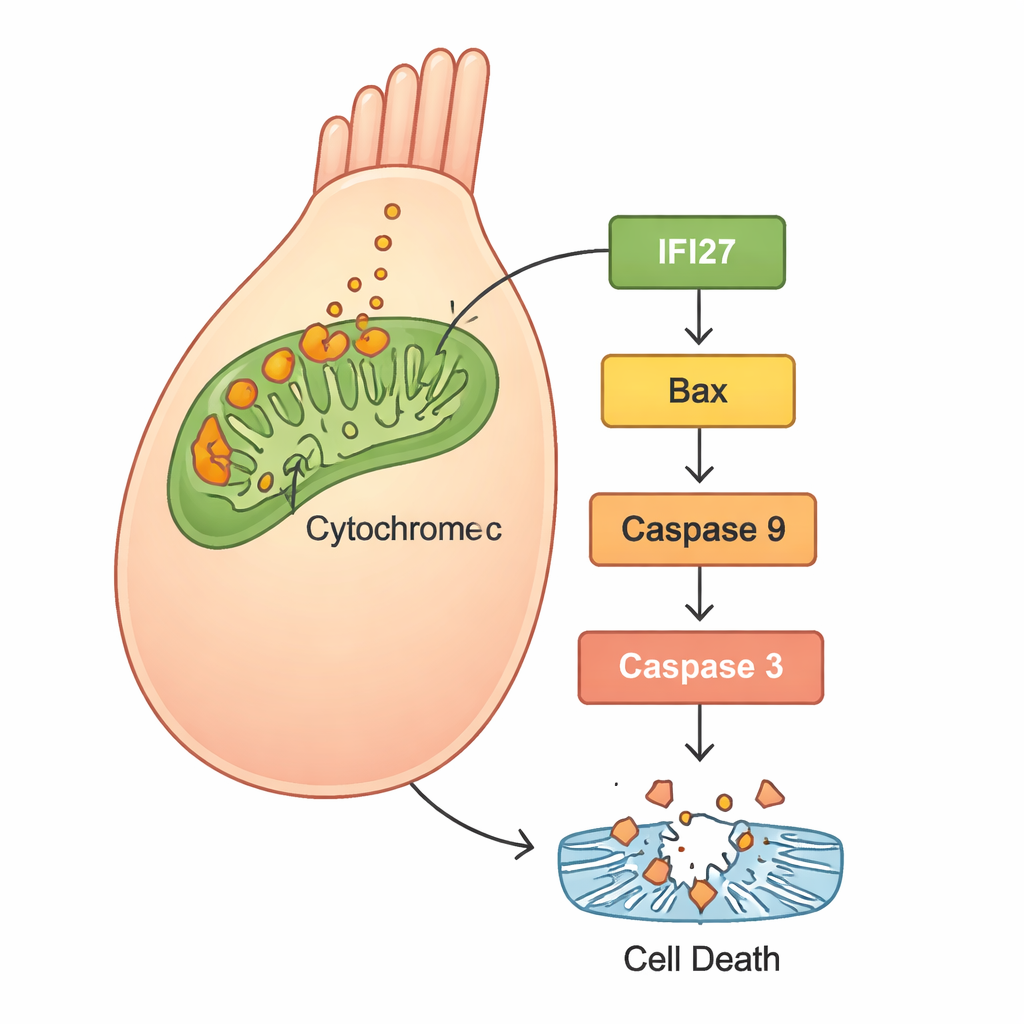
Co to oznacza dla przyszłych terapii
Podsumowując, wyniki sugerują klarowną sekwencję zdarzeń: mutacja GJB2 c.109G>A zaburza prawidłowy rozwój i funkcję ucha wewnętrznego, nie tylko przez zmianę komunikacji międzykomórkowej, lecz także przez wywołanie stresu w mitochondriach. Ten stres zwiększa ekspresję IFI27 i powiązanych genów, uwalnia cytochrom c i aktywuje kaskadę białek popychających komórki włosowe ku programowanej śmierci. Ponieważ komórki włosowe u ludzi nie odrastają łatwo, ich utrata prowadzi do trwałych deficytów słuchu. Pokazanie, że przyciszenie IFI27 może stłumić ten destrukcyjny kaskad w komórkach ludzkich, wskazuje IFI27 jako obiecujący cel dla leków lub terapii genowych. Choć takie terapie są wciąż odległe i prawdopodobnie będą musiały być podawane bardzo wcześnie w życiu — praca ta oferuje konkretną molekularną mapę drogową, zmieniając dawniej tajemniczą mutację genu w potencjalnie możliwą do zapobiegania przyczynę dziecięcej głuchoty.
Cytowanie: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
Słowa kluczowe: genetyczna utrata słuchu, mutacja GJB2, model zebrafish (danio pręgowany), mitochondrialna apoptoza, IFI27