Clear Sky Science · pl
Skuteczna apoptoza poprzez podwójne uszkodzenia nici DNA w ludzkich komórkach nabłonkowych indukowane nietermicznym działaniem wysokopolowych szerokopasmowych fal terahercowych
Nowe światło na zabijanie komórek nowotworowych
Leczenie nowotworów często balansuje na ostrzu noża: musi zniszczyć komórki guza, nie szkodząc przy tym znacząco tkance zdrowej ani układowi odpornościowemu. W tym badaniu zbadano nietypowe narzędzie do tego zadania — intensywne fale terahercowe (THz), rodzaj niewidzialnego promieniowania pośredniego między mikrofale a podczerwienią. Naukowcy pokazują, że precyzyjnie dostrojone, wysokopolowe impulsy THz mogą wywołać w komórkach nowotworowych kontrolowany proces „samobójczy”, bez przegrzewania tkanek i bez brutalnej śmierci komórkowej prowadzącej do zapalenia.
Dlaczego delikatna śmierć komórki ma znaczenie
Wiele powszechnych terapii przeciwnowotworowych skłania komórki ku śmierci, lecz często kosztem szkód ubocznych. Leki i środki biologiczne mogą stracić skuteczność w miarę rozwoju oporności nowotworu i osłabiać układ odpornościowy. Metody fizyczne, takie jak promieniowanie rentgenowskie, radioaktywność czy ablacja termiczna, mogą uszkadzać otaczającą zdrową tkankę, często powodując nekrozę — gwałtowną formę śmierci komórkowej wywołującą zapalenie i ból. Metoda, która zamiast tego indukuje apoptozę — uporządkowany proces autodestrukcji, w którym komórki cicho się rozkładają — mogłaby zaoferować znacznie mniej traumatyczny sposób zmniejszania guzów, zwłaszcza tych blisko skóry.
Fale terahercowe wobec komórek raka piersi
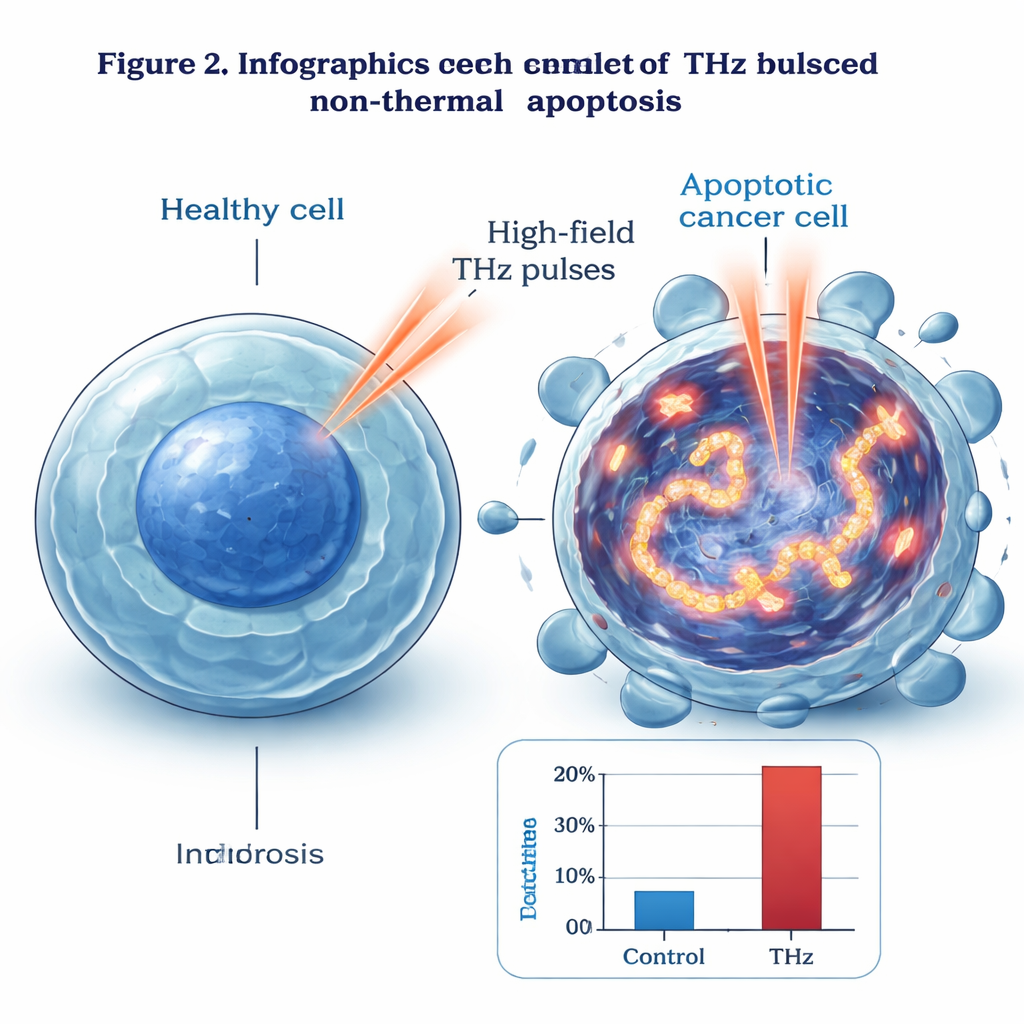
Zespół skupił się na ludzkich komórkach raka piersi (MCF‑7), rodzaju komórek nabłonkowych często używanych w badaniach laboratoryjnych. Eksponowali te komórki na bardzo silne, szerokopasmowe impulsy THz przez okres do czterech godzin, utrzymując temperaturę na poziomie fizjologicznym. Natężenia pola osiągały kilka milionów woltów na centymetr — znacznie więcej niż w codziennych urządzeniach. W tych warunkach odsetek komórek poddających się apoptozie systematycznie rósł wraz z czasem ekspozycji. Przy najwyższej testowanej intensywności THz niemal 99% komórek nowotworowych weszło w apoptozę, podczas gdy mniej niż 1% zginęło na skutek nekrozy. Ta masowa, „czysta” fala zaprogramowanej śmierci komórkowej sugeruje, że impulsy THz robią coś więcej niż tylko podgrzewają komórki.
Efekty nietermiczne i bezpieczne limity temperatury
Ze względu na silne pochłanianie promieniowania THz przez wodę oczywistym zmartwieniem jest przypadkowe nagrzewanie. Naukowcy użyli obrazowania termicznego, by śledzić zmiany temperatury podczas naświetlania. Nawet po czterech godzinach przy umiarkowanej intensywności komórki nowotworowe ogrzały się jedynie o około 3 °C, a nekroza pozostała poniżej 4%. Oddzielne eksperymenty kontrolne, w których komórki były jedynie podgrzewane przez cztery godziny, wykazały, że temperatury poniżej 41 °C powodowały niemal brak śmierci, podczas gdy gwałtowny wzrost nekrozy następował powyżej 43 °C. Nawet przy najbardziej intensywnych ustawieniach THz badacze utrzymywali temperaturę komórek na poziomie nieprzekraczającym tego progu 43 °C i wciąż obserwowali niemal całkowitą apoptozę przy minimalnej nekrozie. Obniżając częstotliwość powtarzania impulsów, wykazali, że można kontrolować temperaturę przy zachowaniu silnych efektów przeciwnowotworowych, co podkreśla, że działa mechanizm nietermiczny.
Rozrywanie DNA i włączanie genów śmierci
Aby odnaleźć ten mechanizm, grupa zajrzała do wnętrza komórek. W mikroskopie elektronowym komórki traktowane THz wykazywały klasyczne wczesne cechy apoptozy: skondensowany materiał genetyczny, zmienione jądra i nienaruszone błony zewnętrzne. Używając fluorescencyjnego markera γ‑H2AX wykryto rozległe podwójne przerwania nici DNA — uszkodzenia znacznie częstsze w komórkach naświetlonych niż w kontrolach nieleczonych lub lekko podgrzanych. Wzór uszkodzeń odpowiadał profilowi intensywności wiązki THz, nasilając się w kierunku jej środka. Analizy genów i białek ujawniły silną aktywację zestawu cząsteczek reagujących na stres i uszkodzenia, takich jak GADD45B i c‑Jun, podczas gdy znane elementy tradycyjnych ścieżek śmierci komórkowej, w tym p53 i wiele kaspaz, nie zmieniały się znacząco. Autorzy proponują, że intensywne pola THz mogą wywoływać gwałtowne wibracyjne „rezonanse” w DNA, mechanicznie naprężając i łamiąc helisę, a następnie uruchamiając odrębną ścieżkę apoptozy niezależną od p53 i kaspaz.
Z naczynia laboratoryjnego do przyszłych terapii
Choć eksperymenty przeprowadzono w hodowlach komórkowych, sugerują one nowy styl fizycznej terapii przeciwnowotworowej. Wydaje się, że wysokopolowe fale THz mogą penetrować kilka milimetrów wilgotnej tkanki — wystarczająco, by dotrzeć do powierzchownych guzów — a jednocześnie szybko tracić moc, co potencjalnie oszczędza głębsze narządy. Ponieważ efekt jest głównie nietermiczny, w teorii można by niszczyć komórki nowotworowe warstwa po warstwie bez poparzenia otaczającej tkanki czy wywoływania silnego zapalenia. Przed nami jednak wiele pracy: proponowany mechanizm „rezonansu” DNA musi zostać potwierdzony, bezpieczeństwo wobec komórek normalnych wymaga gruntownych badań, a konieczne są badania na zwierzętach i próby kliniczne. Mimo to badania otwierają drzwi do koncepcji, że precyzyjnie zaprojektowane impulsy świetlne, dostrojone do naturalnych ruchów biomolekuł, mogłyby w przyszłości zapewnić precyzyjny i względnie łagodny sposób ablacji niektórych nowotworów.
Cytowanie: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Słowa kluczowe: terahercowa terapia nowotworowa, nietermiczna apoptoza, podwójne przerwania nici DNA, komórki raka piersi, fizyczna ablacja guza