Clear Sky Science · pl
Uogólnione modele naczyń krwionośnych dla onkologii opartej na magnetycznych nanocząstkach: właściwości geometryczne i mikrofluidyczne
Naprowadzanie malutkich magnesów przez organizm
Wyobraź sobie możliwość przyciągania leków przeciwnowotworowych bezpośrednio do guza za pomocą magnesu, oszczędzając resztę ciała przed ostrymi skutkami ubocznymi. Badanie to bada, jak drobne magnetyczne cząstki poruszają się przez sieci przypominające naczynia krwionośne i stawia pozornie proste pytanie: w realistycznych warunkach przepływu, czy magnesy rzeczywiście mogą skierować te cząstki tam, gdzie chcą je dostarczyć lekarze?
Dlaczego geometria naczyń i przepływ mają znaczenie
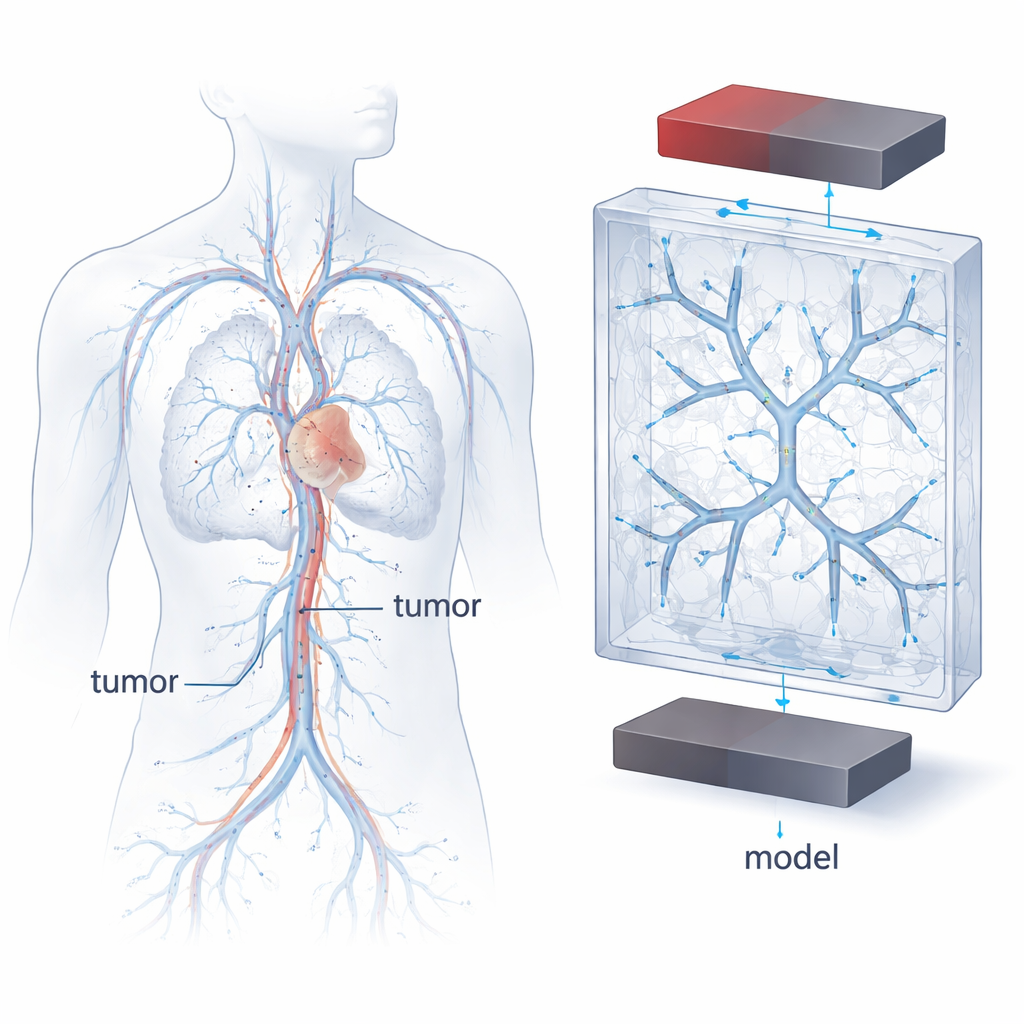
Magnetyczne terapie przeciwnowotworowe opierają się na superparamagnetycznych tlenkach żelaza — SPIONach — które można przyciągać polem magnetycznym, gdy niosą leki przez krwiobieg. Jednak naczynia krwionośne nie są prostymi, prostymi rurami: rozgałęziają się, zwężają, zakrzywiają i dzielą, a prędkość krwi przyspiesza lub zwalnia w odpowiedzi. Zmiany kształtu i prędkości wpływają na ruch cząstek, miejsca ich koncentracji i to, czy mają wystarczająco długi kontakt ze ściankami naczyń, by się przyczepić. Rzeczywiste naczynia u pacjentów są niezwykle zróżnicowane, co utrudnia porównywanie eksperymentów lub przewidywanie zachowania nowej terapii. Autorzy postanowili więc zbudować wysoko kontrolowaną, powtarzalną „modelową sieć naczyń”, która jednocześnie odzwierciedla istotne cechy naczyń odżywiających guz.
Budowanie idealizowanych sieci naczyniowych guza
Aby zaprojektować te modelowe naczynia, zespół sięgnął po klasyczne reguły opisujące rozgałęzianie się prawdziwych tętnic. Jedną z takich reguł jest prawo Murray’ego, łączące średnice naczyń macierzystych i potomnych w energetycznie efektywnej sieci. Korzystając z pomiarów klinicznych z nowotworów piersi i tych praw skalowania, badacze matematycznie wygenerowali drzewa rozgałęzień naśladujące sposób, w jaki naczynia odżywiające guz kurczą się w kierunku sieci włosowatych. Następnie wykorzystali druk 3D o wysokiej rozdzielczości, aby osadzić puste kanały o dwóch, trzech lub czterech poziomach rozgałęzień w przeźroczystych blokach plastiku. Kanały układały się w symetryczny wzór rozgałęzień i rozciągały w trzech wymiarach, oferując uproszczony, lecz fizjologicznie inspirowany pejzaż do badania ruchu cząstek.
Obserwowanie magnetycznych cząstek w akcji
Przez te wydrukowane sieci zespół przepompowywał wodę jako substytut krwi, następnie wprowadzał płyn zawierający SPIONy do górnego odcinka i stosował statyczne pole magnetyczne wokół modelu. Szybkie nagrania dostarczały filmowej dokumentacji tego, jak ciemne obłoki cząstek przemieszczały się przez różne odgałęzienia, podczas gdy analiza komputerowa przetwarzała zmiany jasności na sygnały czasowe odzwierciedlające lokalną obecność cząstek. Poprzez zmianę prędkości przepływu, stężenia cząstek, złożoności rozgałęzień oraz obecności lub braku magnesu, badacze mogli rozdzielić wpływ każdego czynnika na rozkład cząstek, czas ich zalegania i ostateczne osadzanie na ściankach kanałów.
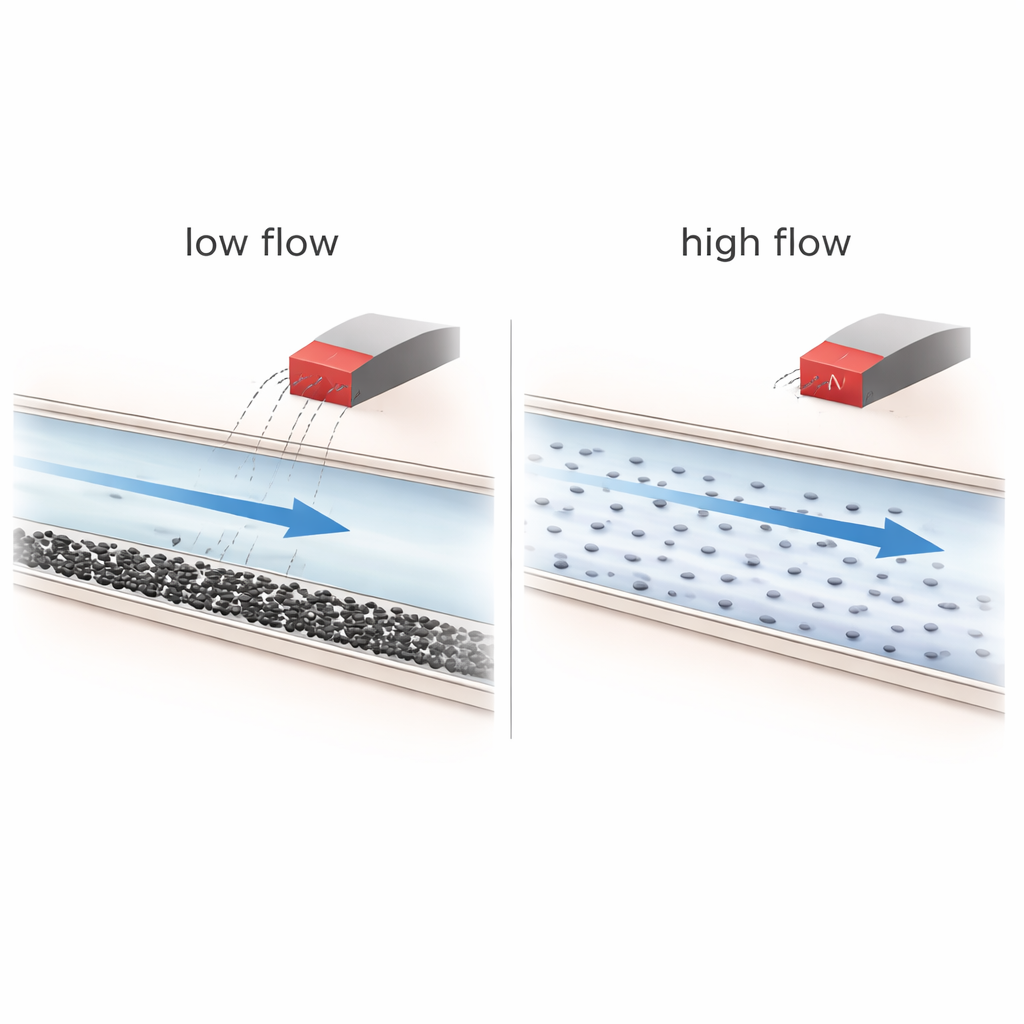
Kiedy magnesy pomagają — a kiedy nie
Eksperymenty pokazują, że warunki przepływu dominują w tej opowieści. Przy wyższych prędkościach przepływu płyn dobrze się miesza, a nanocząstki przemieszczają się szybko; w takich warunkach pole magnetyczne ma prawie żaden wpływ, a cząstki po prostu podążają za liniami prądu w sieci. Przy niskich prędkościach przepływu natomiast grawitacja i efekty stężeniowe powodują osiadanie cząstek ku dnu kanałów, tworząc warstwy stratygrafii, a czasem luźne skupiska. W tej już nierównomiernej sytuacji magnes może popchnąć więcej cząstek w określone odgałęzienia i nieco wydłużyć ich czas zalegania, szczególnie w bardziej złożonych, silnie rozgałęzionych sieciach. Jednak obliczenia pokazują, że siła magnetyczna działająca na pojedynczą cząstkę o średnicy 40 nanometrów jest wielokrotnie mniejsza niż siła lepkości wynikająca z płynącego płynu, co sprawia, że prawdziwe „sterowanie pojedynczą cząstką” jest fizycznie nierealistyczne w testowanych warunkach.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla laika główny wniosek jest taki, że same magnesy nie są w stanie wiarygodnie wyciągnąć swobodnie zawieszonych nanocząstek z szybko płynącego krwiobiegu. Zauważalne efekty magnetyczne pojawiają się jedynie wtedy, gdy cząstki już zwolniły, osiadły lub zgromadziły się w skupiska — sytuacje, które skutecznie wzmacniają ich odpowiedź magnetyczną. Uogólnione, drukowane w 3D modele naczyń przedstawione tutaj dostarczają ustandaryzowanego sposobu badania takich efektów w różnych geometriach sieci i reżimach przepływu. Dla przyszłego magnetycznego ukierunkowania leków praca ta sugeruje, że skuteczne strategie prawdopodobnie będą musiały wykorzystywać zachowania zbiorowe — takie jak kontrolowana agregacja lub systemy nośnikowe — zamiast polegać na naprowadzaniu pojedynczych nanocząstek przez duże, szybko perfundowane naczynia.
Cytowanie: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Słowa kluczowe: magnetyczne celowanie leków, nanocząstki, unaczynienie guza, modele mikrofluidyczne, dostarczanie leków