Clear Sky Science · pl
Celowanie w oś Akt–EphA2 i adhezję międzykomórkową zwiększa wrażliwość komórek nowotworowych na anoikę
Dlaczego unoszące się komórki nowotworowe mają znaczenie
Gdy komórki nowotworowe odrywają się od guza i przemieszczają się przez krwiobieg, przy normalnych warunkach powinny obumrzeć, ponieważ tracą kontakt z otaczającą tkanką. Ten wbudowany mechanizm bezpieczeństwa, zwany śmiercią komórkową wywołaną odłączeniem, pomaga powstrzymać rozwój tkanek w nieodpowiednich miejscach. Komórki przerzutowe często jednak uczą się ignorować ten sygnał i pozostawać przy życiu podczas unoszenia się, co ułatwia im zainicjowanie nowych guzów. W tym badaniu zadano pozornie proste pytanie: czy przywrócenie kluczowego mechanicznego „zmysłu dotyku” w agresywnych komórkach raka piersi może zmusić te wędrujące komórki do śmierci, a jeśli nie — jakimi zapasowymi sztuczkami posługują się, by przetrwać?
Przywracanie utraconego zmysłu dotyku
Komórki nieustannie sprawdzają, jak sztywne jest ich otoczenie, pociągając za struktury, które je kotwiczą. W zdrowej tkance utrata kontaktu lub osadzenie się na bardzo miękkiej powierzchni zwykle uruchamia samozniszczenie. Białko Tropomiozyna 2.1 (Tpm2.1) jest istotnym elementem tej wewnętrznej maszyny napięcia i często jest nieobecne lub obniżone w komórkach nowotworowych. Badacze użyli szeroko badanej linii komórek przerzutowego raka piersi i zmodyfikowali ją tak, by produkowała więcej Tpm2.1, przywracając w dużej mierze zdolność wyczuwania sztywności. Gdy zmodyfikowane komórki zmuszono do wzrostu w specjalnych nienasiąkających naczyniach uniemożliwiających przyczepność, rzeczywiście nastąpiło więcej zgonów komórkowych, wolniejszy wzrost i mniejsza migracja niż w komórkach niemodyfikowanych. Jednak nawet po kilku dniach w zawiesinie około 70% komórek eksprymujących Tpm2.1 było nadal żywych, co sugeruje, że samo przywrócenie zmysłu dotyku nie rozwiązuje problemu w pełni.
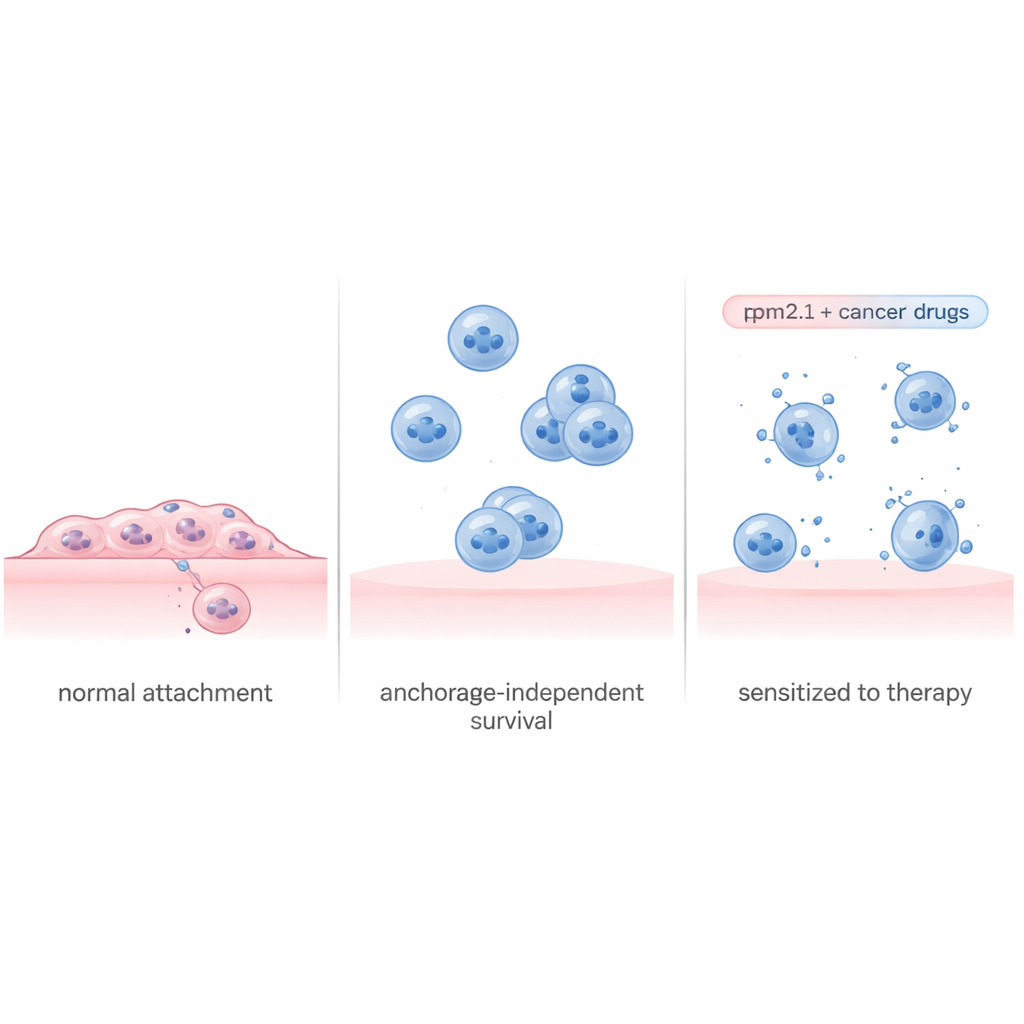
Odczytywanie podręcznika przetrwania komórek nowotworowych
Aby zrozumieć, dlaczego niektóre komórki ginęły, a inne przeżywały, zespół podzielił unoszące się komórki eksprymujące Tpm2.1 na dwie grupy: te wykazujące wczesne oznaki śmierci komórkowej oraz te, które wyglądały na zdrowe. Następnie mierzono, które geny były włączone lub wyłączone w każdej grupie na przestrzeni czterech dni. Komórki umierające wykazały szerokie wyciszenie programów zaangażowanych w podział komórkowy, naprawę DNA i przyleganie, wraz z sygnałami stresowymi wyglądającymi na jednokierunkową drogę do samozniszczenia. Natomiast komórki przetrwałe uruchomiły skoordynowany plan przetrwania. Wczesnie po odłączeniu włączyły szlaki zapalne i związane z układem odpornościowym, a później zwiększyły aktywność głównych obwodów wzrostu i przeżycia, w tym znanego szlaku związanego z białkiem Akt. Jednocześnie zdecydowanie wzmocniły geny ułatwiające przyleganie komórek do siebie, co pozwoliło im tworzyć ochronne skupiska nawet bez przyczepiania się do macierzy zewnątrzkomórkowej.
Siła w liczbie: jak skupiska komórek opierają się śmierci
Ponieważ dane genetyczne wskazywały na zwiększoną adhezję międzykomórkową, badacze sprawdzili, czy zwykłe tłoczenie się może pomóc komórkom przetrwać w zawiesinie. Gdy komórki eksprymujące Tpm2.1 rosły w dużym zagęszczeniu, gdzie tworzenie skupisk było łatwe, znacznie mniej komórek ginęło niż gdy utrzymywano je rozproszone. Jedna cząsteczka adhezyjna, ICAM1, wyróżniała się jako szczególnie podwyższona w komórkach przetrwałych i jest już znana z roli w tworzeniu skupisk krążących komórek nowotworowych oraz ich osadzaniu się w odległych tkankach. Blokowanie ICAM1 małą cząsteczką zwiększało liczbę umierających komórek eksprymujących Tpm2.1 w zawiesinie, przy niewielkim wpływie na standardowe hodowle przyczepne. Wyniki te wspierają koncepcję, że po częściowym przywróceniu wewnętrznej mechaniki komórki nowotworowe nadal mogą uniknąć śmierci, dosłownie trzymając się nawzajem zamiast środowiska.
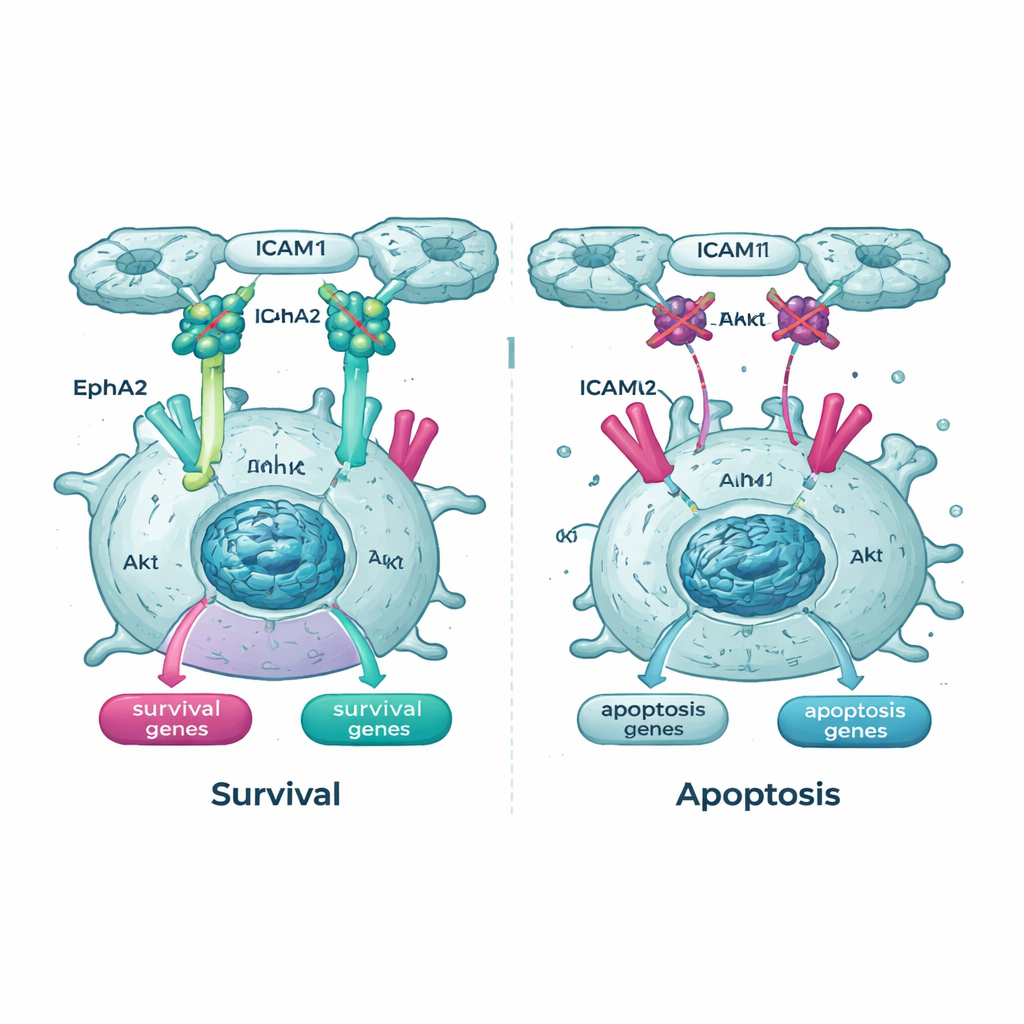
Odcięcie kluczowych lifeline’ów wewnątrz komórki
Przeglądy genetyczne podkreśliły również szlak Akt i jednego z jego partnerów — receptor o nazwie EphA2 — jako ważne lifeline’y dla zawieszonych komórek nowotworowych. W komórkach eksprymujących Tpm2.1 aktywna, ufosforylowana forma Akt była niższa w zawiesinie niż w komórkach kontrolnych, a poziomy i aktywność EphA2 również były zmniejszone. Gdy zespół leczył komórki lekami blokującymi Akt lub EphA2, zarówno komórki normalne, jak i eksprymujące Tpm2.1 stały się znacznie bardziej podatne na śmierć w zawiesinie. Co istotne, komórki z przywróconym czuciem sztywności były szczególnie wrażliwe na te leki w czasie, co sugeruje, że po częściowym przywróceniu mechanicznych kontroli bezpieczeństwa polegają one silniej na pozostałych sygnałach przetrwania.
Przekształcenie stanu przygotowania w śmiertelną słabość
Dla niespecjalisty główny przekaz jest taki, że naprawienie jednego uszkodzonego przełącznika bezpieczeństwa w komórkach nowotworowych — ich zdolności do wyczuwania i reagowania na utratę kontaktu — jest konieczne, ale niewystarczające, by sprowokować ich samozagładę. Komórki, które przeżywają, robią to, łącząc się w grupy i przekierowując swoje wewnętrzne okablowanie przez alternatywne szlaki wzrostu i przeżycia. Praca ta pokazuje, że przywrócenie czucia sztywności za pomocą Tpm2.1 wprowadza komórki przerzutowego raka piersi w „zaprzyjaźniony” stan, w którym są bliżej śmierci, ale jeszcze nie skazane. Blokując następnie szlak Akt–EphA2 i zakłócając adhezję międzykomórkową przez ICAM1, badacze mogą popchnąć te przygotowane komórki za krawędź i znacznie zwiększyć śmierć wywołaną odłączeniem. W praktycznym wymiarze badanie wytycza strategię przyszłych terapii kombinowanych mających na celu wyeliminowanie unoszących się komórek nowotworowych, zanim zdążą zaszczepić nowe przerzuty.
Cytowanie: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Słowa kluczowe: przerzuty raka piersi, adhezja komórek, anoika, szlak sygnalizacyjny Akt, czucie sztywności