Clear Sky Science · pl
Fioletowe światło LED i surowy gliceryna synergicznie zwiększają produkcję astaksantyny w Aurantiochytrium limacinum
Dlaczego świecące mikroby mogą mieć dla ciebie znaczenie
Barwne związki ze świata mikroskopijnego cicho przekształcają sposoby wytwarzania suplementów diety, kosmetyków, a nawet paszy dla ryb. W tym badaniu sprawdzono, jak drobny organizm morski Aurantiochytrium limacinum można skłonić przy pomocy fioletowego światła LED i tanich przemysłowych produktów ubocznych do wytwarzania cennych cząsteczek, takich jak astaksantyna — silny czerwony przeciwutleniacz występujący także w łososiu i krewetkach — obok zdrowych olejów omega‑3, np. DHA. Praca wskazuje drogę do bardziej zrównoważonych, tańszych metod produkcji tych składników, bez polegania na dzikich rybach czy energochłonnych fabrykach chemicznych.
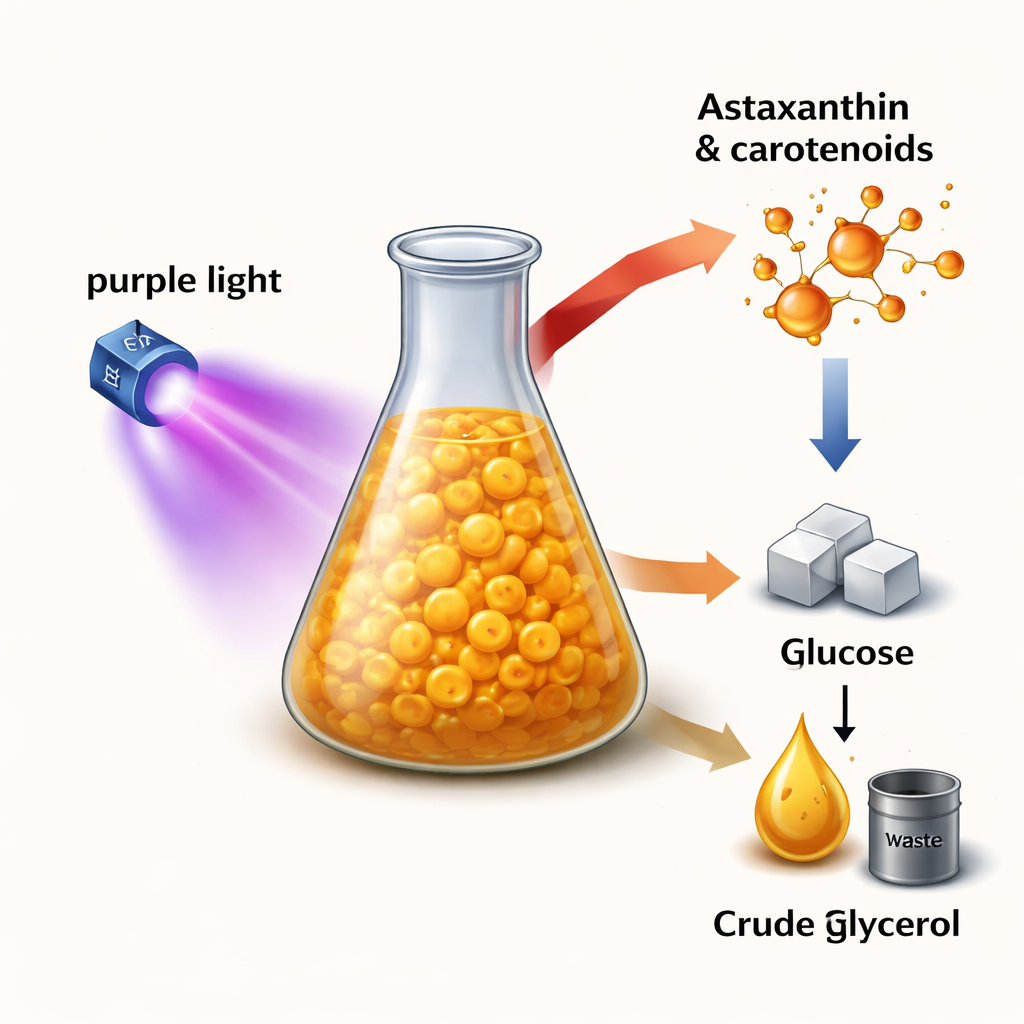
Maleńka fabryka z morza
Aurantiochytrium limacinum to mikroskopijny protist morski, który dobrze rozwija się w ciemności i wykorzystuje organiczny węgiel zamiast światła słonecznego. Jest atrakcyjny dla przemysłu, ponieważ potrafi jednocześnie wytwarzać dwa wartościowe produkty: DHA, tłuszcz omega‑3 ważny dla zdrowia mózgu i serca, oraz karotenoidy — pigmenty nadające wielu roślinom i zwierzętom żółte, pomarańczowe i czerwone barwy. Wśród tych karotenoidów astaksantyna wyróżnia się silnymi właściwościami przeciwutleniającymi i przeciwzapalnymi, co zwiększa popyt w suplementach, żywności funkcjonalnej i produktach do pielęgnacji skóry. Do tej pory większość astaksantyny pochodziła albo z oleju rybnego, albo z energochłonnej syntezy chemicznej, co budzi obawy o zrównoważony rozwój i bezpieczeństwo.
Właściwy kolor światła
Naukowcy zbadali, jak różne kolory światła — ciemność, zwykłe białe światło i wąskopasmowe fioletowe diody LED (410–420 nm) — wpływają na produktywność tego mikroorganizmu. Hodowali kultury na glukozie (prosty cukier) lub na glicerynie jako głównym źródle węgla, a następnie mierzyli wzrost komórek, magazynowanie tłuszczu i poziomy karotenoidów. Komórki rosły równie dobrze przy wszystkich kolorach światła, a ich całkowita zawartość tłuszczu pozostawała na podobnym poziomie. Zmienił się natomiast skład pigmentów: światło fioletowe prowadziło do najwyższych poziomów karotenoidów, następnie białe światło, a najmniej produkowano w ciemności. Zarówno β‑karoten, jak i kanthaksantyna — pomarańczowe pigmenty występujące wcześniej w ścieżce biosyntezy astaksantyny — znacznie wzrosły pod wpływem fioletowego światła, szczególnie gdy źródłem węgla była gliceryna. Sama astaksantyna była jednak najliczniej obecna w kulturach zasilanych glukozą, co pokazuje, że kolor światła i rodzaj pożywienia subtelnie kierują, jak daleko w ścieżce pigmentów komórki posuwają się.
Przekształcanie odpadów w kolor i olej
Głównym wyzwaniem w komercjalizacji tego mikroorganizmu są koszty jego dokarmiania. Glukoza jest stosunkowo droga w skali przemysłowej, natomiast produkcja biodiesla generuje duże ilości surowej gliceryny — niskowartościowego produktu ubocznego, którego utylizacja bywa problematyczna. Autorzy sprawdzili, czy tę nieczystą glicerynę można oczyścić na tyle, by posłużyła jako użyteczne substrat. Po prostych zabiegach — rozcieńczeniu, zakwaszeniu w celu usunięcia mydeł i soli oraz w niektórych przypadkach dodatkowym oczyszczeniu na węglu aktywowanym — surowa gliceryna wspierała wzrost mikroorganizmów porównywalny z obserwowanym przy użyciu czystej glukozy lub gliceryny. Przy fioletowym świetle LED kultury hodowane na oczyszczonej surowej glicerynie wytwarzały wysokie poziomy β‑karotenu i kanthaksantyny, a ostateczne ilości astaksantyny były porównywalne z tymi z standardowych pożywek, przy jednoczesnym utrzymaniu produkcji lipidów neutralnych (oleju).
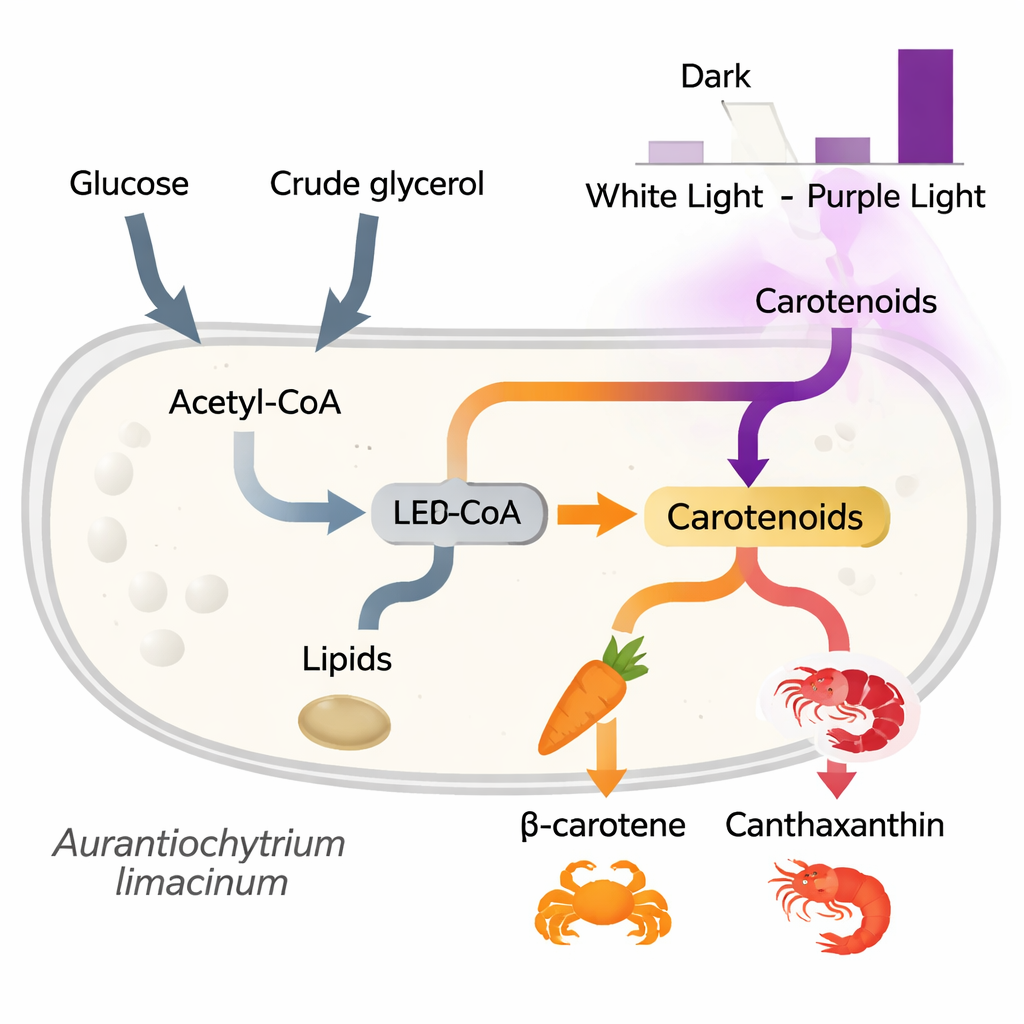
Zajrzeć pod maskę komórki
Aby zrozumieć, jak światło i rodzaj pożywienia przekształcają metabolizm, zespół przeanalizował także, które geny były włączane lub wyłączane w różnych warunkach, wykorzystując sekwencjonowanie RNA. Stwierdzili, że geny zaangażowane w pobieranie i przetwarzanie gliceryny były silnie aktywowane, gdy gliceryna była źródłem węgla, co potwierdza, że komórki potrafią efektywnie kierować ten pochodzący z odpadów węgiel do metabolizmu centralnego. Co zaskakujące, wiele genów związanych z syntezą tłuszczów i karotenoidów było mniej aktywnych we wczesnym punkcie czasowym pod wpływem fioletowego światła, mimo że poziomy pigmentów były wyższe później. Ten wzorzec sugeruje, że komórki mogą najpierw osłabić niektóre procesy w odpowiedzi na stres świetlny, a następnie zwiększyć produkcję pigmentów jako późniejszą reakcję ochronną, wykorzystując karotenoidy jako naturalne „filtry przeciwsłoneczne” i przeciwutleniacze.
Co to oznacza dla przyszłych produktów
Dla osób niezajmujących się specjalistycznie tematem kluczowy wniosek jest taki, że staranne dostrojenie zarówno oświetlenia, jak i diety może przemienić morski mikroorganizm w elastyczną, niskokosztową fabrykę składników związanych ze zdrowiem. Fioletowe światło LED zwiększa produkcję barwnych, ochronnych pigmentów bez poświęcania wytwarzania korzystnych olejów, podczas gdy umiarkowanie oczyszczona surowa gliceryna — zasadniczo strumień odpadów przemysłowych — może zastąpić droższe cukry jako podstawowe źródło pożywienia. Razem te strategie wskazują drogę do bardziej zielonej, ekonomicznej produkcji astaksantyny i DHA, zmniejszając presję na dzikie połowy i chemię opartą na paliwach kopalnych, jednocześnie wykorzystując dyskretną moc biotechnologii mikrobiologicznej.
Cytowanie: Yamakawa, K., Kawano, K., Kato, S. et al. Purple LED light and crude glycerol synergistically enhance astaxanthin production in Aurantiochytrium limacinum. Sci Rep 16, 6623 (2026). https://doi.org/10.1038/s41598-026-37313-4
Słowa kluczowe: astaksantyna, Aurantiochytrium, fioletowe światło LED, surowa gliceryna, mikrobowe bioprodukty