Clear Sky Science · pl
TRMT6 łagodzi podatność i przebieg zapalenia okrężnicy wywołanego DSS na wieloraki sposób poprzez regulację translacji
Dlaczego to badanie jelit ma znaczenie
Choroba zapalna jelit (IBD) — obejmująca chorobę Leśniowskiego–Crohna i wrzodziejące zapalenie jelita grubego — dotyka miliony ludzi na całym świecie i może powodować przewlekły ból, krwawienia, utratę masy ciała i zmęczenie. U podstaw tych schorzeń leży kruche, jednowarstwowe wyłożenie jelita, które musi nieustannie się naprawiać, jednocześnie powstrzymując tryliony mikroorganizmów. To badanie odkrywa wcześniej niedocenianego molekularnego „opiekuna”, białko o nazwie TRMT6, które pomaga komórkom jelitowym rosnąć, goić się i regulować swój metabolizm. Zrozumienie, jak działa TRMT6, może otworzyć nowe drogi do łagodniejszych, bardziej ukierunkowanych terapii IBD.
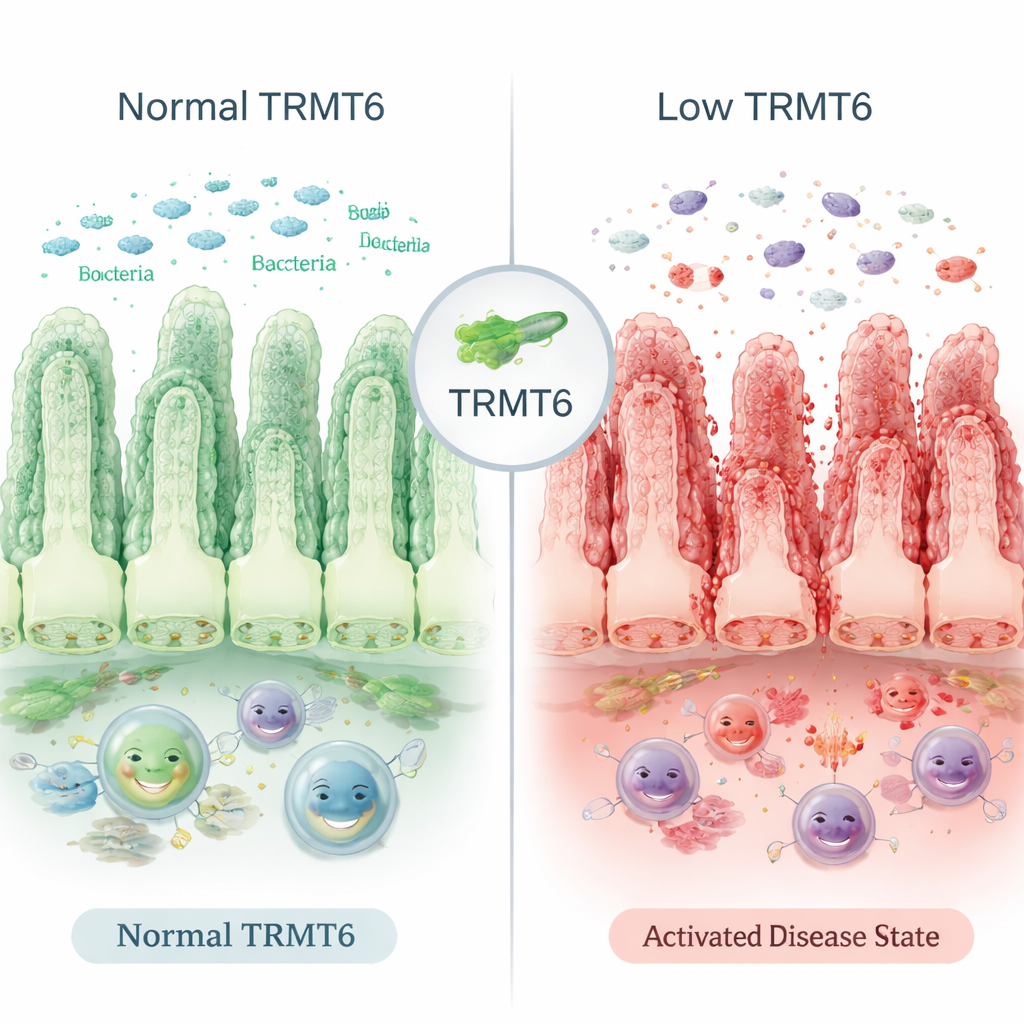
Mikroskopijny strażnik ściany jelita
Wewnętrzna powierzchnia jelita pokryta jest jedną warstwą komórek, która odnawia się co kilka dni. Ten żywy dywan działa jako bariera, oddzielając bakterie jelitowe od tkanek organizmu. Badacze stwierdzili, że TRMT6, enzym obecny w tych komórkach jelitowych, jest zmniejszony w próbkach tkanek od osób z aktywną IBD oraz u myszy z chemicznie wywołanym zapaleniem okrężnicy. TRMT6 nie zmienia sekwencji DNA; zamiast tego subtelnie modyfikuje RNA — robocze kopie informacji genetycznej, które kierują produkcją białek — w sposób wpływający na efektywność syntezy białek. Gdy poziomy TRMT6 spadają, proces wytwarzania białek słabnie, a wyściółka jelita staje się bardziej podatna na uszkodzenia.
Co się dzieje, gdy TRMT6 jest wyłączone
Aby sprawdzić, jak ważne jest TRMT6, zespół zaprojektował myszy, u których TRMT6 został specyficznie usunięty w komórkach jelita cienkiego. W normalnych warunkach zwierzęta te wyglądały zdrowo, a ich jelita wydawały się w dużej mierze prawidłowe w badaniu mikroskopowym. Jednak po wystawieniu myszy na działanie chemicznego czynnika (DSS), który drażni przewód pokarmowy i jest powszechnie stosowany do modelowania zapalenia okrężnicy, obraz zmienił się dramatycznie. W porównaniu z normalnymi rodzeństwem, myszy pozbawione TRMT6 traciły więcej masy ciała, miały krótsze i bardziej obrzęknięte okrężnice oraz wykazywały głębsze uszkodzenia w jelicie cienkim. Drugi model genetyczny, w którym TRMT6 usunięto tylko z komórek macierzystych jelita — komórek stale odnawiających wyściółkę — dał podobnie ciężki przebieg choroby, potwierdzając, że enzym jest szczególnie istotny w tej odnawiającej się populacji komórek.
Spowolniona naprawa, zaburzony użytek paliwa i nieposłuszne mikroby
Bliższa analiza tkanki jelitowej ujawniła, dlaczego brak TRMT6 jest tak szkodliwy podczas zapalenia okrężnicy. W uszkodzonym jelicie było więcej komórek przechodzących zaprogramowaną śmierć komórkową i mniej komórek aktywnie dzielących się, co wykazano standardowymi barwieniami histologicznymi. Kluczowy regulator wzrostu, białko MYC, był wyraźnie zredukowany na poziomie białka, mimo że jego informacyjny RNA zmniejszył się tylko nieznacznie. Ta rozbieżność sugeruje, że TRMT6 pomaga komórkom jelitowym efektywnie tłumaczyć RNA MYC na białko, umożliwiając szybką naprawę wyściółki. Aby pójść dalej, badacze połączyli pomiary na dużą skalę RNA, białek, małych cząsteczek (metabolitów) i DNA bakteryjnego. Te analizy „multi‑omics” wykazały, że utrata TRMT6 zaburza białka zaangażowane w gospodarkę tłuszczową i pobór składników odżywczych, zmienia poziomy wielu lipidopodobnych cząsteczek i kwasów organicznych w jelicie i krwi oraz przesuwa równowagę drobnoustrojów jelitowych z kilku korzystnych grup w stronę gatunków powiązanych z zapaleniem.
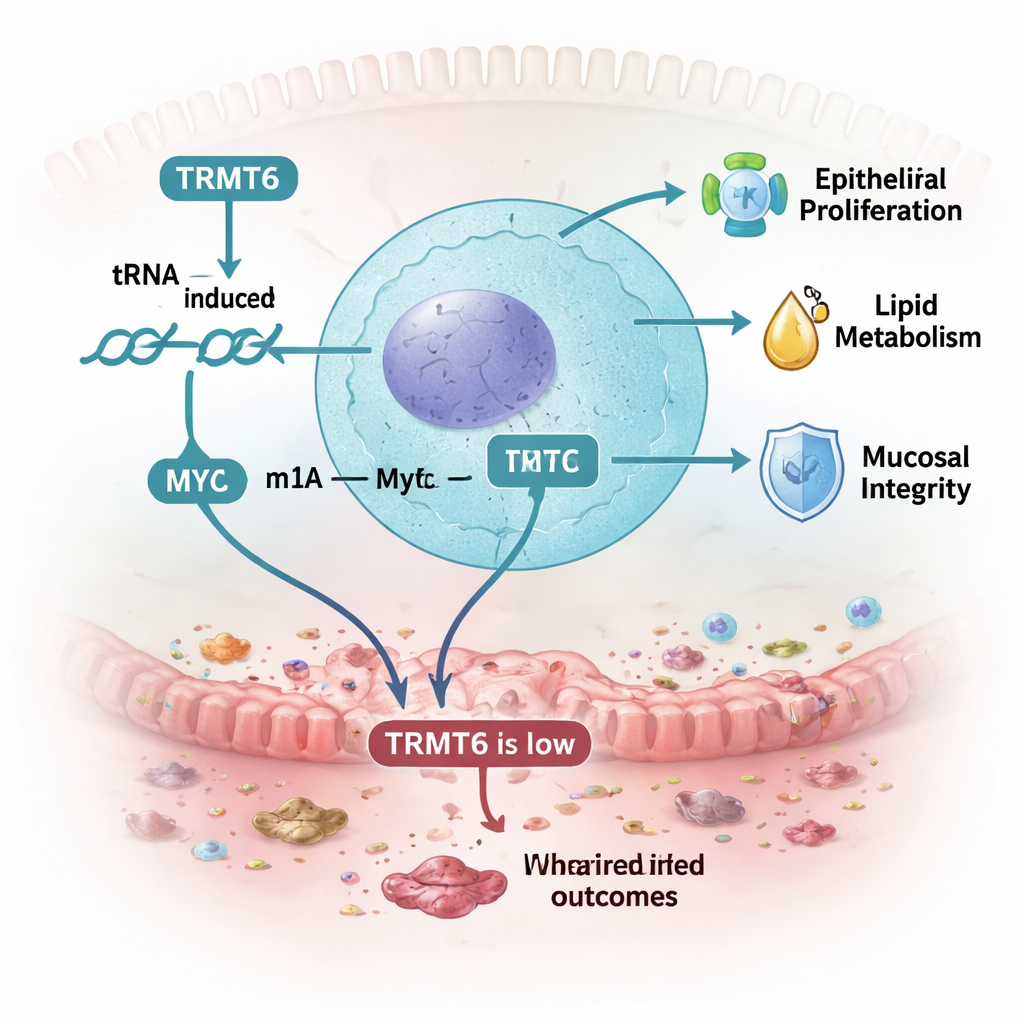
Molekularne centrum łączące barierę, metabolizm i zapalenie
W sumie wyniki przedstawiają TRMT6 jako centralne centrum, które pomaga wyściółce jelita radzić sobie ze stresem. Poprzez dokładne regulowanie konkretnej chemicznej modyfikacji tRNA, TRMT6 wspiera produkcję MYC i innych białek napędzających odnowę komórek, regulujących przetwarzanie lipidów i utrzymujących szczelne oddzielenie organizmu od zamieszkujących go mikroorganizmów. Gdy TRMT6 jest nieobecne lub zredukowane, ściana jelita naprawia się wolniej, wchłanianie składników odżywczych jest mniej wydajne, a warunki sprzyjają powstaniu bardziej szkodowej społeczności mikrobiologicznej. Pod wpływem dodatkowego czynnika zapalnego te słabości przekładają się na cięższe zapalenie okrężnicy u myszy, co odzwierciedla zmniejszone poziomy TRMT6 obserwowane w ludzkich tkankach IBD.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że IBD to nie tylko problem układu odpornościowego; wynika też z niepowodzeń w codziennym utrzymaniu komórek jelitowych. TRMT6 wyłania się jako jedno z narzędzi komórki do utrzymania równowagi między produkcją białek, metabolizmem i naprawą bariery. Chociaż badania te znajdują się wciąż we wczesnym, przedklinicznym etapie, sugerują, że łagodne zwiększenie aktywności TRMT6 lub naśladowanie jego efektów na RNA i syntezę białek mogłoby pewnego dnia pomóc wzmocnić wyściółkę jelita i złagodzić zapalenie u osób z IBD. Potrzebne będą większe badania w różnych modelach choroby i na próbkach pacjentów, ale praca ta wskazuje nowy, bardziej precyzyjny kierunek w walce z przewlekłym zapaleniem jelit.
Cytowanie: Zhang, X., Du, Y., Ye, Y. et al. TRMT6 mitigates susceptibility and progression of DSS-induced colitis multifacetedly via translational regulation. Sci Rep 16, 6809 (2026). https://doi.org/10.1038/s41598-026-37299-z
Słowa kluczowe: choroba zapalna jelit, bariera jelitowa, modyfikacja RNA, mikrobiom jelitowy, metabolizm jelitowy