Clear Sky Science · pl
Wpływ zdefiniowanej mikrobiofy Oligo-MM12 na kolonizację jelit i szerzenie się Listeria monocytogenes
Dlaczego drobnoustroje w twoich jelitach mają znaczenie
Wielu ludzi kojarzy Listeria monocytogenes jako groźny drobnoustrój przenoszony przez żywność, związany z zanieczyszczonymi produktami gotowymi do spożycia i ciężkimi zachorowaniami u osób wrażliwych. Mniej oczywiste jest to, że to, czy ta bakteria zyska przyczółek w organizmie, zależy nie tylko od naszego układu odpornościowego, lecz także od tętniącej życiem społeczności mikroorganizmów już zamieszkujących jelita. W tym badaniu wykorzystano specjalnie zaprojektowane modele myszy i miniaturowy „sztuczny okrężnicę”, aby postawić proste, lecz ważne pytanie: jak złożoność mikrobiomu jelitowego wpływa na zdolność Listerii do kolonizacji jelita i rozprzestrzeniania się w organizmie?
Opowieść o dwóch mikrobiologicznych sąsiedztwach
Aby rozwiązać to zagadnienie, badacze porównali dwa rodzaje myszy. Jedna grupa, nazywana myszami SPF, miała bogaty, naturalny zestaw bakterii jelitowych podobny do tego wykrywanego u wielu zwierząt laboratoryjnych. Druga grupa, myszy Oligo-MM12, była zasiedlona znacznie prostszą społecznością składającą się z zaledwie 12 dobrze scharakteryzowanych szczepów bakterii. Ponieważ każdy składnik tej społeczności jest znany i stabilny w kolejnych pokoleniach, myszy Oligo-MM12 są potężnym narzędziem do rozbijania, które mikroby pomagają zablokować intruzów, a które mogą pozostawiać luki w naszej obronie. Porównując te myszy, zespół mógł sprawdzić, jak gęsty, zróżnicowany ekosystem jelitowy różni się od uproszczonego, minimalistycznego w radzeniu sobie z wyzwaniem infekcyjnym.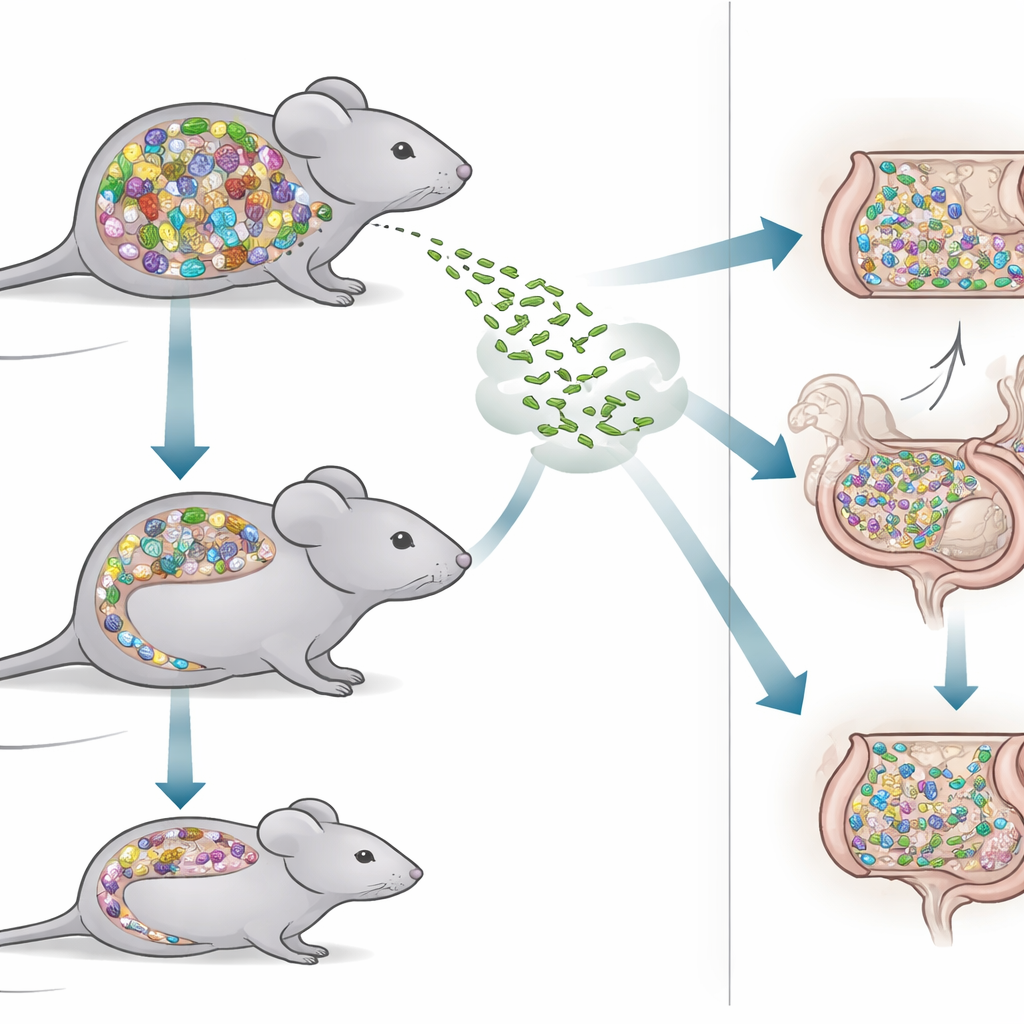
Śledząc Listerię przez jelito i poza nie
Naukowcy zakażali obydwa typy myszy tą samą doustną dawką Listerii i monitorowali, ile bakterii pojawiało się w kale i narządach wewnętrznych przez trzy dni. Co ciekawe, prostsza społeczność Oligo-MM12 początkowo wydawała się lepiej powstrzymywać Listerię: pierwszego dnia po zakażeniu te myszy wydalały mniej komórek Listerii w stolcu niż myszy SPF. Jednak ta wczesna przewaga zanikła. Do trzeciego dnia myszy Oligo-MM12 wydalały więcej Listerii, podczas gdy myszy SPF stopniowo obniżały jej poziomy. Pomimo wyraźnych różnic w jelicie, liczby Listerii w narządach wewnętrznych, takich jak wątroba, śledziona i węzły chłonne, były podobne między modelami myszy, co sugeruje, że gdy Listeria dociera do głębszych tkanek, złożoność mikrobiomu odgrywa mniejszą rolę.
Symulacja okrężnicy w kontrolowanym układzie
Aby oddzielić efekty tkanek gospodarza i odporności od zachowania samych mikroorganizmów, zespół przeprowadził także eksperyment ex vivo z użyciem urządzenia zwanego bioreaktorem micro-Matrix. Przygotowali zawiesiny kałowe z każdego typu myszy, dodali je do pożywki bogatej w składniki odżywcze w zamkniętych, beztlenowych studzienkach i wprowadzili Listerię do niektórych z tych miniaturowych kultur, pozostawiając inne jako kontrolne. Przez pięć dni mierzyli liczby Listerii i sekwencjonowali DNA bakterii, aby śledzić ewolucję społeczności. W tej sztucznej okrężnicy Listeria rosła do podobnych poziomów niezależnie od tego, czy stawiała czoła złożonemu mikrobiotowi SPF, czy prostszej społeczności Oligo-MM12, a jej obecność powodowała jedynie umiarkowane przesunięcia w całkowitym składzie społeczności. Kontrast z żywymi zwierzętami podkreśla, jak silnie układ odpornościowy, wyściółka jelita oraz przepływy żółci i śluzu kształtują infekcję w prawdziwym jelicie.
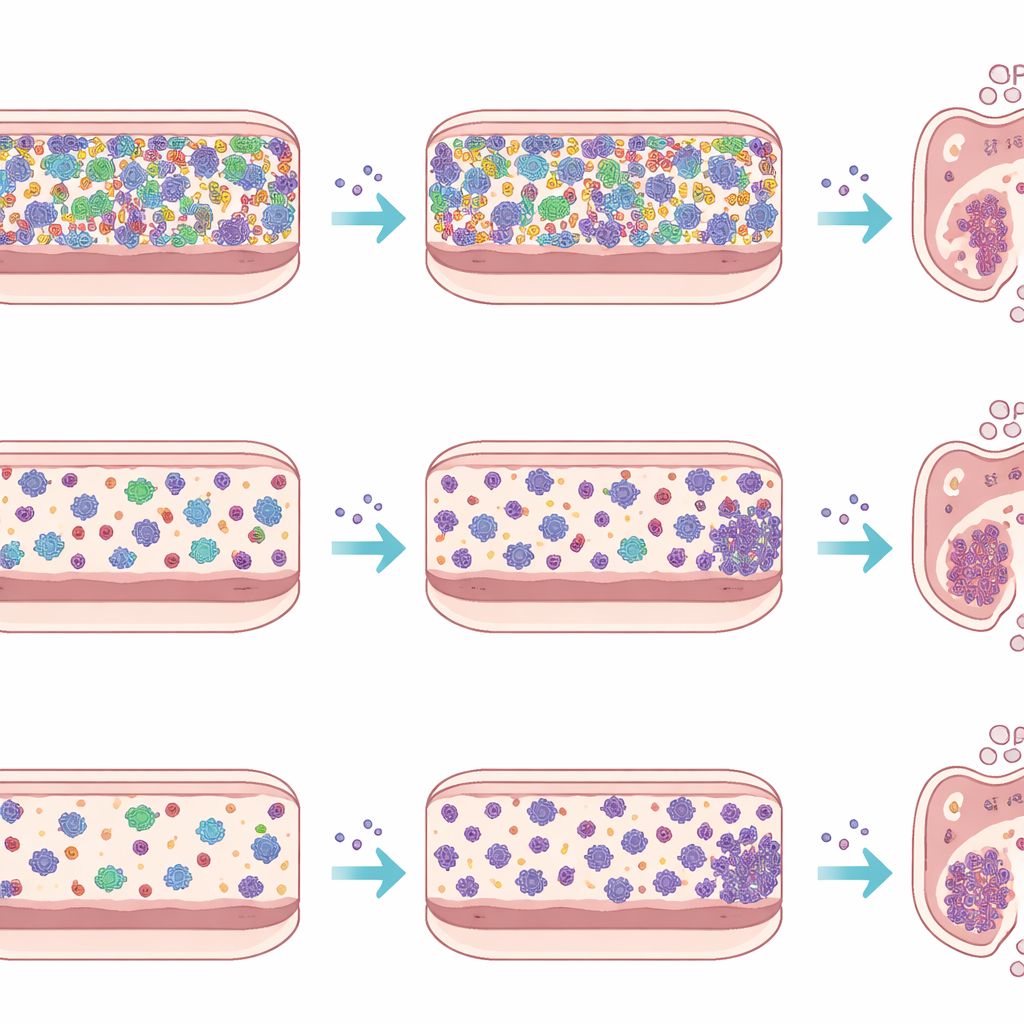
Kluczowi mikrobiologiczni zwycięzcy, przegrani i obserwatorzy
Analizując, które grupy bakterii wzrastały lub słabły podczas infekcji, badanie wskazuje kandydatów, którzy mogą wpływać na powodzenie Listerii. U myszy Oligo-MM12 poziomy Akkermansia, bakterii związanej ze śluzem i często kojarzonej ze zdrowiem jelit, spadły drugiego dnia, a następnie silnie odbiły do trzeciego dnia. U myszy SPF kilka rodzajów znanych z produkcji korzystnych metabolitów lub wspierania integralności bariery, takich jak Blautia i Bacteroides, obniżyło się podczas infekcji, podczas gdy niektóre bakterie podobne do Prevotella wykazywały złożone wzrosty i spadki, które mogą odzwierciedlać bezpośrednie ataki ze strony własnych substancji przeciwbakteryjnych Listerii. Ex vivo te wzorce były w dużej mierze stłumione, co wzmacnia ideę, że wiele zaobserwowanych zmian wynika z trójstronnych interakcji między patogenem, rezydentnymi mikroorganizmami i środowiskiem gospodarza, a nie tylko z prostej konkurencji mikroba z mikroblem.
Co to oznacza dla ochrony ludzi
Dla osób niebędących specjalistami główny przekaz jest taki, że nie wszystkie zdrowo wyglądające mikrobioty chronią przed infekcją w ten sam sposób i że „większa różnorodność” nie zawsze oznacza lepszą ochronę w każdej chwili. Uproszczona społeczność Oligo-MM12 zapewniła silną wczesną oporność na Listerię w jelicie, ale z upływem czasu bardziej złożony mikrobiom SPF lepiej radził sobie z usuwaniem intruza. Praca pokazuje, że starannie zaprojektowane, niskozłożone modele mikrobioty, połączone z kontrolowalnymi systemami ex vivo, mogą ujawnić, które grupy bakterii i czynniki środowiskowe są kluczowe dla blokowania groźnych patogenów przenoszonych przez żywność. Ostatecznie takie wnioski mogą pokierować opracowaniem ukierunkowanych probiotyków lub terapii opartych na mikrobiomie, które wzmocnią właściwych mikrobiologicznych sojuszników we właściwym czasie, aby zapobiegać poważnym zakażeniom Listerią u pacjentów z grup ryzyka.
Cytowanie: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Słowa kluczowe: Infekcja Listerią, mikrobiom jelitowy, oporność na kolonizację, model myszy, probiotyki