Clear Sky Science · pl
Zintegrowana analiza regulatorów globalnych i genów efflux związanych z odwróceniem oporności na antybiotyki w wielolekoopornej Klebsiella pneumoniae
Dlaczego te szpitalne zarazki są tak trudne do zabicia
W szpitalach na całym świecie niektóre szczepy bakterii Klebsiella pneumoniae stały się niezwykle trudne do leczenia. Odpierają działanie wielu antybiotyków, które kiedyś działały niezawodnie, zamieniając rutynowe infekcje w zagrażające życiu przypadki. To badanie zagląda pod mikroskopową osłonę tych mikroorganizmów, by zrozumieć jedną z ważnych sztuczek, której używają: mikroskopijne pompy, które wyrzucają antybiotyki z powrotem na zewnątrz komórki, oraz genetyczne przełączniki, które wydają się regulować aktywność tych pomp.
Superbakterie i ich molekularne wyjścia awaryjne
Wielolekooporna Klebsiella pneumoniae jest dziś spotykana w wielu szpitalach, w tym w irackim ośrodku medycznym, gdzie przeprowadzono to badanie. Te bakterie potrafią przetrwać działanie kilku ważnych rodzin antybiotyków jednocześnie, takich jak fluorochinolony, aminoglikozydy i cefalosporyny trzeciej generacji. Jednym ze sposobów, w jaki to czynią, jest osadzenie w swojej otoczce komórkowej silnych „pomp efflux”. Jednym z najważniejszych systemów jest AcrAB‑TolC, który przechodzi przez błony bakteryjne i działa jak maleńka pompa, chwytająca cząsteczki antybiotyku wewnątrz komórki i wypychająca je na zewnątrz, zanim leki zdążą wyrządzić poważne szkody. Gdy te pompy są bardzo aktywne, stężenie antybiotyku wewnątrz bakterii nigdy nie rośnie do poziomu zabójczego.
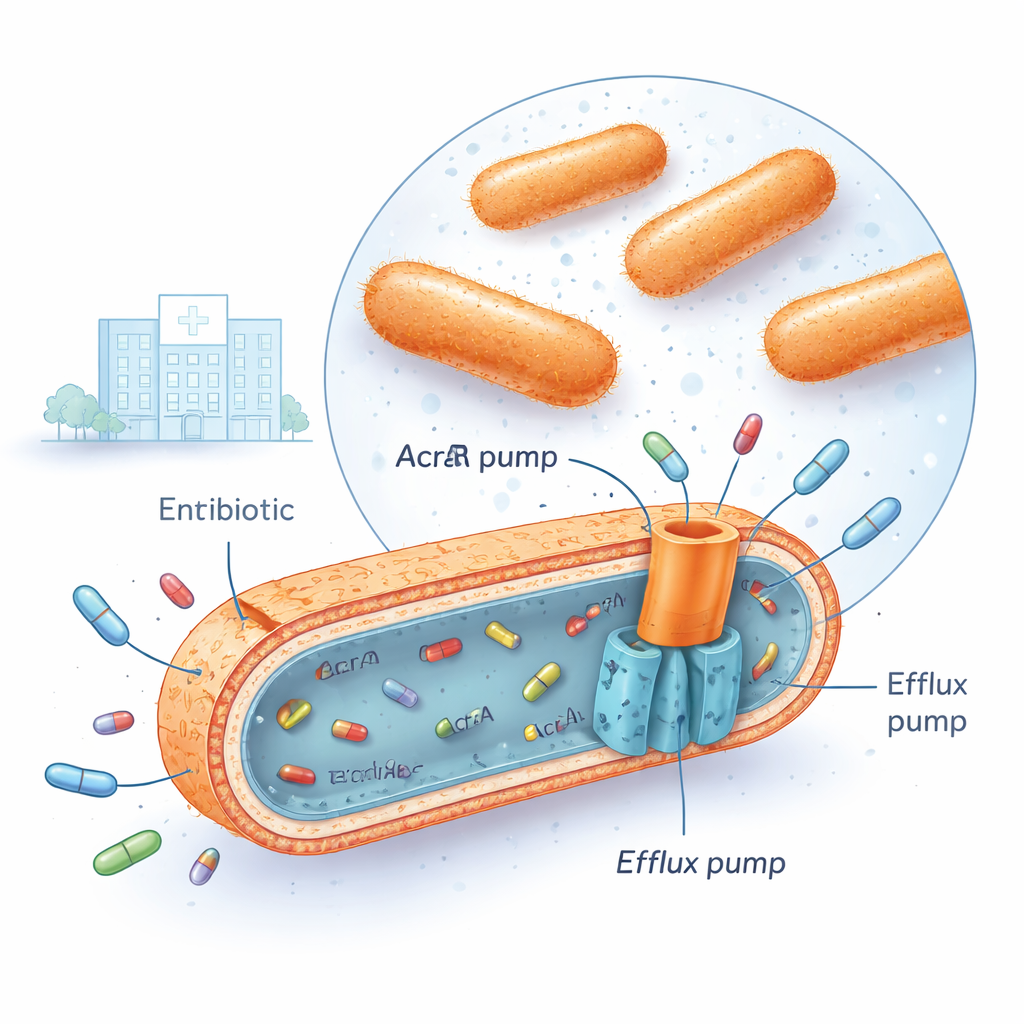
Przełączniki genowe towarzyszące nadmiernej pracy pomp
Naukowcy zebrali 30 klinicznych izolatów wielolekoopornej Klebsiella pneumoniae i porównali je z 10 izolatami wrażliwymi na antybiotyki oraz ze standardowym szczepem referencyjnym. Za pomocą techniki zwanej ilościowym PCR w czasie rzeczywistym zmierzyli, jak bardzo pewne geny są włączone. Skoncentrowali się na trzech „regulatorach globalnych” — genach nazwanych marA, soxS i rob — oraz na trzech częściach pompy AcrAB‑TolC (acrA, acrB i tolC). W szczepach opornych dwa regulatory, marA i soxS, były zwykle podwyższone około czterokrotnie do pięciokrotnie w porównaniu z bakteriami wrażliwymi, podczas gdy acrB, kluczowy składnik pompy, był zwiększony niemal ośmiokrotnie. Analiza statystyczna wykazała, że gdy poziomy marA i soxS były wysokie, poziomy acrB zwykle też były wysokie, a te szczepy wytrzymywały znacznie wyższe dawki fluorochinolonów, takich jak cyprofloksacyna. Trzeci regulator, rob, zmieniał się niewiele i nie korelował z aktywnością pompy, co sugeruje, że odgrywa mniejszą rolę w badanych warunkach.
Wyłączanie pomp, by osłabić oporność
Stwierdzenie, że geny pomp i regulatorów są aktywne równocześnie, jest sugestywne, ale samo w sobie nie dowodzi, że faktycznie napędzają oporność. Aby sprawdzić, czy pompy są funkcjonalnie istotne, zespół użył narzędzia chemicznego nazwanego PAβN. Związek ten nie jest stosowany jako lek u pacjentów, lecz w laboratorium może zablokować pompy podobne do AcrAB‑TolC i powstrzymać ich wypompowywanie antybiotyków. Naukowcy wybrali dziesięć opornych izolatów, które miały szczególnie wysokie poziomy genu acrB, i zmierzyli, jaka ilość cyprofloksacyny jest potrzebna, by zatrzymać ich wzrost, z PAβN i bez niego. W ośmiu z tych dziesięciu szczepów zablokowanie pompy obniżyło wymaganą dawkę cyprofloksacyny co najmniej czterokrotnie, a czasem nawet szesnastokrotnie. Ten spadek pokazuje, że w wielu z tych superbakterii aktywne pompy efflux rzeczywiście stanowią główny powód, dla którego tolerują wysokie dawki antybiotyków.
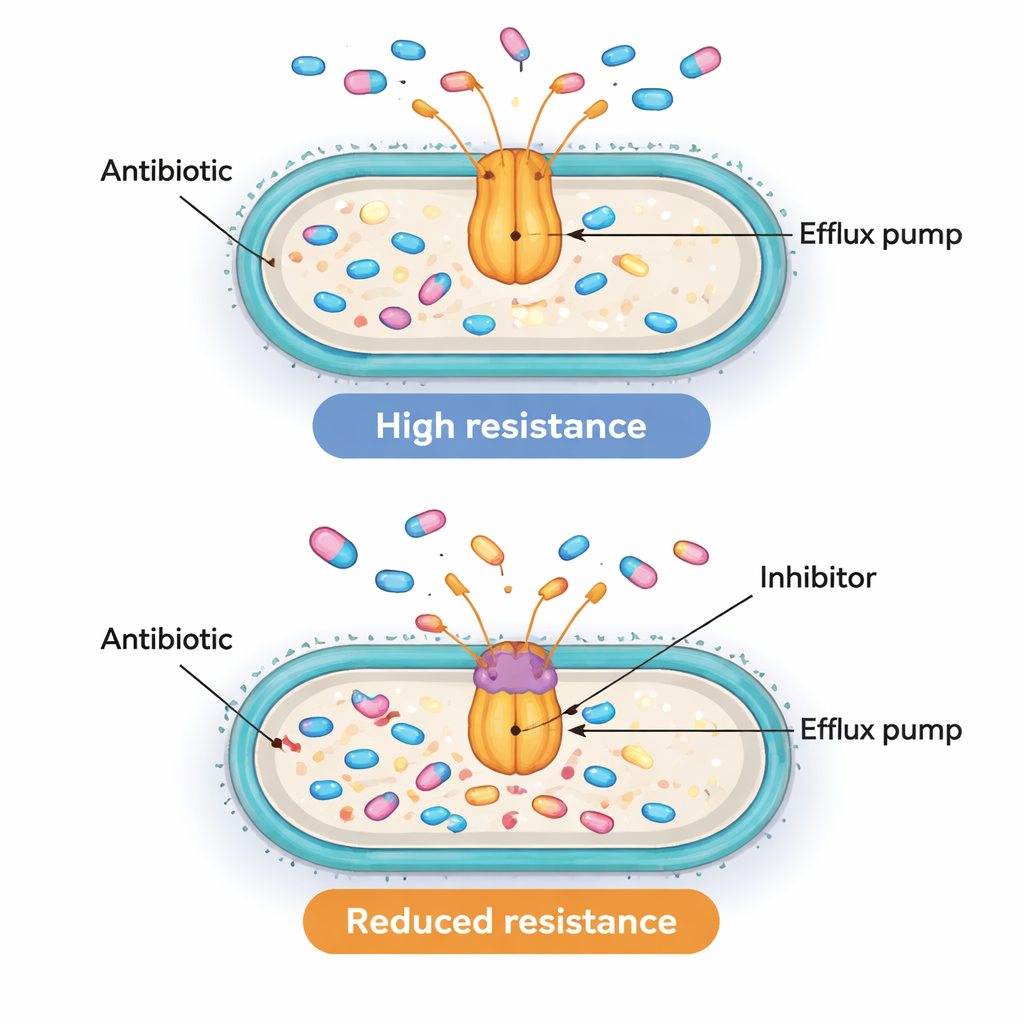
Złożona układanka oporności z obiecującymi celami
Nie każdy szczep zachowywał się tak samo. Niektóre bakterie z silnie ekspresjonowanymi genami pomp odzyskały wrażliwość jedynie częściowo po zablokowaniu pomp, co sugeruje, że inne drogi oporności — takie jak zmiany miejsca działania antybiotyku wewnątrz komórki, produkcja enzymów rozkładających lek czy alternatywne pompy — również mają znaczenie. Na przykład gentamycyna, aminoglikozyd, pozostawała w dużej mierze niezmieniona względem wzorców obserwowanych dla genów marA/soxS i AcrAB‑TolC, podkreślając, że wielolekooporność zwykle powstaje z kilku nakładających się mechanizmów, a nie jednego czynnika.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że niektóre szpitalne bakterie potrafią przetrwać antybiotyki nie tylko przez ich blokowanie czy rozkładanie, lecz także przez aktywne ich wyrzucanie. To badanie łączy zwiększoną aktywność dwóch genowych „przełączników”, MarA i SoxS, z bardziej aktywnymi pompami efflux i silniejszą opornością na powszechnie stosowaną klasę antybiotyków. Gdy pompy są eksperymentalnie zablokowane, wiele z tych bakterii staje się przynajmniej częściowo wrażliwych ponownie. Choć praca nie dowodzi jeszcze dokładnie, jak te przełączniki kontrolują pompy, wskazuje zarówno regulatory, jak i pompy jako atrakcyjne cele. W dłuższej perspektywie łączenie konwencjonalnych antybiotyków z bezpiecznymi blokatorami pomp — lub lekami obniżającymi aktywność tych regulatorów globalnych — mogłoby pomóc przywrócić skuteczność istniejących terapii przeciw groźnym infekcjom wielolekoopornym.
Cytowanie: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Słowa kluczowe: oporność na antybiotyki, pompy efflux, Klebsiella pneumoniae, fluorochinolony, odwrócenie oporności