Clear Sky Science · pl
Obniżenie poziomu enzymu deubikwitynującego USP10 koreluje z apoptozą neuronów w mielopatii związanej z HTLV-1
Dlaczego to ma znaczenie dla osób żyjących z wirusowymi chorobami nerwów
Niektóre wirusy nie wywołują jedynie krótkotrwałych infekcji; cicho uszkadzają układ nerwowy przez wiele lat. Wirus ludzkiej białaczki limfocytów T typu 1 (HTLV-1) jest jednym z nich i może prowadzić do przewlekłego schorzenia rdzenia kręgowego zwanego mielopatią związaną z HTLV-1 (HAM). Osoby z HAM stopniowo tracą siłę i kontrolę nad nogami oraz mają problemy z pęcherzem i czuciem. Badanie stawia proste, lecz kluczowe pytanie: dlaczego komórki nerwowe w rdzeniu kręgowym obumierają w tym schorzeniu i czy pojedyncza cząsteczka ochronna może wyjaśnić, kto ma lepsze, a kto gorsze rokowania?
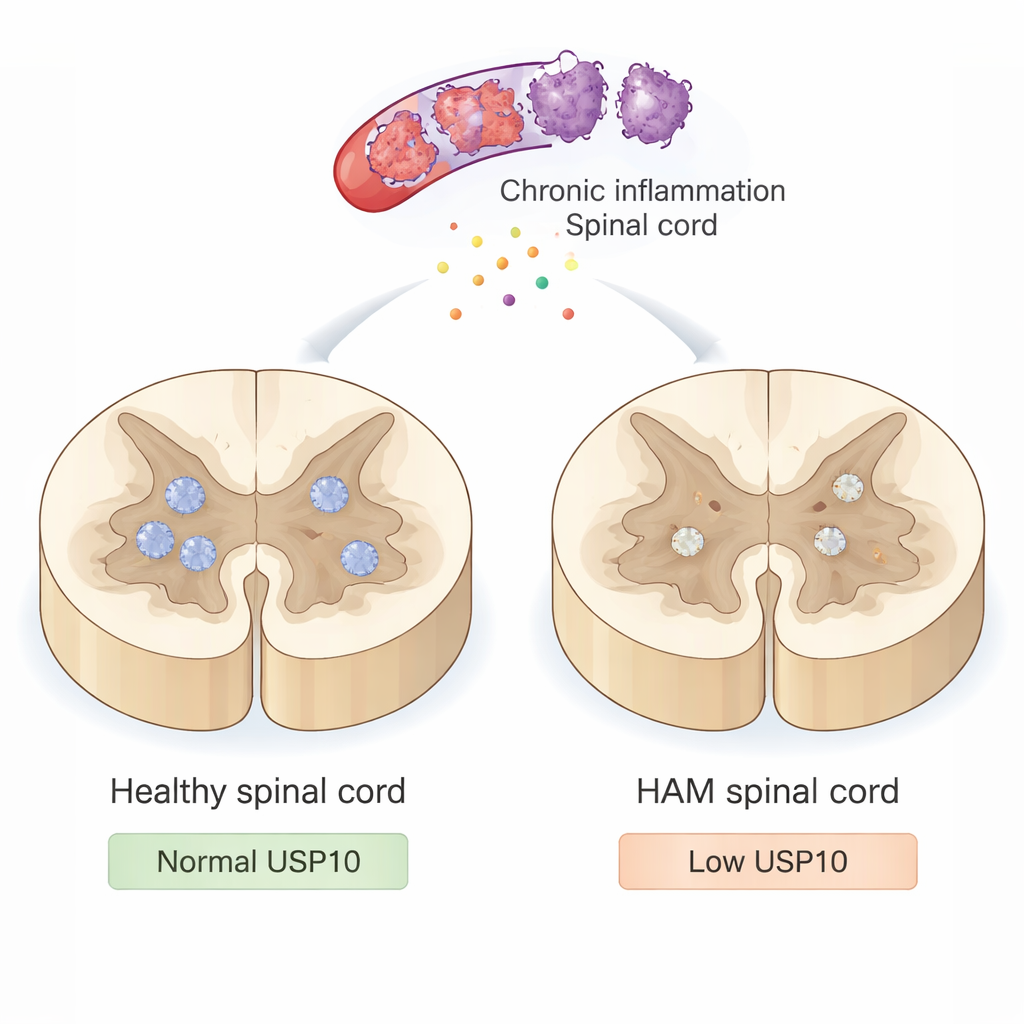
Powolny atak na rdzeń kręgowy
HAM nie jest spowodowana bezpośrednim zakażeniem komórek nerwowych przez wirusa. Zamiast tego HTLV-1 zakaża komórki układu odpornościowego, które wnikają do rdzenia kręgowego i wywołują długotrwałe zapalenie. Te nadaktywne komórki odpornościowe uwalniają toksyczne substancje i sygnały zapalne, które, choć mają na celu kontrolę infekcji, również uszkadzają pobliskie neurony i ich osłonkę mielinową. Z upływem czasu to tli się atak prowadzi do sztywnienia, osłabienia nóg i trudności w chodzeniu. Mimo to lekarze wciąż nie rozumieją w pełni, dlaczego niektóre neurony ulegają temu zapalnemu środowisku, podczas gdy inne przetrwają przez dziesięciolecia.
Pod lupą enzym „sprzątający” w komórce
Naukowcy skupili się na białku zwanym USP10, enzymie uczestniczącym w systemie kontroli jakości białek w komórce i znanym z ograniczania stresu komórkowego oraz programowanej śmierci komórek (apoptozy). USP10 jest aktywny w wielu tkankach, w tym w mózgu i rdzeniu kręgowym; wcześniejsze prace w chorobie Parkinsona, udarze i innych schorzeniach sugerują, że pomaga neuronom przetrwać uszkodzenia oksydacyjne i zapalne. Korzystając z próbek rdzenia kręgowego od ośmiu osób, które zmarły z powodu HAM, oraz dwóch neurologicznie zdrowych kontroli, zespół zastosował techniki barwienia, aby zobaczyć, gdzie USP10 występuje i jak silnie jest ekspresjonowany w komórkach nerwowych.
Mniej USP10, więcej obumierających neuronów
W zdrowych rdzeniach kręgowych USP10 był wyraźnie widoczny w wielu neuronach. W większości przypadków HAM jednak barwienie USP10 w neuronach było wyraźnie osłabione, a u jednego pacjenta prawie nieobecne. Naukowcy następnie szukali cech apoptozy dwoma metodami: testem TUNEL wykrywającym pofragmentowane DNA oraz barwieniem aktywnej kaspazy-3, białka zaangażowanego we wczesne etapy śmierci komórki. W kontrolach praktycznie żadne neurony nie wykazywały tych sygnałów śmierci. Dla kontrastu u pacjentów z HAM duża część neuronów była TUNEL-dodatnia i wiele wykazywało aktywną kaspazę-3. Co ważne, próbki z niższą ekspresją USP10 miały tendencję do większej liczby neuronów apoptycznych i mniejszej liczby przeżywających neuronów oznaczonych NeuN, standardowym markerem neuronalnym. Jeden godny uwagi pacjent z HAM, który po 22 latach nadal chodził z laską, miał silną ekspresję USP10 i stosunkowo zachowaną liczbę neuronów, co sugeruje, że wyższy poziom USP10 może chronić przed ciężkimi następstwami choroby.
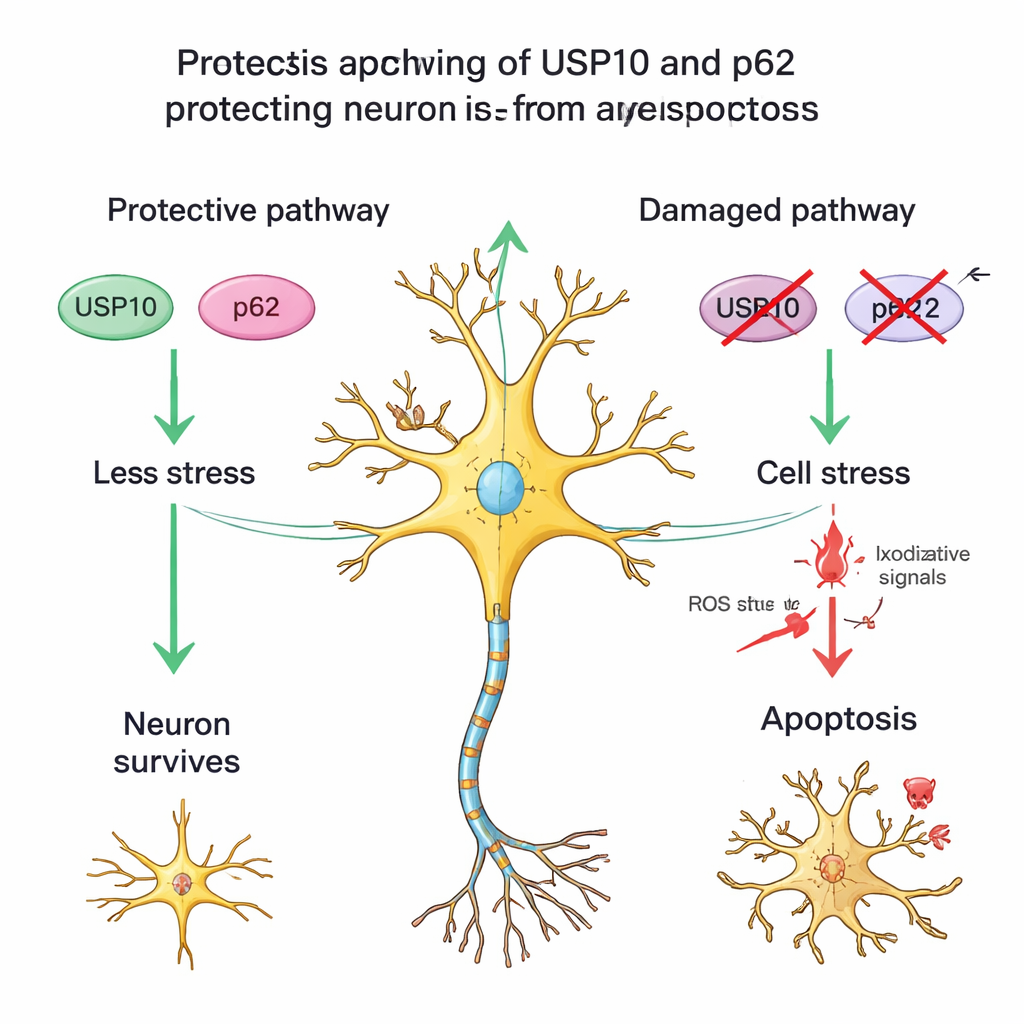
Proteinowy partner i komórki zestresowane, ale żyjące
Zespół zbadał także inne białko, p62, które współdziała z USP10 w obróbce uszkodzonych białek oraz regulacji szlaków stresu i przeżycia. W zdrowych rdzeniach kręgowych barwienie p62 było umiarkowane; wśród pacjentów z HAM ci z niskim USP10 często mieli też słabsze barwienie p62 i mniej przeżywających neuronów. Ten wzorzec wspiera koncepcję partnerstwa USP10–p62, które pomaga neuronom przetrwać przewlekłe zapalenie. Naukowcy zauważyli ponadto wiele neuronów w tkance HAM, które miały typowy kształt komórek nerwowych, ale utraciły barwienie NeuN — cechę obserwowaną przy innych uszkodzeniach mózgu, gdy neurony są poważnie zestresowane, lecz nie całkowicie martwe. Sugeruje to, że w HAM część neuronów ginie bezpowrotnie, podczas gdy inne pozostają w uszkodzonym, podatnym stanie, prawdopodobnie z powodu osłabienia mechanizmów obronnych związanych z USP10.
Co to może znaczyć dla przyszłej diagnostyki i leczenia
To badanie nie dowodzi, że utrata USP10 bezpośrednio powoduje śmierć neuronów, ponieważ opiera się na ograniczonej liczbie próbek sekcyjnych i nie pozwala śledzić zmian w czasie. Mimo to spójne powiązania między niskim USP10, obniżonym p62, większą liczbą oznak apoptozy i mniejszą liczbą przeżywających neuronów wskazują na wspólną ścieżkę mogącą łączyć przewlekłe zapalenie z powolną degeneracją neuronów w HAM. Dla pacjentów pojawia się zachęcająca możliwość: pomiar lub wzmocnienie szlaków związanych z USP10 w rdzeniu kręgowym — albo potencjalnie w łatwiej dostępnych materiałach, takich jak płyn mózgowo-rdzeniowy — mogłoby w przyszłości pomóc zidentyfikować osoby o wyższym ryzyku szybkiego pogorszenia, ukierunkować monitoring lub zainspirować nowe terapie wzmacniające naturalne mechanizmy ochrony komórkowej w wirusowo wywołanych chorobach neurozapalnych.
Cytowanie: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Słowa kluczowe: mielopatia związana z HTLV-1, neurozapalenie, apoptoza neuronów, USP10, degeneracja rdzenia kręgowego