Clear Sky Science · pl
Aktywność antybakteryjna i cytotoksyczność cementów na bazie trójwapniowego krzemianu z różnymi dodatkami antybakteryjnymi
Dlaczego to ma znaczenie przy następnym wypełnieniu
Gdy masz głęboki ubytek, stomatolodzy coraz częściej starają się oszczędzić jak najwięcej naturalnej tkanki zęba zamiast wszystko frezować. Często oznacza to pozostawienie cienkiej warstwy zmiękczonego, zawierającego bakterie zębiny pod wypełnieniem. W tym badaniu postawiono proste, ale kluczowe pytanie: czy można ulepszyć szeroko stosowany cement do naprawy zębów tak, by dyskretnie zabijał pozostałe drobnoustroje, nie szkodząc komórkom żyjącym wewnątrz zęba?
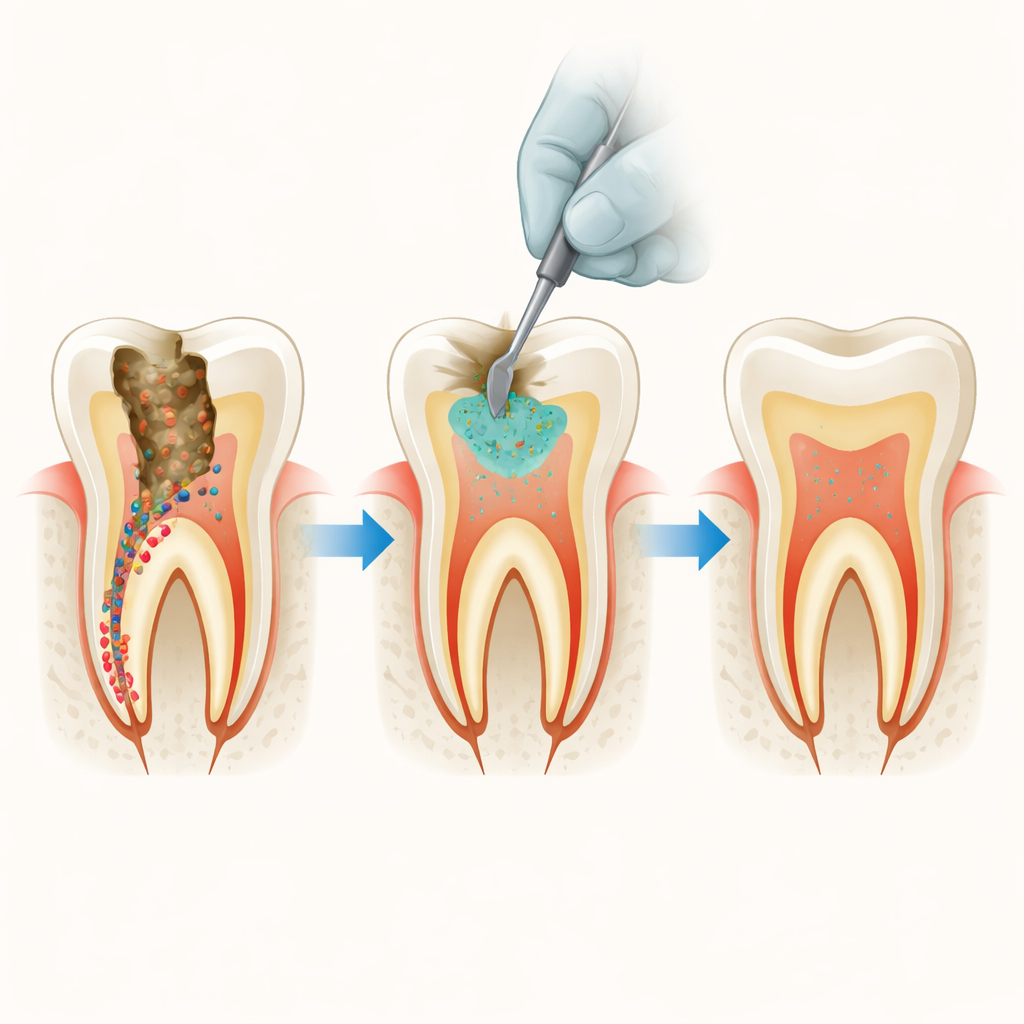
Głębokie ubytki i ukryte drobnoustroje
Nowoczesne techniki „minimalnego borowania” mają na celu uniknięcie odsłonięcia miękkiego rdzenia zęba, czyli miazgi, poprzez pozostawienie zębiny, która może się ponownie zmineralizować. Wadą jest to, że w tej warstwie mogą przetrwać bakterie wywołujące próchnicę, takie jak Streptococcus mutans czy gatunki Lactobacillus. Z czasem te mikroby mogą wywołać ponowną próchnicę pod pozornie zdrowym wypełnieniem. Cementy na bazie trójwapniowego krzemianu są popularne do uszczelniania głębokich ubytków, ponieważ sprzyjają odtwarzaniu minerałów i tworzą szczelną barierę, jednak same w sobie nie są zbyt skuteczne w zatrzymywaniu bakterii.
Przekształcanie powszechnego cementu w środek przeciw drobnoustrojom
Naukowcy wzbogacili ten znany cement o pięć różnych dodatków antybakteryjnych w różnych stężeniach. Dwa z nich to związki organiczne często występujące w środkach dezynfekcyjnych (chlorek benzalkoniowy i cetrimid), a trzy to substancje nieorganiczne stosowane w produktach stomatologicznych lub materiałach (tlenek tytanu, tlenek cynku i fluorek cyny). Wytłoczyli te mieszaniny w małe dyski i umieścili je na płytkach pokrytych pięcioma rodzajami bakterii związanych z próchnicą i zakażeniami jamy ustnej. Mierząc przejrzyste strefy wokół każdego dysku, gdzie bakterie nie rosły, określali, jak silnie każda receptura hamowała rozwój drobnoustrojów.
Znajdowanie najlepszego kompromisu między zabijaniem bakterii a oszczędzaniem komórek
Ponieważ materiał, który zabija bakterie, ale jednocześnie zatruwa komórki zęba, byłby bezużyteczny w jamie ustnej, zespół badał także, jak najbardziej obiecujące dodatki wpływają na komórki żywe. Poddali badaniu pośrednio dwa typy ludzkich komórek — fibroblasty, będące powszechnymi komórkami podporowymi, oraz mezenchymalne komórki macierzyste miazgi zęba, które pomagają naprawiać tkankę zębową. Test zmiany koloru mierzył, ile komórek pozostało czynnych, a specjalne barwniki fluorescencyjne pokazywały żywe (zielone) i martwe (czerwone) komórki pod mikroskopem. Układ ten odwzorowywał rzeczywistą sytuację w głębokim ubytku, gdzie cement oddzielony jest od miazgi cienką warstwą zębiny i uwalnia substancje, które dyfundują w kierunku komórek.
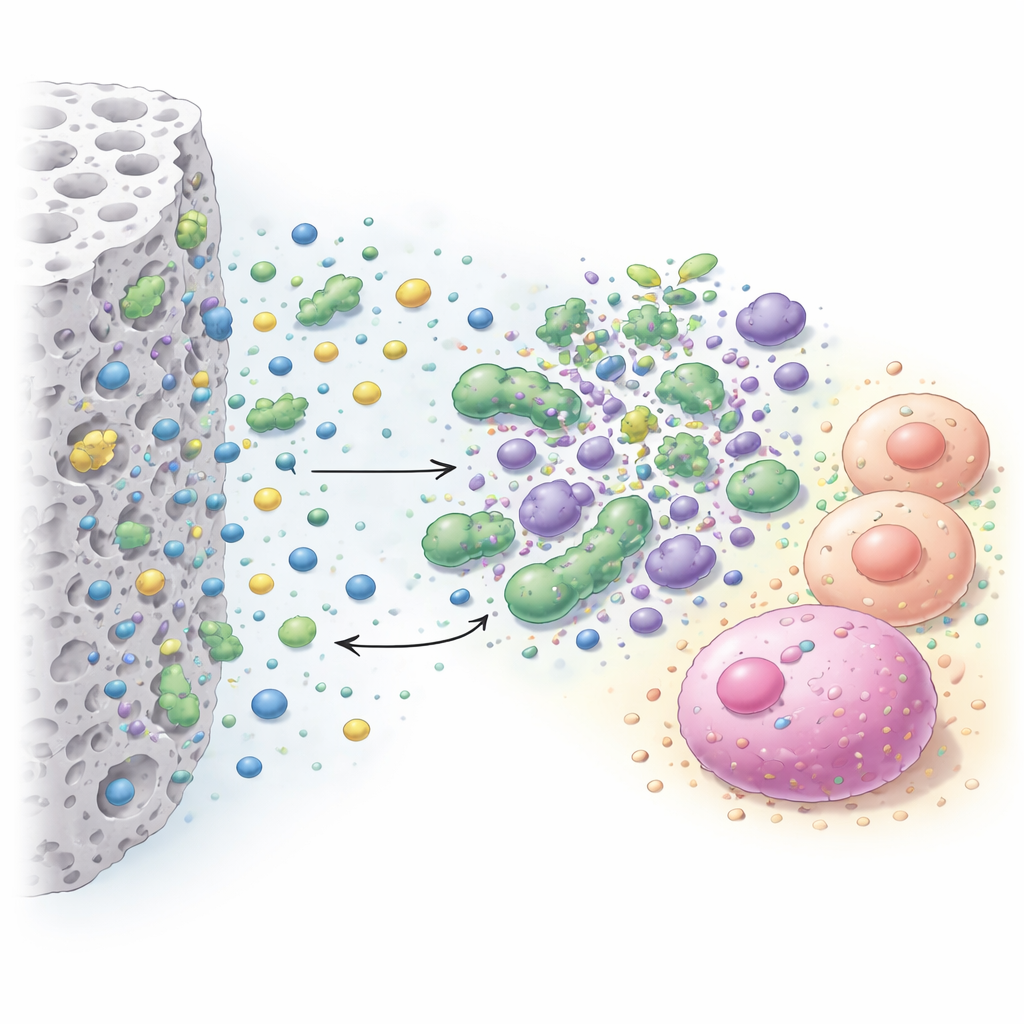
Co zadziałało najlepiej, a co było zbyt agresywne
Wyniki wykazały, że rodzaj i ilość dodatku miały kluczowe znaczenie. Chlorek benzalkoniowy dał najsilniejszy i najszerszy efekt antybakteryjny, tworząc duże strefy bez drobnoustrojów przeciwko wszystkim testowanym gatunkom, szczególnie wobec szczepów Lactobacillus często występujących w głębokiej próchnicy. Cetrimid także pomagał, lecz zwykle wymagał wyższych stężeń, aby dorównać chlorkowi benzalkoniowemu. Trzy nieorganiczne środki poprawiały działanie antybakteryjne cementu tylko przy wyższych dawkach i nawet wtedy głównie wobec określonych bakterii, takich jak S. mutans i Actinomyces. Pod względem bezpieczeństwa sam cement bazowy był łagodny dla obu typów komórek i wydawał się nawet wspierać zdrowie fibroblastów. Dodanie chlorku benzalkoniowego pozostawało nieszkodliwe dla fibroblastów do około 1%, stawało się nieco szkodliwe przy 2–4% i wyraźnie bardziej toksyczne przy 7%. Komórki macierzyste miazgi były ogólnie bardziej wrażliwe: zarówno chlorek benzalkoniowy, jak i cetrimid obniżały ich przeżywalność, przy czym cetrimid stawał się umiarkowanie toksyczny od 2% wzwyż.
Co to może znaczyć dla przyszłej opieki stomatologicznej
Sumując te ustalenia, badanie wskazuje na jedną szczególnie obiecującą recepturę: cement na bazie trójwapniowego krzemianu zawierający 1% chlorku benzalkoniowego. Przy tym stężeniu materiał silnie tłumił szkodliwe bakterie, jednocześnie utrzymując fibroblasty w pełni żywe, a komórki macierzyste miazgi w dużej mierze w stanie żywotnym. W praktycznym ujęciu sugeruje to, że przyszłe głębokie wypełnienia mogłyby być wykonane z cementu, który dyskretnie zwalcza pozostałe drobnoustroje pod powierzchnią, a jednocześnie jest wystarczająco łagodny dla żywej tkanki wewnątrz zęba. Potrzebne są dalsze badania — zwłaszcza w złożonych, rzeczywistych warunkach jamy ustnej — ale ta zrównoważona formuła mogłaby pomóc stomatologom lepiej chronić zęby leczone technikami minimalnie inwazyjnymi.
Cytowanie: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Słowa kluczowe: głębokie ubytki próchnicowe, antybakteryjny cement stomatologiczny, trójwapniowy krzemian, chlorek benzalkoniowy, biokompatybilność komórek miazgi