Clear Sky Science · pl
Wzmacniane kontrastowo obrazowanie MRI T1, PET 11C-DPA-713 i PET 11C-CPPC jako prognostyczne biomarkery obrazowe neurozapalenia w uszkodzeniu mózgu wywołanym radioterapią
Dlaczego to badanie ma znaczenie
W miarę poprawy terapii nowotworów mózgu u dzieci i młodych dorosłych coraz więcej pacjentów przeżywa długie lata po leczeniu. Niestety radioterapia mózgu może pozostawić trwały ślad, uszkadzając naczynia krwionośne i komórki mózgowe, co prowadzi do zaburzeń pamięci, uwagi i funkcji poznawczych. Lekarze potrzebują bezpiecznych, nieinwazyjnych metod wczesnego wykrywania tych ukrytych uszkodzeń, na długo zanim stan pacjenta jawnie wpłynie na codzienne życie. W tym badaniu sprawdzono, czy powszechnie stosowane badanie szpitalne — MRI T1 wzmacniane kontrastowo — może śledzić szkodliwe zapalenie mózgu z porównywalną wiarygodnością co specjalistyczne badania PET, które wiążą się z dodatkową ekspozycją na promieniowanie.
Ukryte uszkodzenia po ratującym życie leczeniu
Uszkodzenie mózgu wywołane radioterapią rozwija się powoli w ciągu miesięcy lub lat po napromieniowaniu. Proces ten jest częściowo napędzany przez neurozapalenie: własne komórki odpornościowe mózgu stają się nadaktywne, naczynia krwionośne ulegają uszkodzeniu, a bariera krew–mózg — zazwyczaj ścisły filtr — zaczyna przeciekać. To przeciekanie pozwala większej liczbie komórek odpornościowych z krwi przedostać się do mózgu, podtrzymując cykl, który ostatecznie może prowadzić do śmierci neuronów i upośledzenia funkcji poznawczych. Obecnie lekarze zwykle rozpoznają to uszkodzenie dopiero wtedy, gdy pacjenci wykazują problemy z nauką lub pamięcią w testach neuropsychologicznych. Autorzy postawili sobie za cel znalezienie obrazowych „wczesnych sygnałów ostrzegawczych”, które ujawniłyby ten proces znacznie wcześniej.
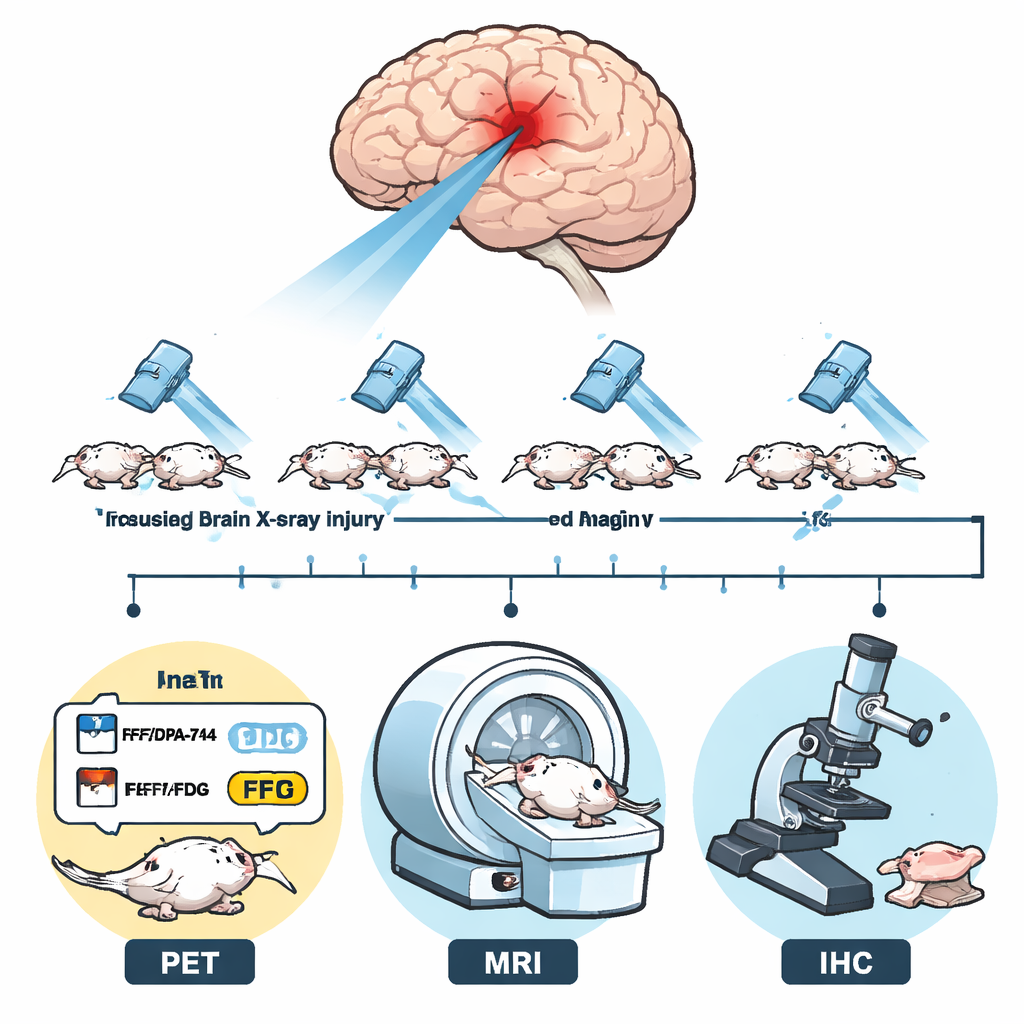
Porównanie trzech sposobów obserwacji zapalenia mózgu
Aby rozwiązać to zagadnienie, badacze użyli modelu mysiego, który naśladuje skoncentrowane napromieniowanie niewielkiego obszaru mózgu, porównywalne z tym, które otrzymują niektórzy pacjenci w wieku nastoletnim. Po napromieniowaniu cztery grupy myszy obserwowano przez dziewięć miesięcy. Jedna grupa była skanowana za pomocą znacznika PET 11C-DPA-713, który wiąże się z białkiem (TSPO) wzrastającym przy aktywacji wielu komórek odpornościowych mózgu. Druga grupa otrzymała inny znacznik PET, 11C-CPPC, który celuje w receptor występujący specyficznie na mikrogleju — rezydentnych komórkach odpornościowych mózgu. Trzecia grupa przeszła standardowe MRI T1 wzmacniane kontrastowo, które uwypukla miejsca, gdzie bariera krew–mózg stała się przeciekająca. Ostatnia grupa nie była poddana obrazowaniu, a zamiast tego ich tkanka mózgowa była badana pod mikroskopem po barwieniu fluorescencyjnym w kierunku markerów aktywowanego mikrogleju i napływających komórek odpornościowych.
Co PET i MRI ujawniły w czasie
Zespół stwierdził, że oba znaczniki PET najsilniej uwidaczniały napromieniowaną stronę mózgu około miesiąca po radioterapii, a następnie stopniowo słabły przez kolejne miesiące. Ten wzorzec odpowiadał spodziewanemu napływowi neurozapalenia, które potem powoli ustępuje, choć nie znika całkowicie. Co istotne, sygnał z MRI wzmacnianego kontrastowo — odzwierciedlający stopień przeciekania bariery krew–mózg — wykazywał bardzo podobny przebieg czasowy. Napromieniowana półkula wykazywała dramatycznie większe wychwyty kontrastu niż strona nieleczona, z maksimum w okolicach jednego miesiąca, po czym sygnał spadał, ale pozostawał podwyższony nawet po dziewięciu miesiącach. Gdy badacze ilościowo ocenili te zmiany, pomiary MRI ściśle odpowiadały sygnałom PET, wykazując silne korelacje statystyczne.
Dowody mikroskopowe potwierdzają obrazowanie
Aby potwierdzić, że zmiany obrazowe rzeczywiście odzwierciedlają stan zapalny, naukowcy zbadali plastry mózgu zabarwione na kilka markerów immunologicznych. Miesiąc po radioterapii napromieniowana półkula wykazywała skok aktywowanego mikrogleju i napływających makrofagów, wraz z bardzo wysokim poziomem białka TSPO. Te mikroskopowe sygnały zmniejszały się z czasem równolegle do obserwacji PET i MRI. Porównując bezpośrednio liczby, autorzy stwierdzili, że zarówno markery PET, jak i sygnał kontrastu w MRI były ściśle powiązane z ilością TSPO i aktywacji mikrogleju widzianą pod mikroskopem. Sugeruje to, że przeciekająca bariera krew–mózg i neurozapalenie są ściśle związane w tej formie uszkodzenia po radioterapii.
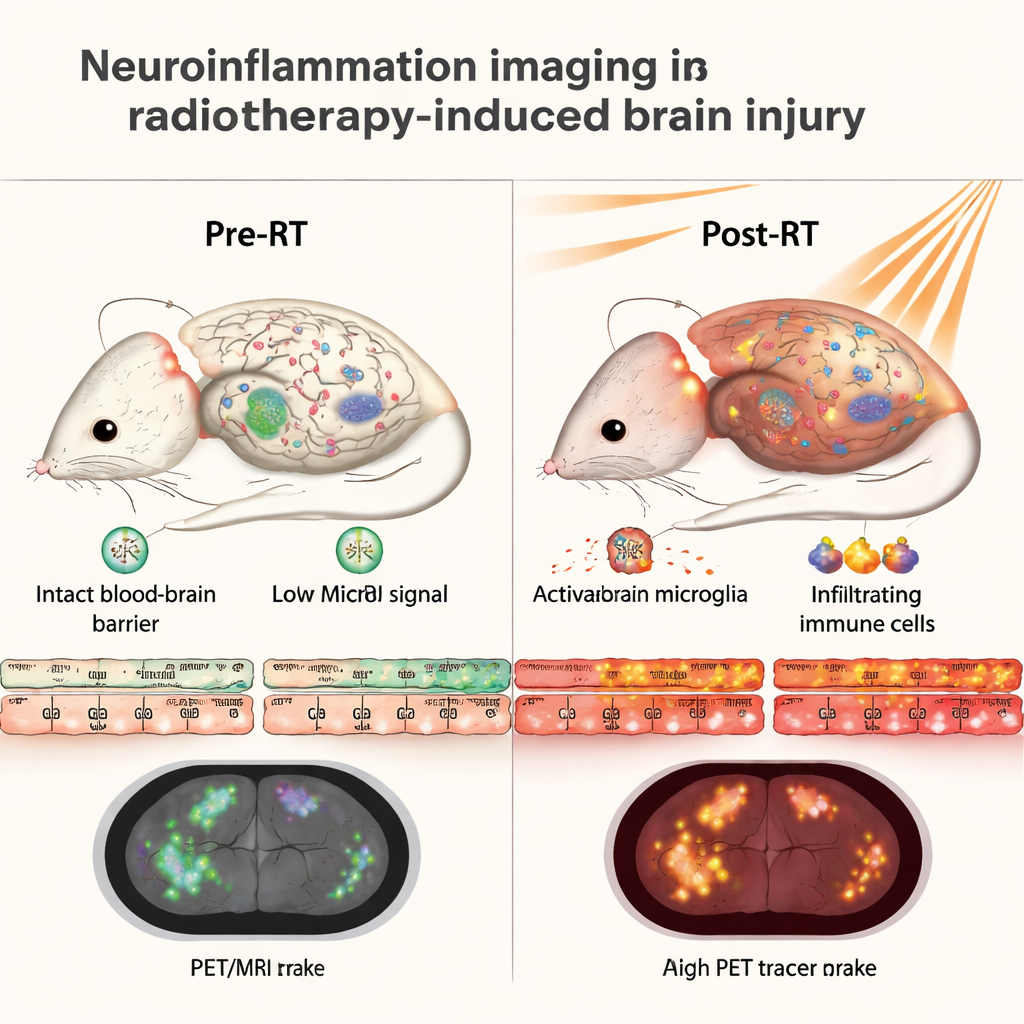
Co to może znaczyć dla pacjentów
Badanie pokazuje, że szeroko dostępna technika kliniczna — MRI T1 wzmacniane kontrastowo — może służyć jako silny pośredni wskaźnik neurozapalenia w mózgu uszkodzonym radioterapią, działając prawie tak dobrze jak specjalistyczne badania PET w tym modelu myszy. Chociaż MRI nie oznacza specyficznych typów komórek tak, jak robią to znaczniki PET, unika dodatkowej ekspozycji na promieniowanie, co czyni tę metodę szczególnie atrakcyjną dla dzieci i młodych dorosłych, którzy już otrzymali wysokie dawki do mózgu. Stosowane rozważnie, MRI z kontrastem mogłoby pomóc klinicystom monitorować stan zdrowia mózgu u osób, które przeżyły chorobę, i oceniać nowe terapie mające na celu ochronę lub naprawę napromienionego mózgu, oferując bezpieczniejsze spojrzenie na proces, który od dawna był trudny do zaobserwowania.
Cytowanie: Maiti, S., Yadav, S.K., Teitz, M. et al. Contrast-enhanced T1-weighted MRI, 11C-DPA-713 PET and 11C-CPPC PET as predictive imaging biomarkers of neuroinflammation in radiotherapy-induced brain injury. Sci Rep 16, 6384 (2026). https://doi.org/10.1038/s41598-026-37264-w
Słowa kluczowe: uszkodzenie mózgu wywołane radioterapią, neurozapalenie, MRI wzmacniane kontrastowo, obrazowanie PET, bariera krew–mózg