Clear Sky Science · pl
Znaczenie kliniczne zaburzeń miedzi, selenu i kadmu w tkankach raka jelita grubego
Dlaczego drobne metale w naszych jelitach mają znaczenie
Rak jelita grubego jest jednym z najczęstszych i najgroźniejszych nowotworów na świecie, a mimo to wciąż w dużej mierze opieramy się na inwazyjnych badaniach, takich jak kolonoskopia, by go wykrywać i monitorować. To badanie koncentruje się na czymś znacznie mniej oczywistym, lecz potencjalnie istotnym: układzie drobnych metali i minerałów w obrębie guzów jelita w porównaniu z przylegającą zdrową tkanką. Analizując, jak zmieniają się stężenia pierwiastków takich jak miedź, selen i kadm w okrężnicy, autorzy badają, czy te ukryte chemiczne odciski palców mogą pomóc lepiej zrozumieć, klasyfikować, a w przyszłości diagnozować raka jelita grubego.
Ukryta chemia wewnątrz guzów jelita
Nasz organizm zależy od pierwiastków śladowych — metali i minerałów potrzebnych w bardzo małych ilościach — do kluczowych zadań, takich jak kontrola uszkodzeń oksydacyjnych, utrzymanie integralności DNA i funkcjonowanie enzymów. Gdy ich poziomy wymykają się równowadze, mogą sprzyjać chorobie. Zespół badał tkanki od 62 pacjentów z rakiem jelita grubego, zawsze pobierając parę próbek: jedną z guza i jedną z sąsiadującej, wyglądającej na zdrową tkanki jelita. Wykorzystując wysoce czułą technikę wykrywającą metale na ekstremalnie niskich poziomach, zmierzono dziesięć pierwiastków, w tym miedź (Cu), mangan (Mn), cynk (Zn), selen (Se) i kadm (Cd). Następnie użyto klasycznych metod statystycznych oraz narzędzi uczenia maszynowego, aby sprawdzić, które wzorce korelują z zaawansowaniem choroby i podstawowymi cechami pacjentów, takimi jak płeć czy miejsce zamieszkania.
Stały sygnał miedzi i zmieniające się mechanizmy obronne
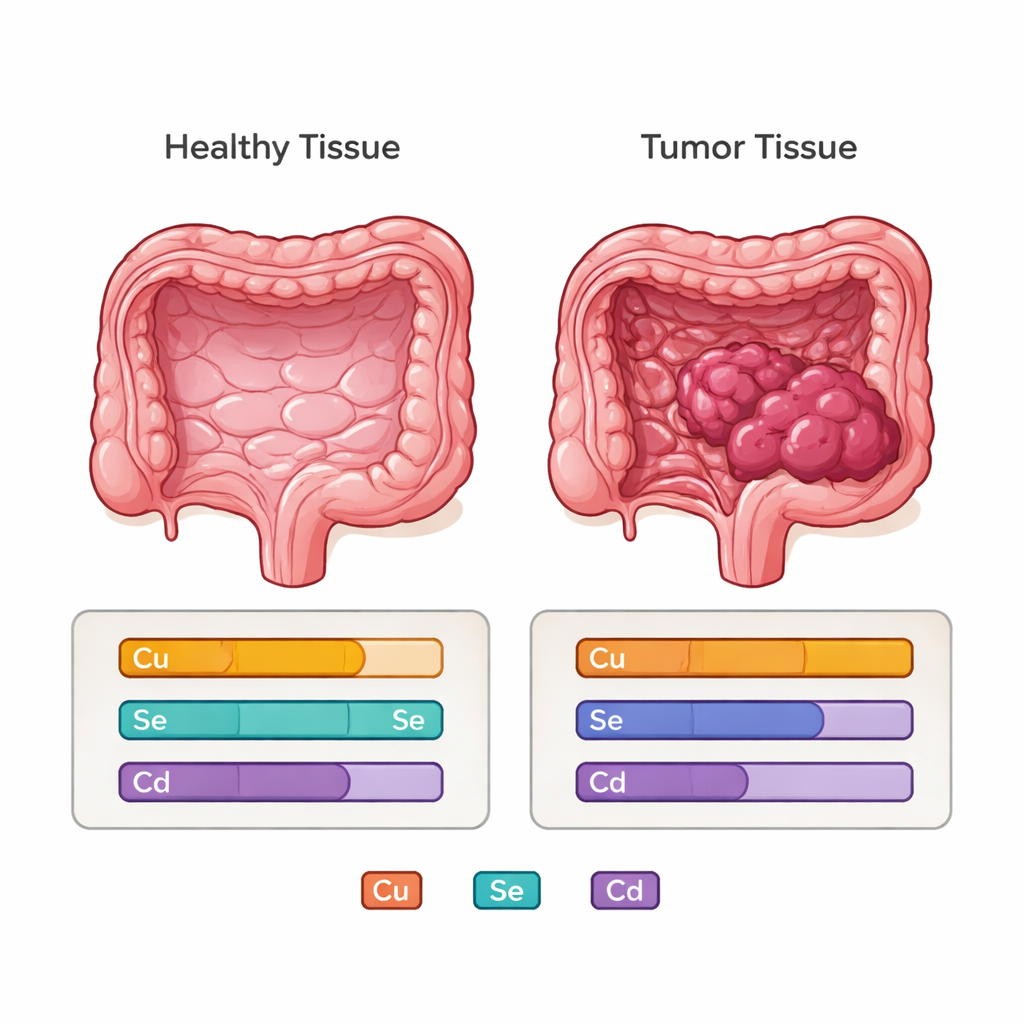
Porównanie tkanki guzowej z zdrową ujawniło wyraźne przesunięcie chemiczne. Guzy generalnie zawierały więcej miedzi i manganu oraz mniej selenu i kadmu niż otaczająca je tkanka. Rozkładając dane według stadium choroby, ukazał się dynamiczny obraz: we wczesnych stadiach kilka ochronnych pierwiastków, takich jak selen, cynk, stront i kadm, miało tendencję do ubytku w guzach. W stadium 3 wzorzec przesunął się w stronę wyraźnych wzrostów miedzi i manganu w tkance nowotworowej. Pacjenci z zajętymi węzłami chłonnymi oraz osoby w bardziej zaawansowanych kategoriach Tumor Node Metastasis szczególnie często wykazywali wyższe poziomy miedzi i manganu w guzach, przy jednoczesnym obniżeniu selenu w próbce guzowej.
Powiązania z płcią, środowiskiem i relacjami między metalami
Chemia tkanki odzwierciedlała również cechy pacjentów i ich miejsce zamieszkania. Kobiety miały wyższe stężenia kadmu w zdrowej tkance jelita niż mężczyźni, co potwierdza wcześniejsze obserwacje z badań krwi. Osoby mieszkające w dużych miastach miały skłonność do wyższego stężenia selenu w zdrowej tkance niż mieszkańcy wsi, chociaż po rygorystycznej korekcie statystycznej większość różnic zależnych od miejsca była umiarkowana. Gdy zespół spojrzał nie tylko na pojedyncze pierwiastki, ale i na stosunki między nimi, pojawiły się uderzające kontrasty: stosunki miedź–cynk i mangan–cynk były wyraźnie wyższe w guzach, podczas gdy stosunek żelazo–miedź był niższy. Te przesunięcia sugerują, że tkanka nowotworowa sprzyja warunkom promującym stres oksydacyjny, zaburzenia mechanizmów obronnych komórek oraz tworzenie naczyń krwionośnych odżywiających guz.
Pozwalając algorytmom przesiać chemiczne wskazówki
Aby ustalić, które pomiary mają największe znaczenie przy klasyfikowaniu stopnia zaawansowania choroby pacjenta, badacze zastosowali algorytm selekcji cech o nazwie Boruta. Metoda ta wielokrotnie testuje, które zmienne niosą prawdziwą informację wykraczającą poza losowy szum. Jak można było oczekiwać, standardowe wskaźniki medyczne, takie jak status węzłów chłonnych i kategoria zaawansowania, znalazły się wysoko w rankingu. Jednak jedną z chemicznych cech, która powtarzalnie się wyróżniała, było to, czy miedź była zwiększona w guzie w porównaniu z własną zdrową tkanką danego pacjenta. Ten względny wzrost miedzi, a nie jakaś ustalona wartość progowa, okazał się stabilnym markerem powiązanym zarówno z ogólnym stadium klinicznym, jak i klasyfikacją Tumor Node Metastasis, nawet w stosunkowo niewielkiej grupie pacjentów.
Co to oznacza dla pacjentów
Dla czytelników niebędących specjalistami kluczowa wiadomość jest taka, że guzy jelita grubego nie tylko różnią się pod mikroskopem — mają również charakterystyczny metalowy odcisk. W tym badaniu guzy miały tendencję do gromadzenia miedzi i manganu przy jednoczesnej utracie selenu i kadmu w porównaniu z przylegającym zdrowym odcinkiem jelita. Najbardziej wyróżniającym się ustaleniem jest konsekwentny wzrost miedzi w tkance guzowej, który koreluje z zaawansowaniem choroby. Chociaż badanie nie oferuje jeszcze nowego testu przesiewowego, pokazuje, że pomiar pierwiastków śladowych bezpośrednio w tkance i koncentracja na indywidualnych zmianach u pacjenta może pogłębić zrozumienie biologii guza i wspierać odkrywanie przyszłych biomarkerów. W większych badaniach uzupełniających, które jednocześnie będą śledzić dietę i narażenia środowiskowe, te elementarne odciski mogłyby w przyszłości pomóc w dokładniejszej diagnostyce i planowaniu leczenia raka jelita grubego.
Cytowanie: Kiełbus, M., Wojnicka, J., Prystupa, A. et al. Clinical relevance of tissue copper, selenium, and cadmium alterations in colorectal cancer. Sci Rep 16, 6700 (2026). https://doi.org/10.1038/s41598-026-37256-w
Słowa kluczowe: rak jelita grubego, pierwiastki śladowe, miedź, selen, biomarkery