Clear Sky Science · pl
Obrazowanie międzykomórkowych biomolekuł za pomocą wskaźników białek fluorescencyjnych z kotwicami lipid–PEG
Obserwowanie, jak komórki rozmawiają w czasie rzeczywistym
Nasze mózgi i organizmy opierają się na stałej chemicznej rozmowie między komórkami. Jony i neuroprzekaźniki przesyłają komunikaty przez maleńkie szczeliny, ale te szybkie, ulotne sygnały są trudne do zaobserwowania bez ich zakłócania. W tym badaniu przedstawiono prosty sposób „malowania” żywych komórek świecącymi czujnikami, które przyczepiają się do ich zewnętrznej powierzchni, co pozwala naukowcom oglądać te przekazy — zwłaszcza jony potasu i neuroprzekaźnik glutaminian — na żywo i ze szczegółami. 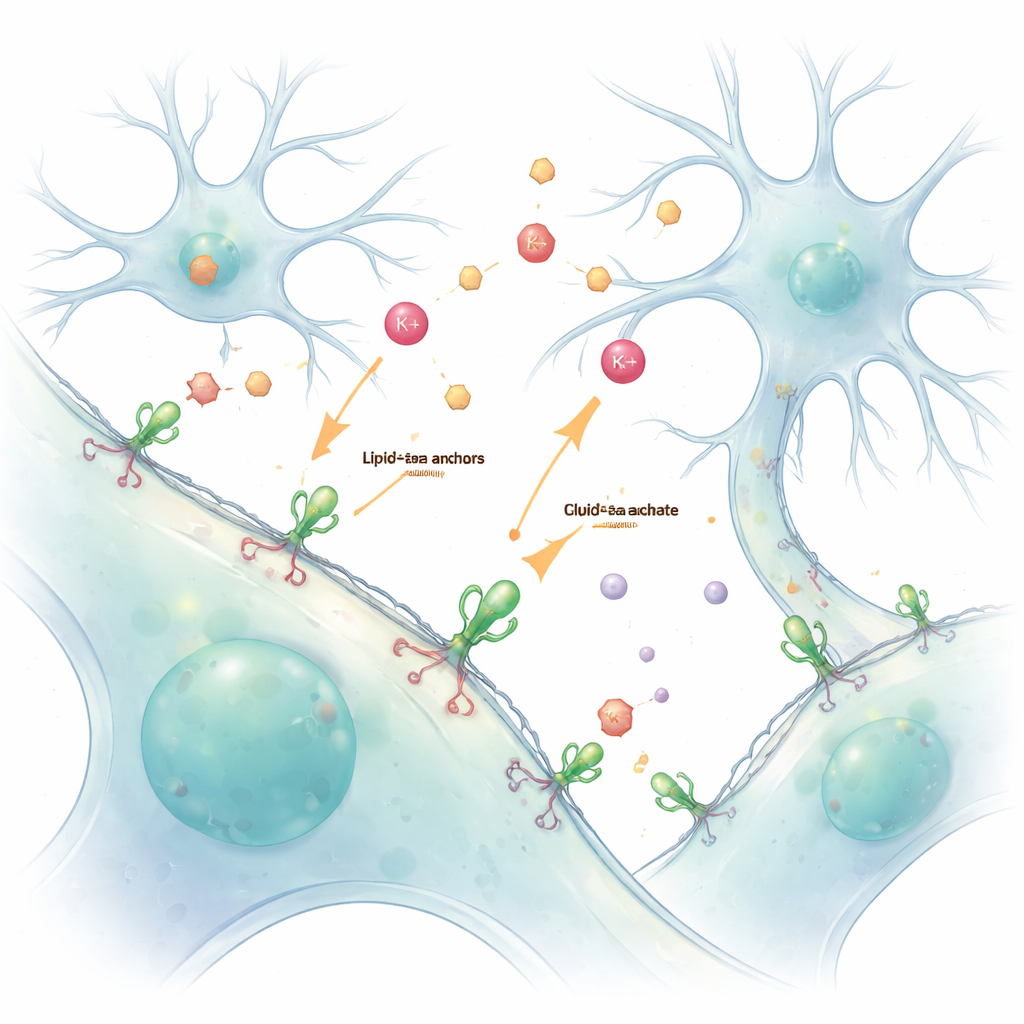
Nowy sposób znakowania powierzchni komórki
Tradycyjnie badacze inżynierują komórki tak, by wytwarzały fluorescencyjne czujniki białkowe z własnego DNA. Choć potężne, podejście genetyczne często powoduje, że czujniki trafiają wewnątrz komórki, co utrudnia oddzielenie tego, co dzieje się wewnątrz, od zdarzeń na zewnątrz. Autorzy rozwiązali to, stosując chemiczny uchwyt zwany kotwicą lipid–PEG. Jeden koniec tej cząsteczki wcina się w zewnętrzną błonę, a drugi koniec jest chemicznie połączony ze świecącym czujnikiem białkowym. Gdy przygotowane czujniki dodaje się do żywych komórek, spontanicznie pokrywają one powierzchnię zewnętrzną, tworząc stabilną, świetlną warstwę, która raportuje, co dzieje się w otaczającym płynie.
Przekształcanie potasu i glutaminianu w światło
Zespół zaadaptował dwa istniejące wskaźniki fluorescencyjne: GINKO2, reagujący na jony potasu, oraz R-iGluSnFR1, reagujący na glutaminian. Oczyszczono te białka z bakterii, a następnie dołączono kotwice lipid–PEG. W hodowlach komórek ludzkich zakotwiczony czujnik potasowy tworzył gładki obrys wzdłuż powierzchni komórki i rozjaśniał się za każdym razem, gdy stężenie potasu zewnątrzkomórkowego wzrastało, a potem przygasał, gdy poziomy spadały. Co ważne, jego właściwości emisji światła i czułość zgadzały się ściśle z oryginalnym, niemodyfikowanym sensorem w eksperymentach probówkowych, co pokazuje, że zakotwiczenie nie osłabiło jego działania. To samo dotyczyło sensora glutaminianu, który po zakotwiczeniu nadal reagował i wyraźnie uwidaczniał glutaminian w przestrzeni tuż poza komórkami.
Słuchanie neuronów w hodowlach i skrawkach
Następnie badacze przeszli do komórek nerwowych z hipokampa myszy, obszaru mózgu ważnego dla uczenia się i pamięci. Pokryli te neurony kotwiczonym sensorem glutaminianu lipid–PEG i załadowali wnętrza tych samych komórek oddzielnym barwnikiem wapniowym, który raportuje aktywność elektryczną. Używając mikroskopii całkowitego wewnętrznego odbicia, mogli obserwować czerwone błyski glutaminianu na powierzchni komórki, podczas gdy zielone sygnały wewnątrz komórek informowały o przepływach sygnału. Ten widok w dwóch kolorach pokazał, że zakotwiczone sensory mogą śledzić spontaniczne uwalnianie neuroprzekaźnika bez jakiejkolwiek modyfikacji genetycznej samych neuronów.
Mapowanie fal chemicznych w tkance mózgowej
Następnie zespół przetestował metodę w ostrych skrawkach mózgu, które zachowują naturalne połączenia hipokampa. Zastosowali zakotwiczony sensor potasu na skrawkach i elektrycznie stymulowali włókna nerwowe. Zakotwiczony sensor generował wyraźne, powtarzalne wzrosty fluorescencji po każdym bodźcu, podczas gdy sensory niezakończone szybko się rozpraszały i dawały słabe, niestabilne sygnały. Poprzez zanurzanie skrawków w roztworach o znanych stężeniach potasu i korygowanie o słabą autofluorescencję tkanki autorzy zbudowali krzywą kalibracyjną i oszacowali rzeczywiste stężenia potasu zewnątrzkomórkowego. Poziomy wyjściowe wynosiły około 2,5 milimolara i wzrastały do około 3,4 milimolara przy umiarkowanej stymulacji, co zgadza się z klasycznymi pomiarami elektrody. Zakotwiczone sensory zarówno dla potasu, jak i glutaminianu ujawniły, jak te sygnały rozchodzą się inaczej: zmiany glutaminianu pozostawały blisko aktywnych synaps, podczas gdy wzrosty potasu rozciągały się na setki mikrometrów, sugerując szersze efekty na pobudliwość sieci. 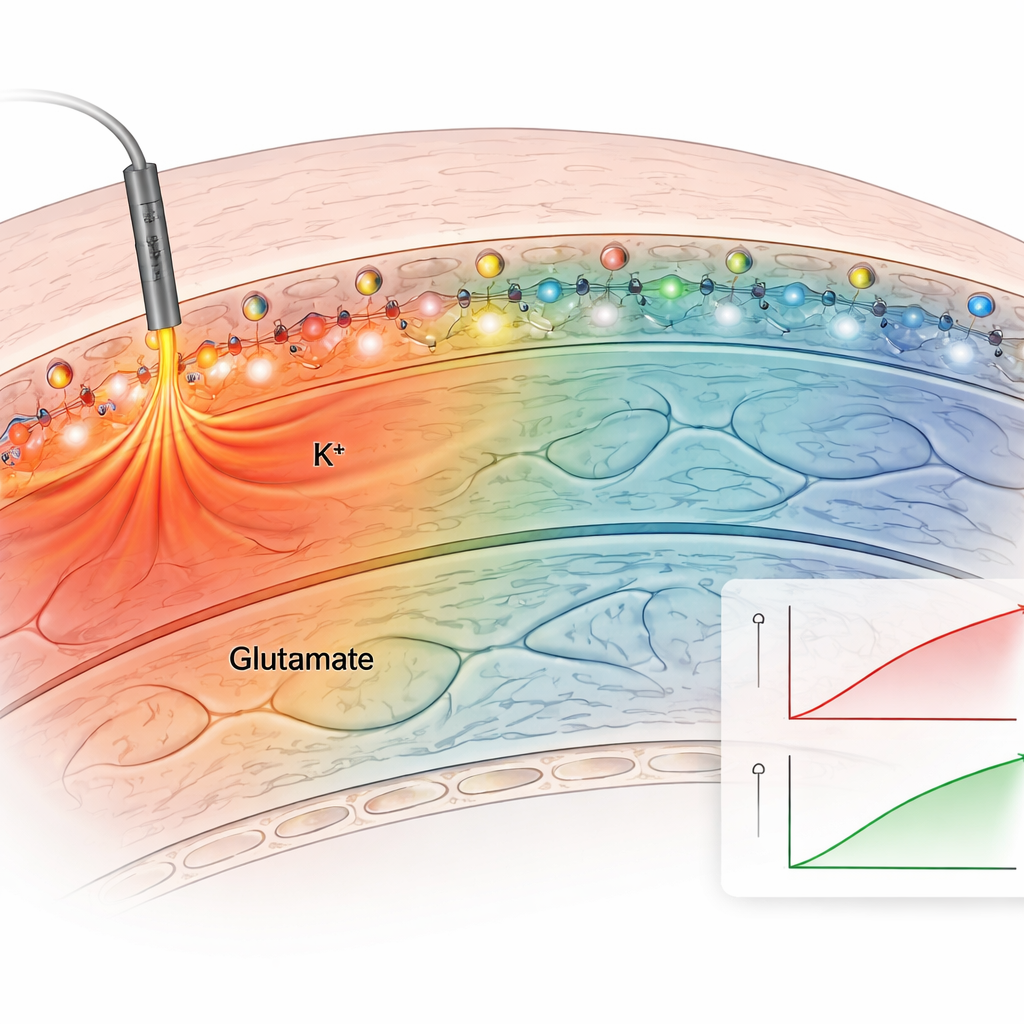
Badaniena temat, jak mózg oczyszcza i generuje sygnały
Ponieważ sensory są zamocowane na powierzchni komórki, autorzy mogli rozłożyć na czynniki pierwsze procesy kształtujące te zewnątrzkomórkowe fale. Zablokowanie transporterów glutaminianu, które normalnie usuwają glutaminian, spowodowało, że zakotwiczony sensor glutaminianu wykazał większe i dłużej utrzymujące się sygnały, potwierdzając, że lokalne wychwytywanie ogranicza rozprzestrzenianie się glutaminianu. Zablokowanie receptorów glutaminianowych typu AMPA zmniejszyło zarówno odpowiedzi elektryczne, jak i sygnały potasu, co wskazuje, że większość wzrostu potasu pochodzi z postsynaptycznych neuronów aktywowanych przez wejście synaptyczne. Zablokowanie kanałów sodowych tetrodotoksyną niemal całkowicie zlikwidowało zmiany potasu, wiążąc je bezpośrednio z potencjałami czynnościowymi. Razem te eksperymenty ilustrują, jak zakotwiczone sensory mogą przekształcić złożoną, rozproszoną chemię w intuicyjne filmy i mapy.
Dlaczego to ma znaczenie dla przyszłych badań nad mózgiem
Dla osób spoza dziedziny kluczowy przekaz jest taki, że to badanie oferuje szybki, niegenetyczny sposób pokrywania żywych komórek i tkanek wysoce czułymi reporterami molekularnymi. Zamiast rekonstruować genetycznie każdy typ komórki, naukowcy mogą dodać gotowe białkowe sensory z zewnątrz i natychmiast wizualizować, jak jony i neuroprzekaźniki zmieniają się w czasie rzeczywistym na powierzchni komórek. Podejście to poprawia kontrolę, powtarzalność i precyzję przestrzenną, unikając jednocześnie wyzwań związanych z dostarczaniem genów, zwłaszcza w delikatnych preparatach, takich jak ostre skrawki mózgu. W miarę rozwoju kolejnych wskaźników fluorescencyjnych dla różnych związków, ta sama strategia kotwiczenia lipid–PEG może stać się powszechnie stosowanym zestawem narzędzi do obserwowania chemicznego języka komórek w całym ciele.
Cytowanie: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Słowa kluczowe: sygnalizacja zewnątrzkomórkowa, fluorescencyjne biosensory, obrazowanie glutaminianu, dynamika potasu, neurony hipokampa