Clear Sky Science · pl
Wybór suplementacji lipidowej do hodowli erytroidów in vitro wpływa na wydajność i cechy retikulocytów
Dlaczego hodowla krwi w laboratorium ma znaczenie
Współczesna medycyna polega na krwi od dawców, ale zapasy często są ograniczone, a nie każdy pacjent może bezpiecznie otrzymać krew od dowolnego dawcy. Naukowcy pracują więc nad metodami hodowli czerwonych krwinek w laboratorium jako niezawodnego, konfigurowalnego zapasu. W tym badaniu postawiono zaskakująco podstawowe, ale kluczowe pytanie: czy rodzaj tłuszczów i cholesterolu podawanych młodym czerwonym krwinkom (retikulocytom) poza organizmem zmienia to, jak dobrze one działają?
Specjalna „skóra” czerwonych krwinek
Czerwone krwinki przetrwają miesiące, przeciskając się przez maleńkie naczynia krwionośne tysiące razy dziennie. Mogą to robić dzięki niezwykłej zewnętrznej „skórze”: elastycznemu szkieletowi białkowemu zakotwiczonym w błonie bogatej w cholesterol. W przeciwieństwie do większości komórek, nawet połowa lipidów w błonie erytrocyta to cholesterol. Ta równowaga sprawia, że komórka jest jednocześnie wytrzymała i podatna na odkształcenia. Za mało cholesterolu – błona staje się krucha; za dużo – sztywnieje. U ludzi zaburzenia w równowadze cholesterolu mogą skracać żywotność krwinek i pogarszać transport tlenu. Aby krew hodowana w laboratorium działała jak prawdziwa, musi odtworzyć tę precyzyjnie wyregulowaną błonę.
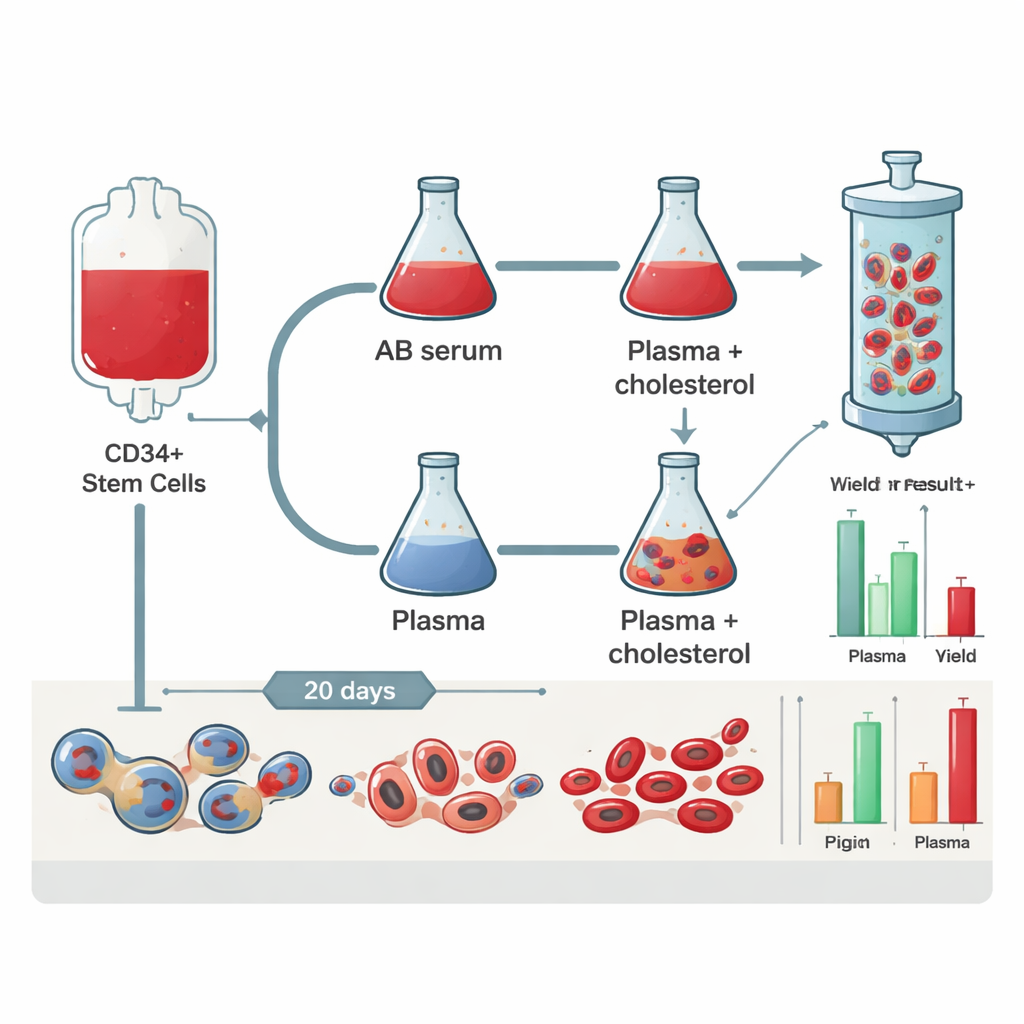
Testowanie różnych przepisów na krew hodowaną w laboratorium
Naukowcy użyli ludzkich komórek macierzystych oznaczonych markerem CD34, które pod wpływem odpowiednich czynników wzrostu mogą dojrzewać do czerwonych krwinek. Zachowali podstawowy przepis hodowlany, ale zmienili główne źródło lipidów (tłuszczów i cholesterolu). Jedna grupa otrzymywała surowicę ludzką AB, frakcję krwi od dawna stosowaną w hodowli erytrocytów. Druga grupa otrzymała zbankowane produkty osocza traktowane rozpuszczalnikami i detergentami w celu inaktywacji wirusów. Trzecia grupa otrzymała to samo osocze plus dodatkową mieszankę lipidów bogatych w cholesterol. Przez 20 dni zespół śledził tempo namnażania komórek, ile z nich skutecznie pozbyło się jądra, przechodząc w retikulocyty, oraz jak łatwo młode komórki dały się przefiltrować i obsłużyć, naśladując procedury przygotowania do transfuzji.
Osocze ubogie w cholesterol daje słabsze komórki
Komórki hodowane w surowicy AB dobrze się namnażały i dawały retikulocyty, które mogły przechodzić przez standardowe filtry krwi z rozsądną skutecznością — znak, że były wystarczająco odkształcalne, by zachowywać się jak normalne erytrocyty. Dla kontrastu, komórki hodowane w samym osoczu po obróbce rozpuszczalnikami rozmnażały się mniej, a co ważniejsze, po filtracji dawały bardzo niewiele retikulocytów, co sugeruje sztywniejsze, mniej elastyczne błony. Bezpośrednie pomiary przy użyciu fluorescencyjnej sondy cholesterolu oraz szczegółowy profil lipidowy potwierdziły, że te retikulocyty z osocza miały uderzająco niski poziom cholesterolu w porównaniu zarówno z prawidłowymi krwinkami, jak i z komórkami hodowanymi w surowicy AB. Komórki wyglądały, jakby wyczuwały ten deficyt: geny i białka zaangażowane w syntezę i import cholesterolu były włączone, co wskazuje, że komórki próbowały zrekompensować ubogie środowisko, ale nie były w stanie tego całkowicie naprawić.
Przywracanie funkcji przez uzupełnienie cholesterolu
Gdy do medium opartego na osoczu dodano dodatkowe lipidy bogate w cholesterol, wiele problemów uległo odwróceniu. Wydajność filtracji zbliżyła się do wyników obserwowanych przy surowicy AB, a całkowity poziom cholesterolu w retikulocytach wzrósł, dorównując młodym krwinkom pochodzącym z krwi rodowitej. Testy kruchego działania osmotycznego, które wystawiają komórki na coraz bardziej rozcieńczone roztwory soli, wykazały, że retikulocyty ubogie w cholesterol pękały wcześnie, podczas gdy komórki hodowane w surowicy i te z uzupełnionym cholesterolem zachowywały się bardziej jak normalne, nieco twardsze retikulocyty. Zespół zbadał także PIEZO1, kanał błonowy wyczuwający naprężenia mechaniczne i pomagający erytrocytom regulować objętość. W komórkach o niskim poziomie cholesterolu PIEZO1 słabo reagował na chemicznego aktywatora, ale jego aktywność została przywrócona po uzupełnieniu cholesterolu. Nawet zdolność pasożyta malarii Plasmodium falciparum do inwazji komórek korelowała z zawartością cholesterolu: inwazja była zmniejszona w retikulocytach pozbawionych cholesterolu i normalizowała się po jego uzupełnieniu.
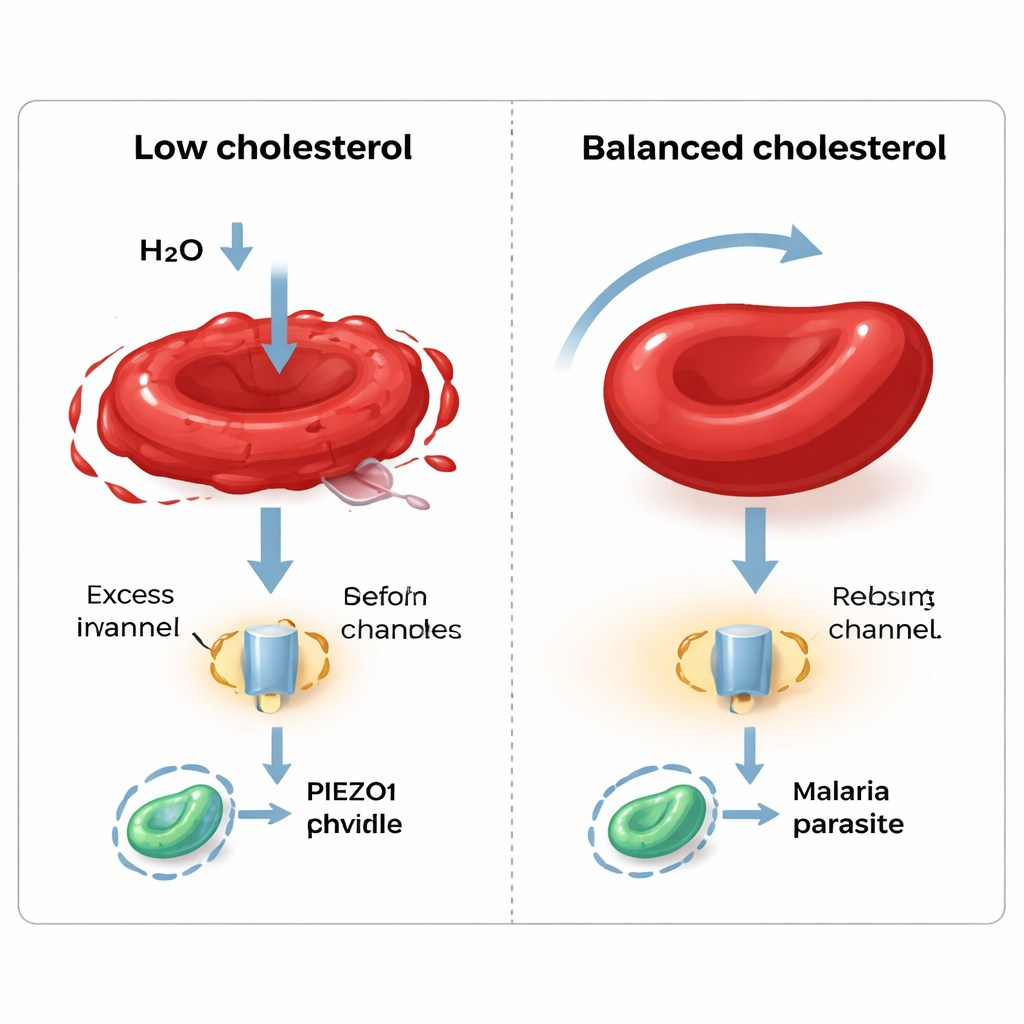
Znajdowanie właściwej równowagi dla przyszłych transfuzji
W sumie wyniki pokazują, że rodzaj suplementu lipidowego użytego podczas hodowli czerwonych krwinek in vitro może silnie wpływać na zawartość cholesterolu, wytrzymałość i zachowanie otrzymanych retikulocytów. Ludzka surowica AB naturalnie dostarcza wystarczająco dużo cholesterolu, by wspierać zdrowy rozwój, podczas gdy niektóre przetworzone produkty osoczowe tego nie robią, chyba że zostaną specjalnie uzupełnione. Nadmiar cholesterolu może jednak zacząć usztywniać komórki, więc potrzebne jest ostrożne dostrojenie. Dla przyszłych biorców krwi hodowanej w laboratorium przesłanie jest proste: dopracowanie „przepisu na błonę” jest równie ważne jak uzyskanie wystarczającej liczby komórek. Mapując, jak tłuszcze, metabolity i białka zmieniają się w różnych warunkach, praca ta dostarcza drogowskazu do standaryzacji mediów hodowlanych, aby retikulocyty wyhodowane w laboratorium wiernie naśladowały swoje naturalne odpowiedniki i były bezpieczne, trwałe i skuteczne we krwiobiegu.
Cytowanie: Freire, C.M., King, N.R., Dzieciatkowska, M. et al. Choice of lipid supplementation for in vitro erythroid cell culture impacts reticulocyte yield and characteristics. Sci Rep 16, 6632 (2026). https://doi.org/10.1038/s41598-026-37229-z
Słowa kluczowe: czerwone krwinki hodowane w laboratorium, cholesterol i błony, hodowla retikulocytów, substytuty krwi, erytropoeza in vitro