Clear Sky Science · pl
Klasyfikacja stadium choroby Alzheimera na podstawie neuroobrazowania MRI przy użyciu głębokiej sieci neuronowej z modułem uwagi bloków splotowych i wstrzyknięciem szumu w stylu GAN
Dlaczego wczesne badania mózgu są ważne
Choroba Alzheimera stopniowo zabiera pamięć i samodzielność, często na długo zanim objawy stają się wyraźne. Rodziny, lekarze i pacjenci chcą metody pozwalającej wykryć chorobę wcześnie, gdy leczenie i zmiany stylu życia mają największą skuteczność. W tym badaniu opisano nowy system komputerowy, który analizuje rutynowe skany mózgu i potrafi z dużą dokładnością przyporządkować osoby do czterech stadiów związanych z utratą pamięci w przebiegu Alzheimera, co może dać klinicystom szybszą, tańszą i bardziej spójną opinię uzupełniającą.
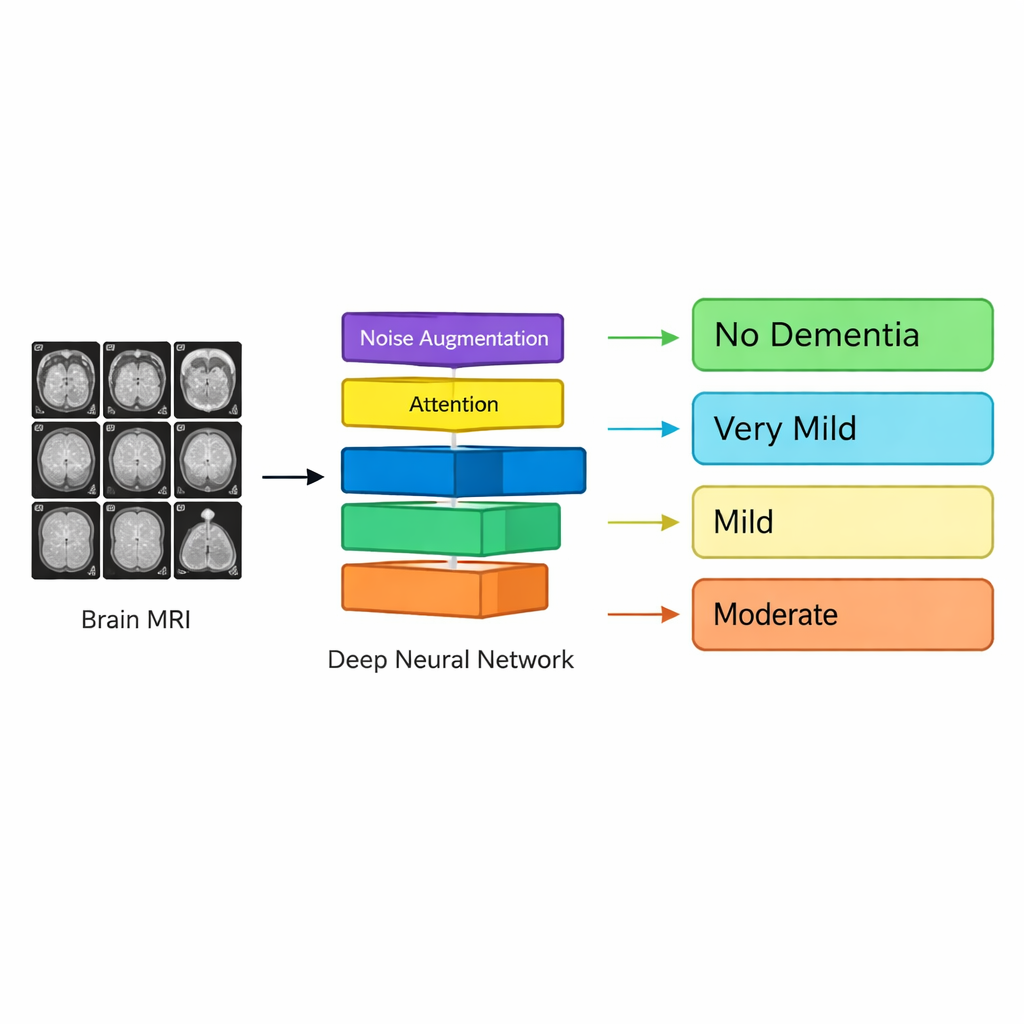
Bliżej wnętrza mózgu
Naukowcy koncentrują się na skanach MRI, które pokazują szczegółową strukturę mózgu bez zabiegu chirurgicznego czy promieniowania. Wykorzystują dane z dużego międzynarodowego projektu Alzheimer’s Disease Neuroimaging Initiative (ADNI), w którym ochotnicy w wieku 55–90 lat regularnie przechodzą testy pamięci i badania obrazowe mózgu. Z tych skanów zespół wyodrębnia 2D-przekroje mózgu i dzieli je na cztery grupy: osoby bez demencji oraz te z bardzo łagodną, łagodną lub umiarkowaną demencją. Odzwierciedla to typowy przebieg Alzheimera w rzeczywistości, gdzie drobne zmiany w pamięci i myśleniu stopniowo się nasilają.
Nauka komputera dostrzegania subtelnych zmian
Zamiast polegać na ekspertach wybierających ręcznie obszary mózgu i cechy, autorzy trenują system głębokiego uczenia — podobny w założeniu do tych używanych w rozpoznawaniu twarzy czy autonomicznych pojazdach — by uczył się bezpośrednio z obrazów. Ich model, nazwany Neuro_CBAM-ADNet, to rodzaj konwolucyjnej sieci neuronowej, która świetnie radzi sobie z rozpoznawaniem wzorców na zdjęciach. W miarę jak obraz MRI przechodzi przez sieć, jest przetwarzany przez kolejne warstwy wykrywające krawędzie, tekstury i coraz bardziej złożone kształty, aż system potrafi wyróżnić wzorce korelujące z różnymi stadami demencji, z których wiele jest zbyt subtelnych, by dostrzec je gołym okiem.
Pomagając komputerowi skupić się na tym, co ważne
Kluczową innowacją jest mechanizm „uwagi”, który delikatnie kieruje sieć tak, by koncentrowała się na najbardziej informatywnych częściach skanu. W praktyce model uczy się, które lokalizacje i wewnętrzne cechy mózgu zwykle się zmieniają w miarę postępu Alzheimera — na przykład rejony związane z pamięcią i procesami poznawczymi — ignorując mniej istotne tło. Badacze rozwiązują też powszechny problem danych medycznych: niektóre stadia choroby występują znacznie rzadziej, przez co model mógłby faworyzować klasę większościową. Aby temu przeciwdziałać, generują dodatkowe obrazy treningowe dla niedostatecznie reprezentowanych grup, dodając starannie kontrolowany szum do istniejących skanów, naśladując naturalną zmienność występującą u prawdziwych pacjentów bez zniekształcania podstawowej anatomii.
Testowanie systemu
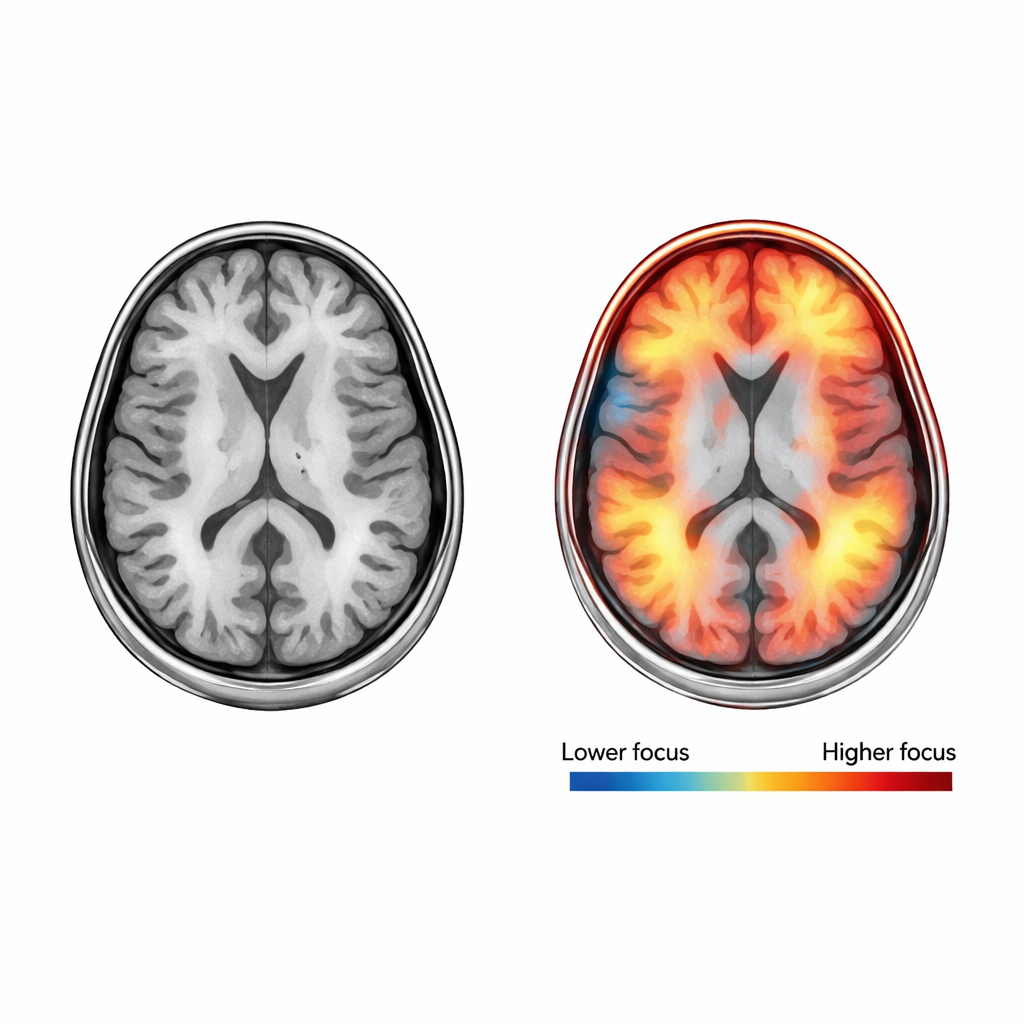
Aby sprawdzić, jak wiarygodnie działa ich system, zespół wielokrotnie trenuje i testuje go na różnych podzbiorach danych, w procesie zwanym walidacją krzyżową. W pięciu niezależnych rundach Neuro_CBAM-ADNet poprawnie klasyfikuje stadium demencji w około 98 procent przypadków, osiągając podobnie wysokie wyniki w zakresie czułości (wychwytywania przypadków), precyzji (unikania fałszywych alarmów) oraz miary łączonej zwanej F1-score. System jest szczególnie mocny w rozróżnianiu wyraźnie różnych grup, takich jak demencja umiarkowana versus brak demencji, a większość błędów występuje między sąsiednimi stadami, takimi jak brak demencji i bardzo łagodna demencja, gdzie nawet specjaliści często się nie zgadzają. Dodatkowe narzędzia, zwane mapami cieplnymi Grad-CAM, pokazują, na które obszary mózgu model „patrzy” przy podejmowaniu decyzji, dostarczając wizualnych wskazówek, które można porównać z znanymi markerami choroby.
Co to oznacza dla pacjentów i lekarzy
Mówiąc prosto, praca ta pokazuje, że dobrze zaprojektowany system AI potrafi odczytywać skany mózgu i przyporządkowywać osoby do czterech stadiów spadku związanego z Alzheimerem z poziomem spójności, który dorównuje, a w niektórych przypadkach przewyższa wcześniejsze podejścia. Robi to, wskazując jednocześnie rejony mózgu, które wpływają na jego decyzje, co może budować zaufanie wśród klinicystów. Choć narzędzie wymaga jeszcze szerszych testów w różnych szpitalach i na różnych aparatach, sugeruje przyszłość, w której rutynowe badania MRI, w połączeniu z przejrzystą sztuczną inteligencją, mogłyby pomóc wykrywać wczesne zmiany mózgowe, wspierać pewniejsze rozpoznania i prowadzić decyzje terapeutyczne zanim choroba zdąży znacznie się rozwinąć.
Cytowanie: Kumar, S., Shastri, S., Mansotra, V. et al. MRI neuroimaging-based Alzheimer’s disease stage classification using deep neural network with convolutional block attention module and GAN-style noise injection. Sci Rep 16, 6946 (2026). https://doi.org/10.1038/s41598-026-37226-2
Słowa kluczowe: choroba Alzheimera, MRI mózgu, głębokie uczenie, wczesna diagnostyka, AI w obrazowaniu medycznym