Clear Sky Science · pl
Dynamiczna konwolucja grafowa z kompleksowym przycinaniem i klasyfikacją GNN w celu precyzyjnego wykrywania przerzutów do węzłów chłonnych
Dlaczego drobne zmiany w węzłach chłonnych mają znaczenie
Gdy rak piersi się rozprzestrzenia, jego pierwszym przystankiem często są węzły chłonne — niewielkie filtry leżące wzdłuż układu limfatycznego. Rozpoznanie, czy komórki nowotworowe dotarły do tych węzłów, jest jednym z kluczowych wskaźników, które lekarze wykorzystują przy wyborze operacji, chemioterapii i radioterapii. Nawet doświadczeni patolodzy mogą jednak przeoczyć bardzo małe skupiska komórek nowotworowych na cyfrowych obrazach mikroskopowych, zwłaszcza gdy wyglądają praktycznie identycznie jak tkanka zdrowa. W tym badaniu przedstawiono nowe rozwiązanie oparte na sztucznej inteligencji, które traktuje tkankę jako sieć połączonych regionów, co pozwala wykrywać subtelne oznaki rozsiewu z imponującą dokładnością.
Przekształcanie obrazów tkanek w sieci
Badacze pracują na ogromnych cyfrowych skanach barwionych tkanek, zwanych obrazami całego preparatu, pochodzących z biopsji węzłów chłonnych u pacjentek z rakiem piersi. Obrazy te zawierają miliony pikseli oraz złożone zestawienia typów komórek, kolorów i tekstur. Aby okiełznać tę złożoność, zespół najpierw oczyszcza obrazy: normalizuje jasność i barwę, redukuje szum oraz generuje dodatkowe wersje przez obracanie i odbicia fragmentów, tak aby komputer nauczył się radzić sobie z naturalną zmiennością. Każdy fragment obrazu jest następnie dzielony na małe, stosunkowo jednorodne regiony („superpiksele”), które stają się punktami — węzłami — w grafie, a relacje między sąsiednimi regionami tworzą łączące je krawędzie. Takie podejście sieciowe lepiej zachowuje nieregularne kształty i układy rzeczywistej tkanki niż tradycyjne metody oparte na siatce pikseli.
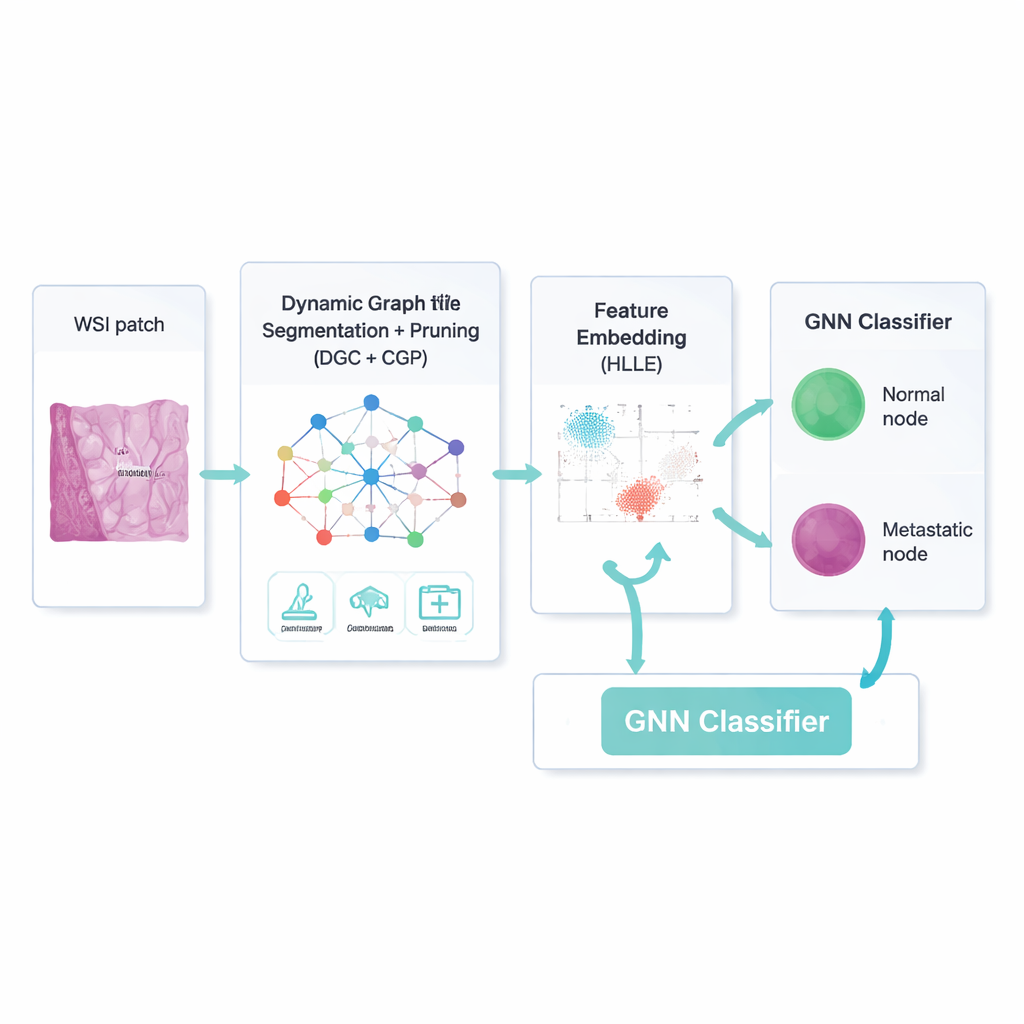
Mądrzejszy sposób skupiania się na istotnym
Samą konstrukcją sieci nie rozwiążemy problemu; wiele połączeń i cech obrazu jest nieistotnych, a nawet mylących. Dlatego ramy metodyczne wykorzystują dynamiczny konwolucyjny autoenkoder grafowy — typ sieci neuronowej, który uczy się zarówno wyglądu każdego regionu, jak i tego, jak regiony na siebie wpływają. Dodatkowy mechanizm „uwagi” uczy model nadawać większą wagę niektórym kanałom obrazu niż innym, na przykład podkreślając krawędzie na granicy guza. Jednocześnie strategia nazwana Comprehensive Graph Gradual Pruning stopniowo przycina nieprzydatne elementy: słabe połączenia między regionami, mniej użyteczne cechy numeryczne i niskowpływowe wagi modelu. Przycinanie odbywa się w trakcie treningu, nie po jego zakończeniu, dzięki czemu system uczy się robić więcej przy użyciu mniejszej liczby zasobów, kończąc jako szybszy i łatwiejszy do interpretacji.
Kompresja wzorców bez utraty ich kształtu
Po tym, jak model oddzieli prawdopodobne obszary węzłów chłonnych od tła tkankowego, nadal musi opisać każdy region w sposób kompaktowy, lecz znaczący. Do tego autorzy używają techniki opartej na lokalnym osadzaniu liniowym z wykorzystaniem hesjanu (Hessian-based Locally Linear Embedding). Mówiąc prościej, redukuje ona dużą liczbę cech numerycznych do mniejszego zestawu, starając się jednocześnie zachować zakrzywiony „kształt” rozmieszczenia rzeczywistych przykładów w przestrzeni cech — na przykład to, jak drobne przerzuty odróżniają się od normalnych komórek odpornościowych subtelnymi wzorcami tekstury lub koloru. Te skompresowane opisy stają się wejściem do klasyfikatora opartego na grafowych sieciach neuronowych, który ponownie działa na sieci regionów i ich oczyszczonych połączeniach, decydując dla każdego węzła, czy jest przerzutowy, czy nie.
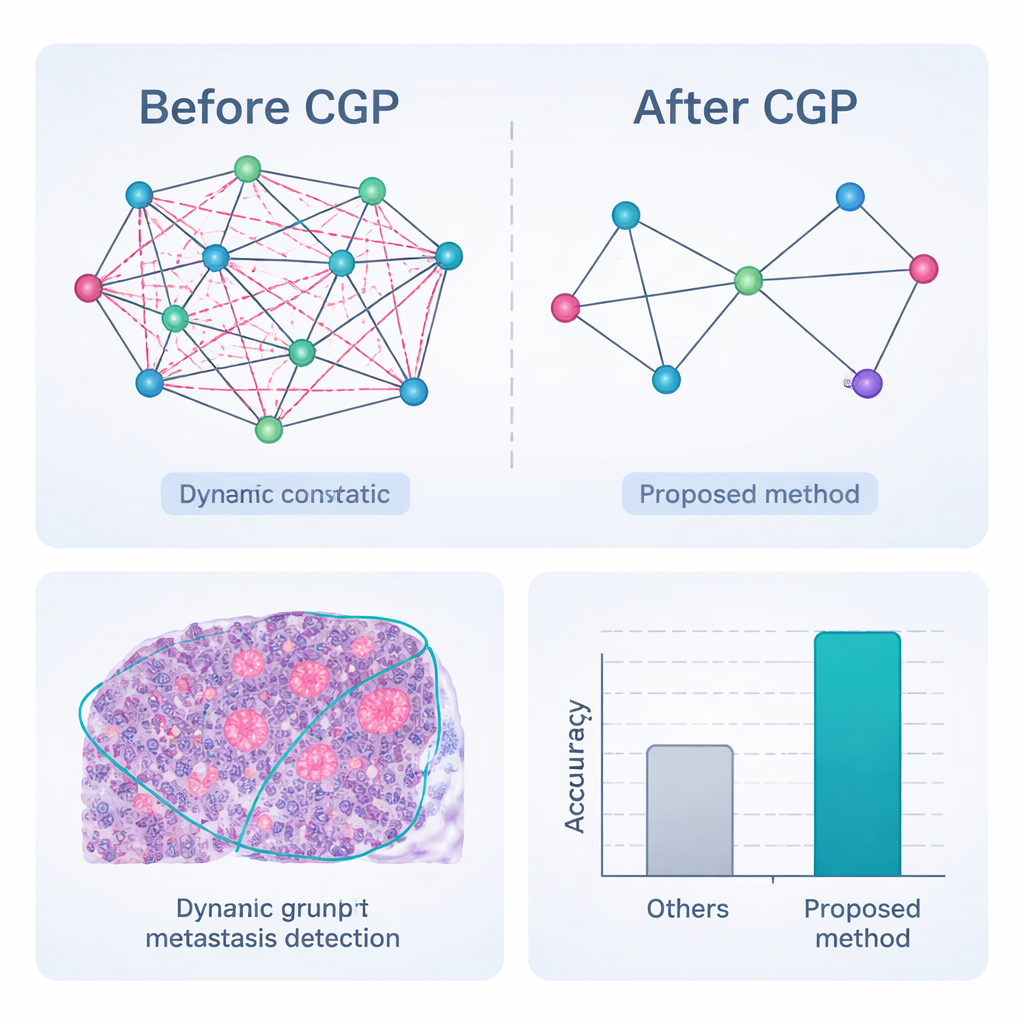
Testowanie ram metodologicznych
Pełen pipeline — wstępne przetwarzanie, dynamiczna segmentacja grafowa z przycinaniem, osadzanie cech i klasyfikacja oparta na grafie — oceniono na zestawie CAMELYON17, publicznej kolekcji 1000 starannie oznakowanych skanów węzłów chłonnych od pacjentek z rakiem piersi. W porównaniu z szeregiem silnych konkurentów opartych na głębokim uczeniu, w tym popularnych sieciach konwolucyjnych i hybrydowych modelach transformerowych, nowa metoda osiągnęła najwyższe wyniki w niemal wszystkich miarach. Prawidłowo sklasyfikowała węzły jako nowotworowe lub nie w 98,65% przypadków i wykazała lepszą zgodność z eksperckimi obrysami obszarów guza, szczególnie dla bardzo małych lub słabo widocznych przerzutów. Co ważne, ponieważ graf jest agresywnie przycinany, system osiąga te wyniki przy znacznie mniejszej liczbie obliczeń i niższym użyciu pamięci, co czyni go bardziej odpowiednim do zastosowań w czasie rzeczywistym w obciążonych pracowniach patologicznych.
Co to oznacza dla pacjentów i klinicystów
W praktycznych słowach praca ta pokazuje, że traktowanie tkanki jako inteligentnie przyciętej sieci połączonych regionów może pomóc komputerom pełnić rolę niezwykle skrupulatnych drugich czytelników preparatów węzłów chłonnych. Koncentrując uwagę i moc obliczeniową na najbardziej informacyjnych strukturach, przy jednoczesnym odrzuceniu szumu, ramy te lepiej wykrywają drobne ziarna nowotworu, które mogłyby inaczej zostać przeoczone, i robią to na tyle efektywnie, żeby być praktyczne. Chociaż potrzebne są dalsze walidacje kliniczne, takie narzędzia mogą wspierać patologów w podejmowaniu szybszych, bardziej spójnych decyzji dotyczących tego, czy rak się rozprzestrzenił — informacji, która bezpośrednio kształtuje plany leczenia i ostatecznie wyniki dla pacjentów.
Cytowanie: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Słowa kluczowe: przerzuty do węzłów chłonnych, patologia cyfrowa, sieć neuronowa grafowa, segmentacja obrazów medycznych, rak piersi