Clear Sky Science · pl
Charakterystyka strukturalna wiązania metalu w ludzkiej tirozyloproteinowej sulfotransferazie 2, TPST2
Dlaczego drobne jony metali mają znaczenie dla sygnalizacji komórkowej
W naszych komórkach niezliczone molekularne maszyny dyskretnie regulują wzrost tkanek, działanie hormonów i komunikację komórek układu odpornościowego. Jedną z takich maszyn jest enzym TPST2, który dołącza niewielką grupę siarczanową do wybranych białek podczas ich przejścia przez centrum wysyłkowe komórki — aparat Golgiego. Badanie to ujawnia, jak proste jony metali, takie jak sód i mangan, zwiększają wydajność TPST2 przez subtelne usztywnienie fragmentów jego struktury — wgląd, który może łączyć równowagę minerałów w komórkach z rakiem i chorobami związanymi z hormonami. 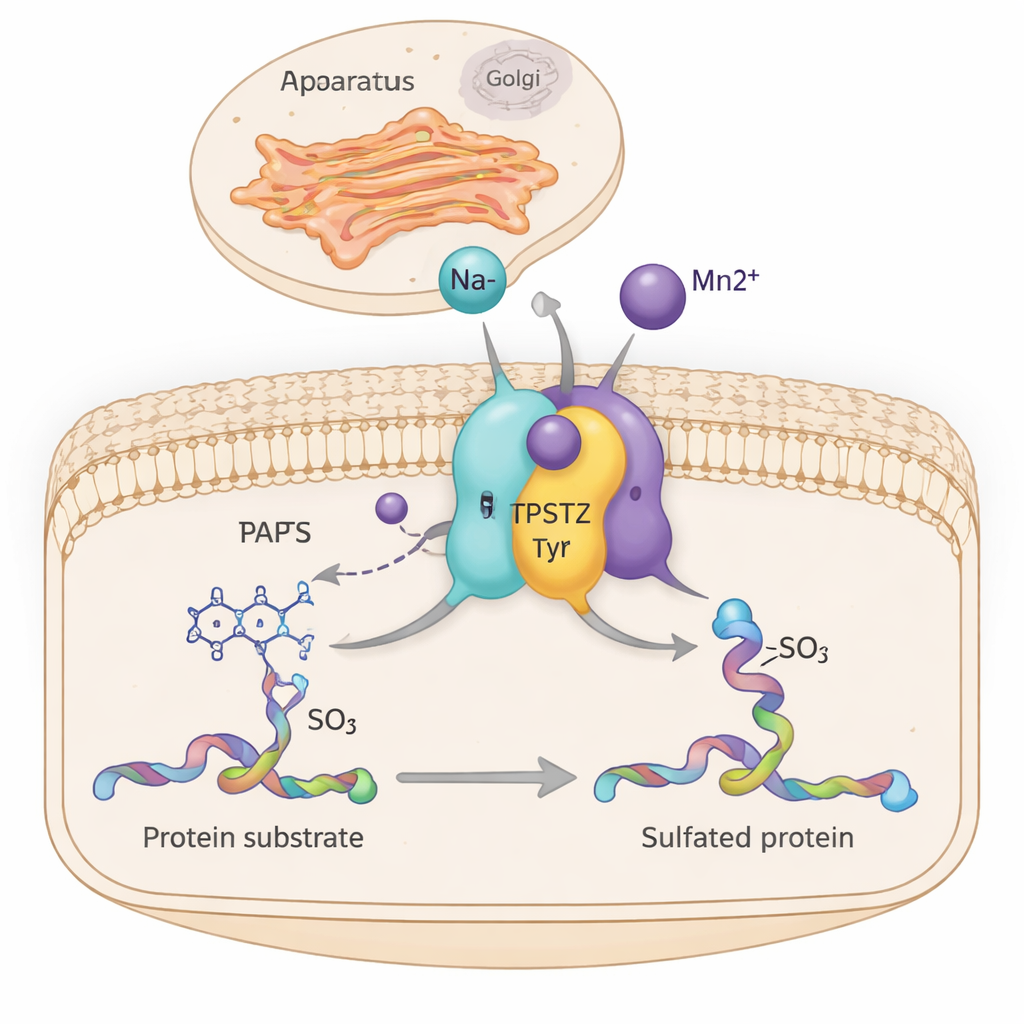
Białko, które ozdabia inne białka
TPST2 należy do rodziny enzymów przeprowadzających „sulfację tyrozyny”, czyli chemiczną modyfikację wprowadzoną w określone reszty tyrozynowe białek. Sulfowane białka odgrywają kluczowe role poza komórkami, wpływając na krzepnięcie krwi, migrację białych krwinek, wiązanie hormonów z receptorami, a nawet na to, jak wirusy wnikają do komórek. U ludzi występują dwie główne sulfotransferazy, TPST1 i TPST2, które osadzone są w błonie Golgiego i modyfikują białka podczas ich przygotowywania do eksportu. Badania na myszach pokazują, że utrata TPST2 zaburza produkcję hormonów tarczycy, zahamowuje wzrost i powoduje niepłodność samców, podkreślając jej znaczenie dla prawidłowej fizjologii.
Powiązania z rakiem i ucieczką przed układem odpornościowym
Ostatnie badania wiążą TPST2 bezpośrednio z chorobami. W czerniaku TPST2 modyfikuje część receptora interferonowego w sposób osłabiający sygnalizację odpornościową, a zablokowanie TPST2 zwiększa skuteczność terapii przeciwko punktom kontrolnym układu odpornościowego ukierunkowanym na PD-1. W raku trzustki szlak zależny od TPST2 pomaga stabilizować białko (integrynę β4), które sprzyja wzrostowi i szerzeniu się guza. Hamowanie TPST2 w tych modelach spowalnia podziały i inwazję komórek nowotworowych. Ponieważ TPST2 działa na białka na powierzchni komórek, skutecznie przeprogramowuje sposób, w jaki komórki odbierają i reagują na otoczenie, co czyni go atrakcyjnym celem dla nowych terapii.
Odnalezienie metalowych „włączników”
Biochemicy od dawna wiedzieli, że aktywność TPST2 znacznie wzrasta w obecności metali dwuwartościowych, takich jak mangan (Mn²⁺), ale brakowało wyjaśnienia strukturalnego. W tym badaniu autorzy wytworzyli katalityczne jądro ludzkiego TPST2 i skrystalizowali je razem z produktem ubocznym reakcji oraz z jonami sodu (Na⁺) lub manganu. Przy użyciu krystalografii rentgenowskiej o wysokiej rozdzielczości odkryli dwie małe kieszenie wiążące metal wewnątrz enzymu, każdą o uporządkowaniu wokół centrów w sześciokrotnym (oktaedrycznym) układzie atomów. Strojąc długość fali promieniowania rentgenowskiego do unikalnych sygnatur różnych metali, potwierdzili, że Mn²⁺ selektywnie zajmuje te miejsca, podczas gdy metale takie jak cynk i miedź wiążą się słabo w innych lokalizacjach lub wcale.
Usztywnienie kluczowych ruchomych elementów zamiast przekształcenia całości
Zaskakująco, TPST2 z sodem i TPST2 z manganem wyglądały niemal identycznie w skali całego białka; nie zaobserwowano dramatycznego otwierania ani zamykania struktury. Zamiast tego metale oddziaływały głównie na dwa elastyczne regiony przy wlocie do miejsca aktywnego: helisę nazwaną α3 oraz pobliski pętlę znaną jako pętla α12–α13. W stanach bez metalu lub przy luźnym wiązaniu te segmenty wykazują ruchliwość i częściowe uporządkowanie. Po związaniu Na⁺ stają się bardziej uporządkowane; Mn²⁺ dodatkowo je usztywnia, co ilustruje zmniejszony ruch termiczny w danych rentgenowskich oraz analizy elastyczności wykonane komputerowo. Ta dodatkowa sztywność nieznacznie podnosi temperaturę topnienia enzymu i uważa się, że obniża „entropowy” koszt organizacji miejsca aktywnego — ułatwiając i przyspieszając umieszczanie substratów TPST2 w odpowiedniej pozycji do sulfacji. 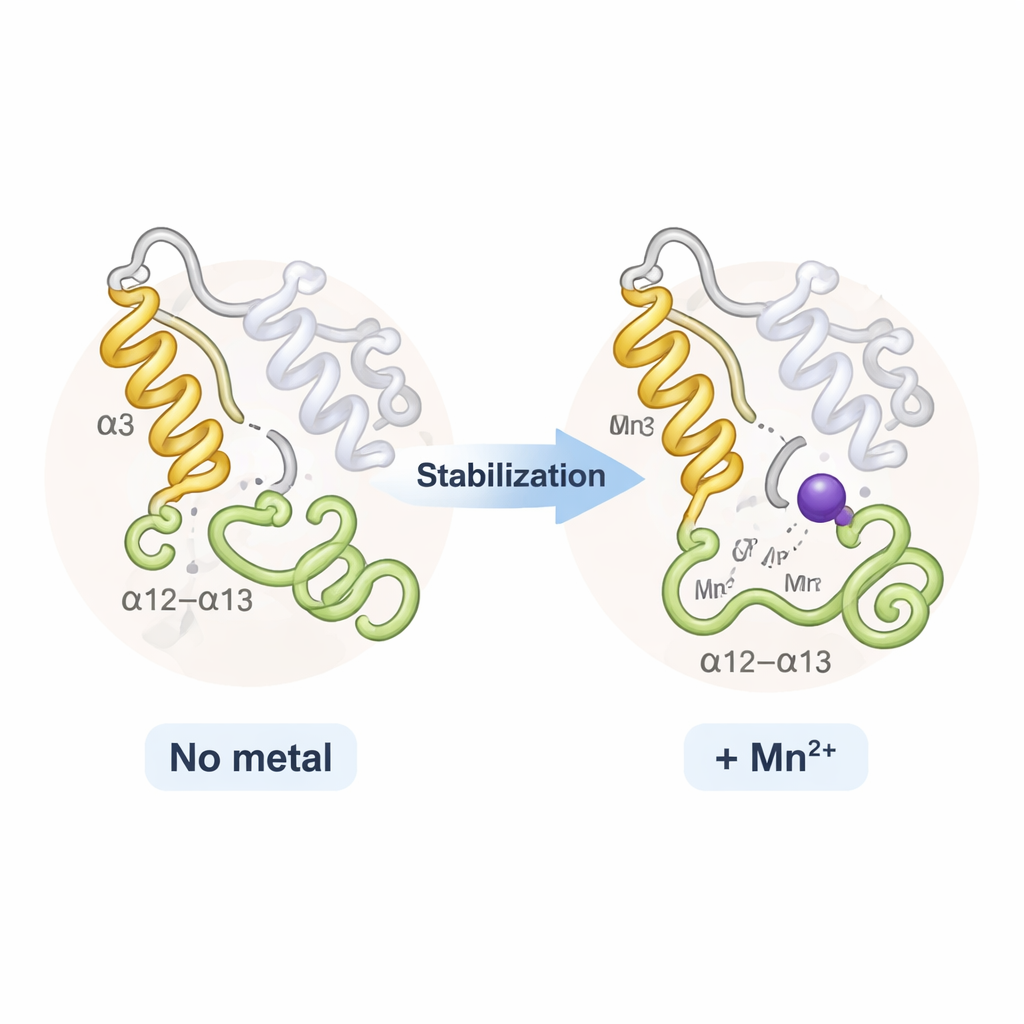
Od minerałów komórkowych do kontroli sygnalizacji
Autorzy proponują model „aktywacji przez uporządkowanie”. W braku związanych jonów TPST2 jest wiotki wokół wejścia do miejsca aktywnego i działa nieefektywnie. Sód, obficie obecny w komórkach, może zająć te same miejsca i stworzyć częściowo uporządkowany, umiarkowanie aktywny stan. Mangan, występujący w aparacie Golgiego w ściśle kontrolowanych ilościach mikromolowych, wiąże się silniej i blokuje kluczowe regiony w optymalnie ułożonym stanie, maksymalizując efektywność katalityczną. To sugeruje, że subtelne zmiany poziomu manganu w Golgim mogą regulować, jak silnie TPST2 modyfikuje swoje cele. Ponieważ TPST2 wpływa na produkcję hormonów i sygnalizację związaną z rakiem, praca podkreśla potencjalne powiązanie między balansem jonów metali, „ozdobami” białek a chorobami — oraz dostarcza ram strukturalnych do projektowania leków, które modulują aktywność TPST2 przez naśladowanie lub zakłócanie wiązania metalu.
Cytowanie: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Słowa kluczowe: sulfacja tyrozyny, TPST2, mangan, aparat Golgiego, modyfikacja białka