Clear Sky Science · pl
Interpretable hybrid ensemble with attention-based fusion and EAOO-GA optimization for lung cancer detection
Dlaczego wczesne wykrywanie raka płuca ma znaczenie dla wszystkich
Rak płuca jest jednym z najbardziej zabójczych nowotworów głównie dlatego, że często bywa wykrywany zbyt późno, gdy opcje leczenia są ograniczone, a szanse przeżycia gwałtownie maleją. Lekarze coraz częściej polegają na tomografii komputerowej (TK) i programach komputerowych, aby wychwycić podejrzane zmiany w płucach zanim pojawią się objawy. W artykule przedstawiono nowy system sztucznej inteligencji (AI), którego celem jest nie tylko zwiększenie dokładności takich komputerowych diagnoz, lecz także poprawa ich niezawodności i czytelności dla klinicystów.
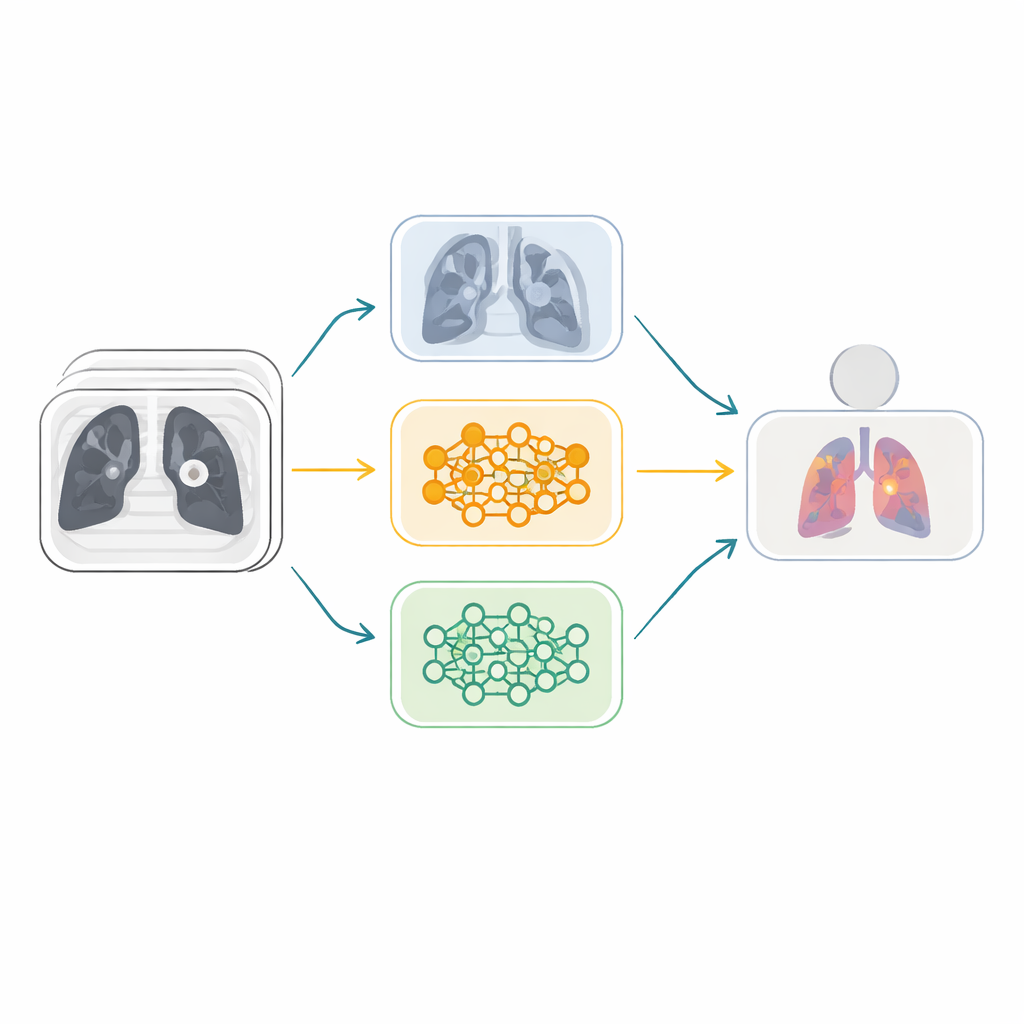
Jak komputery „czytają" skany płuc
Nowoczesne systemy AI mogą analizować obrazy TK i uczyć się wzorców, które odróżniają niegroźną plamkę od niebezpiecznego guza. Systemy te, oparte na głębokich sieciach neuronowych, już wykazały, że w wąskich zadaniach mogą dorównywać lub przewyższać ekspertów ludzkich. W praktyce klinicznej napotykają jednak trzy istotne przeszkody: mogą dopasować się nadmiernie do jednego zbioru danych i zawieść na nowych pacjentach, mają trudności z niezrównoważonymi danymi, w których niektóre typy przypadków są rzadkie, oraz często działają jak nieprzejrzyste „czarne skrzynki”, którym klinicyści trudno zaufać. Autorzy koncentrują się na tych wyzwaniach, analizując powszechnie stosowany zestaw danych TK płuc zawierający trzy typy przypadków: guzy łagodne, guzy złośliwe oraz skany prawidłowe.
Wiele eksperckich spojrzeń zamiast jednego
Zamiast polegać na pojedynczej sieci neuronowej, badacze budują zespół — ensemble — czyli grupę różnych modeli AI głosujących wspólnie. Wyjściem są sześć zaawansowanych architektur rozpoznawania obrazów, początkowo trenowanych na milionach zwykłych zdjęć, zaadaptowanych do skanów TK płuc. Modele te łączone są parami w trzy gałęzie „fuzji”, z których każda łączy dwa sieciowe rozwiązania o uzupełniających się mocnych stronach. W obrębie każdej gałęzi działa specjalny mechanizm uwagi, znany jako Squeeze-and-Excitation, który uczy się, które kanały cech wewnętrznych niosą najważniejsze wskazówki wizualne — na przykład subtelne faktury czy kształty guzków — i wzmacnia je, jednocześnie tłumiąc mniej informacyjne wzorce. Dzięki temu system koncentruje się na medycznie istotnych detalach zamiast na szumie.
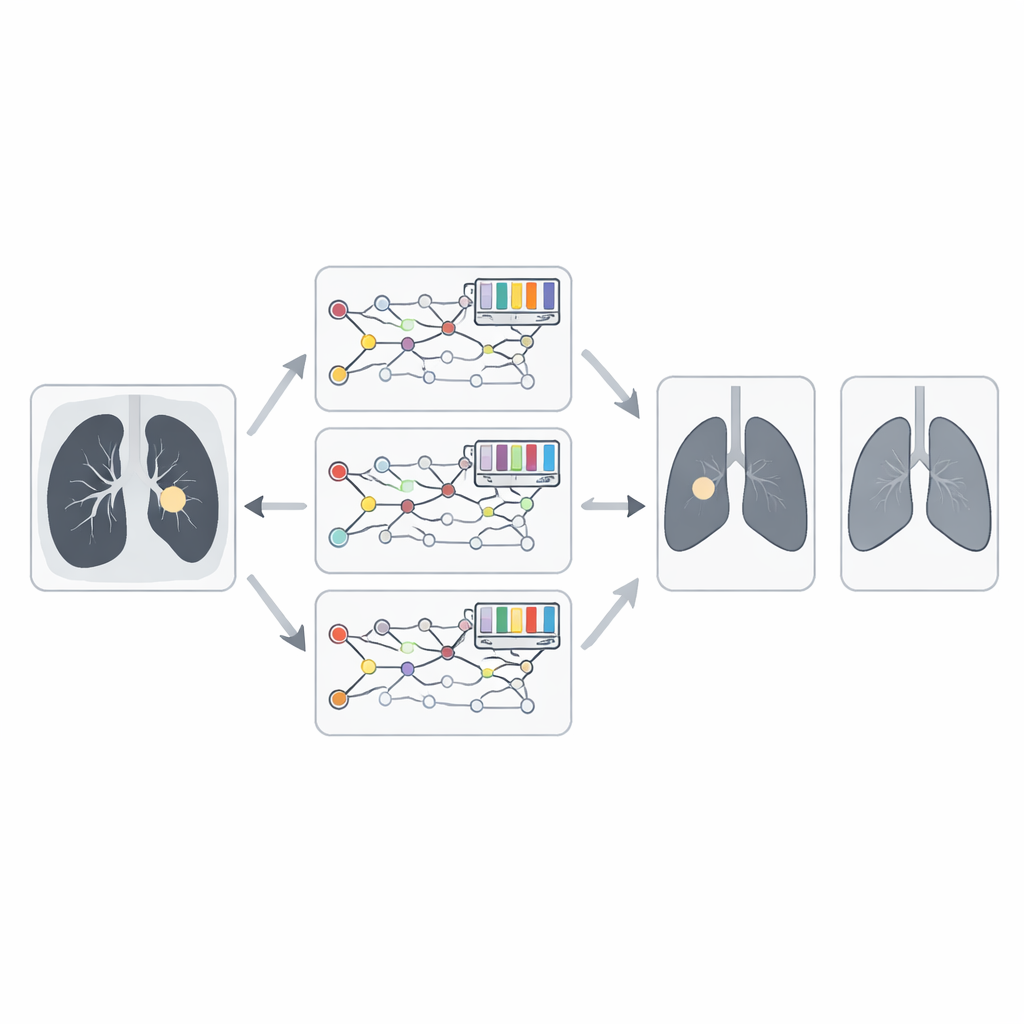
Pozwolić przyrodzie zoptymalizować zespół
Proste uśrednienie opinii trzech silnych gałęzi nadal pozostawia pole do poprawy. Kluczowy pomysł w tej pracy polega na użyciu optymalizatora inspirowanego naturą do określenia, jaką wagę przypisać każdej gałęzi. Autorzy wprowadzają rozszerzoną wersję algorytmu Animated Oat Optimization, wzbogaconą operacjami genetycznymi, takimi jak krzyżowanie i mutacja. Mówiąc prościej, algorytm traktuje kandydackie kombinacje wag jak populację i wielokrotnie ją „ewoluuje”, zachowując te rozwiązania, które prowadzą do dokładniejszych prognoz raka, a przetasowując pozostałe. Po wielu iteracjach znajduje skuteczną równowagę, w której najbardziej wiarygodne modele fuzji mają większy wkład w ostateczną diagnozę.
Zrównoważenie rzadkich przypadków i otwarcie czarnej skrzynki
Rzeczywiste zbiory medyczne często zawierają znacznie więcej przypadków złośliwych niż łagodnych czy prawidłowych, co może skłaniać system AI do nadmiernego rozpoznawania raka. Aby temu zapobiec, autorzy stosują technikę SMOTE do generowania dodatkowych syntetycznych przykładów dla niedoreprezentowanych klas, wyrównując rozkład treningowy. Dodają także warstwę wyjaśniającą przy użyciu Grad-CAM, która tworzy mapy cieplne pokazujące obszary obrazu mające największy wpływ na każdą decyzję. W przypadkach złośliwych podświetlane obszary zazwyczaj pokrywają się z nieregularnymi, promieniasto rozgałęzionymi guzkami; w przypadkach łagodnych lub prawidłowych uwaga przesuwa się na gładsze struktury tkanki. To pomaga radiologom zweryfikować, czy model patrzy na właściwe struktury, a nie na nieistotne artefakty.
Jak system radzi sobie na danych z praktyki klinicznej
Testowany na zbiorze danych IQ-OTH/NCCD dotyczącego raka płuca, proponowany ensemble osiąga imponującą skuteczność na poziomie około 99,4 procent, z równie wysoką precyzją, czułością i miarą F1. System konsekwentnie przewyższa każdą pojedynczą sieć, prostsze schematy fuzji oraz szereg innych metod optymalizacji. Co kluczowe, autorzy dodatkowo walidują model na osobnym, powszechnie używanym zbiorze CT znanym jako LIDC-IDRI, gdzie utrzymuje on niemal 98-procentową dokładność. Ten zewnętrzny test sugeruje, że system uogólnia się poza obrazy, na których był pierwotnie trenowany — istotny warunek dla narzędzia mającego wspierać klinicystów w różnych szpitalach i przy różnych ustawieniach skanerów.
Co to oznacza dla pacjentów i klinicystów
Dla laika najważniejszy wniosek jest taki, że łączenie kilku „ekspertów” AI, staranne dostrajanie ich współpracy i zwiększanie przejrzystości ich rozumowania może znacząco poprawić wczesne wykrywanie raka płuca na podstawie skanów TK. Ramy zaproponowane w tym artykule przekształcają surowe obrazy w wysoce dokładną, stosunkowo interpretowalną drugą opinię dla radiologów. Jeśli systemy takie zostaną dalej potwierdzone w badaniach klinicznych i zaadaptowane do codziennych procedur szpitalnych, mogą pomóc wykrywać niebezpieczne guzy wcześniej, ograniczyć niepotrzebne badania kontrolne i ostatecznie poprawić przeżywalność oraz jakość życia osób zagrożonych rakiem płuca.
Cytowanie: Al Duhayyim, M., Aldawsari, M.A., Ismail, A. et al. Interpretable hybrid ensemble with attention-based fusion and EAOO-GA optimization for lung cancer detection. Sci Rep 16, 8159 (2026). https://doi.org/10.1038/s41598-026-37187-6
Słowa kluczowe: wykrywanie raka płuca, analiza tomografii komputerowej, zbiór modeli głębokiego uczenia, Sztuczna inteligencja w obrazowaniu medycznym, wyjaśnialna diagnostyka