Clear Sky Science · pl
Integracyjne uczenie maszynowe i dokowanie molekularne ujawniają, że narirutyna celuje w ABCC1/ABCG2 w celu przebudowy mikrośrodowiska immunologicznego w raku jelita grubego
Związek z owoców z wielkimi nadziejami przeciw rakowi
Rak jelita grubego jest jednym z najgroźniejszych nowotworów na świecie, a wielu pacjentów nadal musi znosić ciężkie terapie i oporność na leki. W badaniu przyjrzano się narirutynie, naturalnej substancji występującej w owocach cytrusowych, żeby sprawdzić, czy może ona pomóc organizmowi walczyć z nowotworami okrężnicy w sposób łagodniejszy — poprzez zmianę sposobu, w jaki komórki nowotworowe radzą sobie z lekami, oraz zachowania komórek odpornościowych w otoczeniu guza.
Od owocu cytrusowego do celu przeciwnowotworowego
Naukowcy zaczęli od prostego pytania: gdyby narirutyna była lekarstwem, do których części naszych komórek by się wiązała? Korzystając z dużych publicznych baz danych onkologicznych i narzędzi predykcyjnych, przeskanowali tysiące genów z guzów jelita grubego i tkanki zdrowej. Następnie nałożyli te geny związane z rakiem z genami, na które narirutyna najprawdopodobniej wpływa. Spośród ponad 3 000 zmienionych genów w raku jelita grubego narirutyna została przewidziana jako znacząco oddziałująca z zaledwie dziewięcioma, a szczególnie z pięcioma „centralnymi” genami pełniącymi kluczowe funkcje wewnątrz komórek guza.
Kluczowi strażnicy na powierzchni komórek nowotworowych
Wśród tych genów centralnych wyróżniły się dwa: ABCC1 i ABCG2. Kodują one białka-pompy, które znajdują się w błonie zewnętrznej komórek i wypompowują leki na zewnątrz — jeden z powodów, dla których niektóre nowotwory stają się oporne na chemioterapię. Nowa analiza sugeruje, że narirutyna może wiązać się z tymi pompami i potencjalnie wpływać na ich działanie. Inne geny centralne, w tym CA12, EPHX2 oraz PTGS1, uczestniczą w regulacji równowagi kwasowo-zasadowej, metabolizmu lipidów i sygnałów zapalnych. Razem te geny pomagają określić, czy guz rośnie niekontrolowanie, jak reaguje na leki i jak oddziałuje z pobliską tkanką.
Symulowane wiązanie i rzeczywiste wyniki
Aby sprawdzić, czy narirutyna faktycznie może przylegać do tych białek-docelowych, zespół wykorzystał dokowanie molekularne — wysokorozdzielcze modele komputerowe przewidujące, jak mała cząsteczka mieści się w większym białku. Symulacje wykazały, że narirutyna dobrze dopasowuje się do kieszeni na białkach docelowych i tworzy stabilne interakcje, co oznacza, że wiązanie jest fizycznie możliwe. Analiza danych pacjentów pokazała, że geny centralne wyraźnie odróżniają tkankę nowotworową od normalnej i korelują z przeżyciem chorych. Na przykład wyższe poziomy ABCC1 i PTGS1 wiązały się z gorszymi wynikami, co sugeruje, że obniżenie aktywności tych genów — potencjalnie za pomocą związków takich jak narirutyna — mogłoby przynieść korzyści.
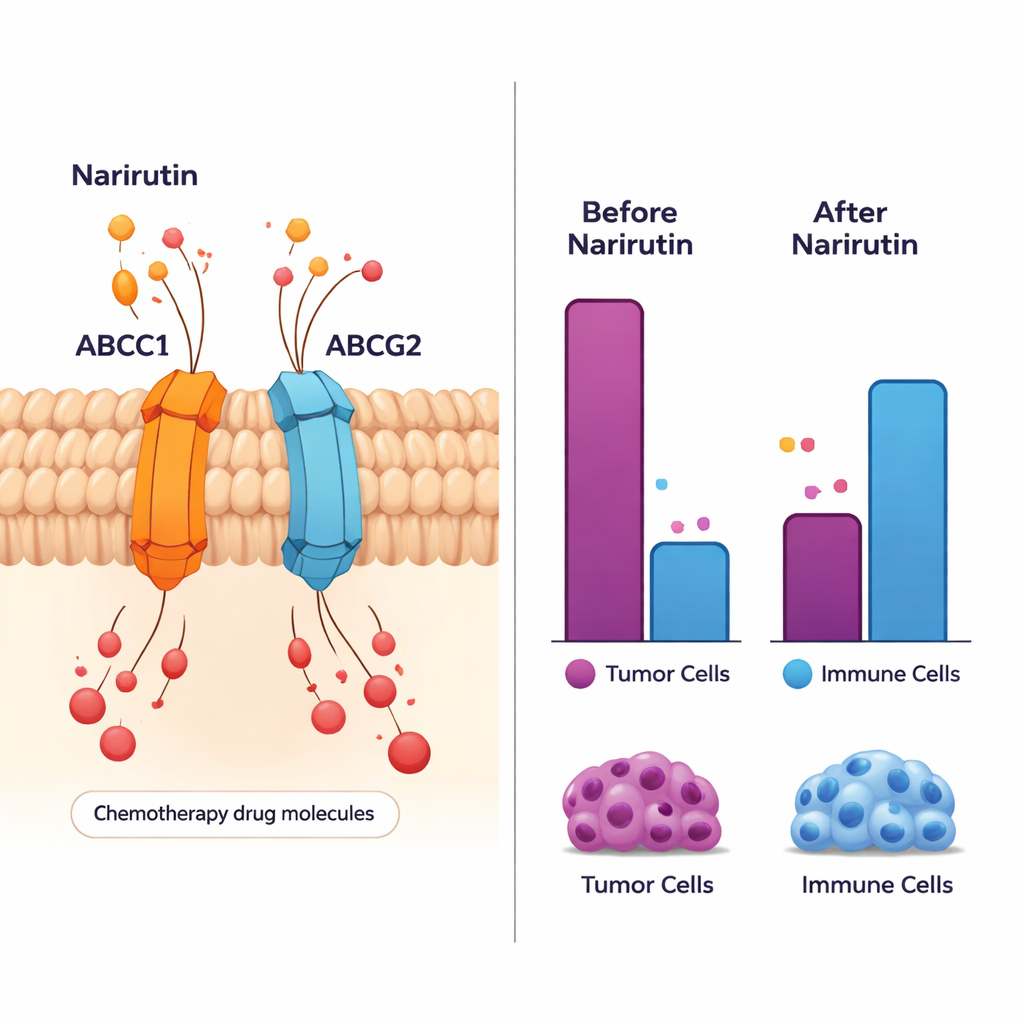
Przebudowa „sąsiedztwa” immunologicznego guza
Nowotwór nie rozwija się w izolacji; funkcjonuje w złożonym „sąsiedztwie” komórek odpornościowych, naczyń krwionośnych i tkanki podporowej. Badanie przeanalizowało 28 różnych typów komórek odpornościowych wokół guzów jelita grubego i wykryło szerokie przesunięcia w porównaniu z tkanką zdrową. Niektóre pomocne komórki odpornościowe, takie jak aktywowane komórki B i określone komórki T, były bardziej liczne lub zachowywały się inaczej w guzie. Główne cele narirutyny, zwłaszcza ABCC1, ABCG2 i PTGS1, wykazywały silne powiązania z tymi zmianami immunologicznymi. Sugeruje to, że działając na te geny, narirutyna może nie tylko wpływać bezpośrednio na komórki nowotworowe, lecz także modulować lokalną odpowiedź immunologiczną — potencjalnie czyniąc środowisko mniej sprzyjającym wzrostowi guza.
Nadzieje, ale wciąż dużo pracy do wykonania
Mówiąc prosto, badanie proponuje, że naturalny flawonoid z cytrusów mógłby „zatkać pompy”, których komórki nowotworowe używają do unikania chemioterapii, oraz pomóc zresetować immunologiczne otoczenie guzów jelita grubego. Praca opiera się na zaawansowanych analizach komputerowych i dużych zestawach genetycznych, a nie na badaniach laboratoryjnych czy klinicznych, więc stanowi wczesny, lecz ważny krok. Jeśli przyszłe eksperymenty na komórkach, zwierzętach i pacjentach potwierdzą te przewidywania, narirutyna — lub leki inspirowane nią — mogłyby w przyszłości stać się częścią terapii kombinowanych, które uczynią standardowe leczenie raka jelita grubego bardziej skutecznym i mniej podatnym na oporność.
Cytowanie: Bian, R., Wang, H., Zhang, H. et al. Integrative machine learning and molecular docking reveal Narirutin targets ABCC1/ABCG2 for immune microenvironment remodeling in colorectal cancer. Sci Rep 16, 7649 (2026). https://doi.org/10.1038/s41598-026-37181-y
Słowa kluczowe: rak jelita grubego, narirutyna, oporność na leki, mikrośrodowisko guza, modulacja immunologiczna