Clear Sky Science · pl
Badania przesiewowe obejmujące cały genom identyfikują głównych regulatorów ekspresji powierzchniowego białka prionowego
Dlaczego to ma znaczenie dla zdrowia mózgu
Choroby prionowe, takie jak choroba Creutzfeldta–Jakoba u ludzi czy tzw. „choroba szalonych krów” u bydła, są rzadkie, ale zawsze śmiertelne. Głównym sprawcą jest normalne białko mózgowe, zwane białkiem prionowym, które może przyjmować nieprawidłową konformację i szerzyć uszkodzenia między komórkami. Im więcej tego białka znajduje się na powierzchni komórek nerwowych, tym łatwiej choroba może się rozwinąć. W tym badaniu celem było zmapowanie, w całym genomie, które geny kontrolują, ile białka prionowego pojawia się na zewnętrznej stronie komórek przypominających neurony. Taka mapa może pomóc naukowcom w opracowaniu nowych sposobów obniżania poziomu tego białka i potencjalnie spowolnienia różnych chorób neurodegeneracyjnych.
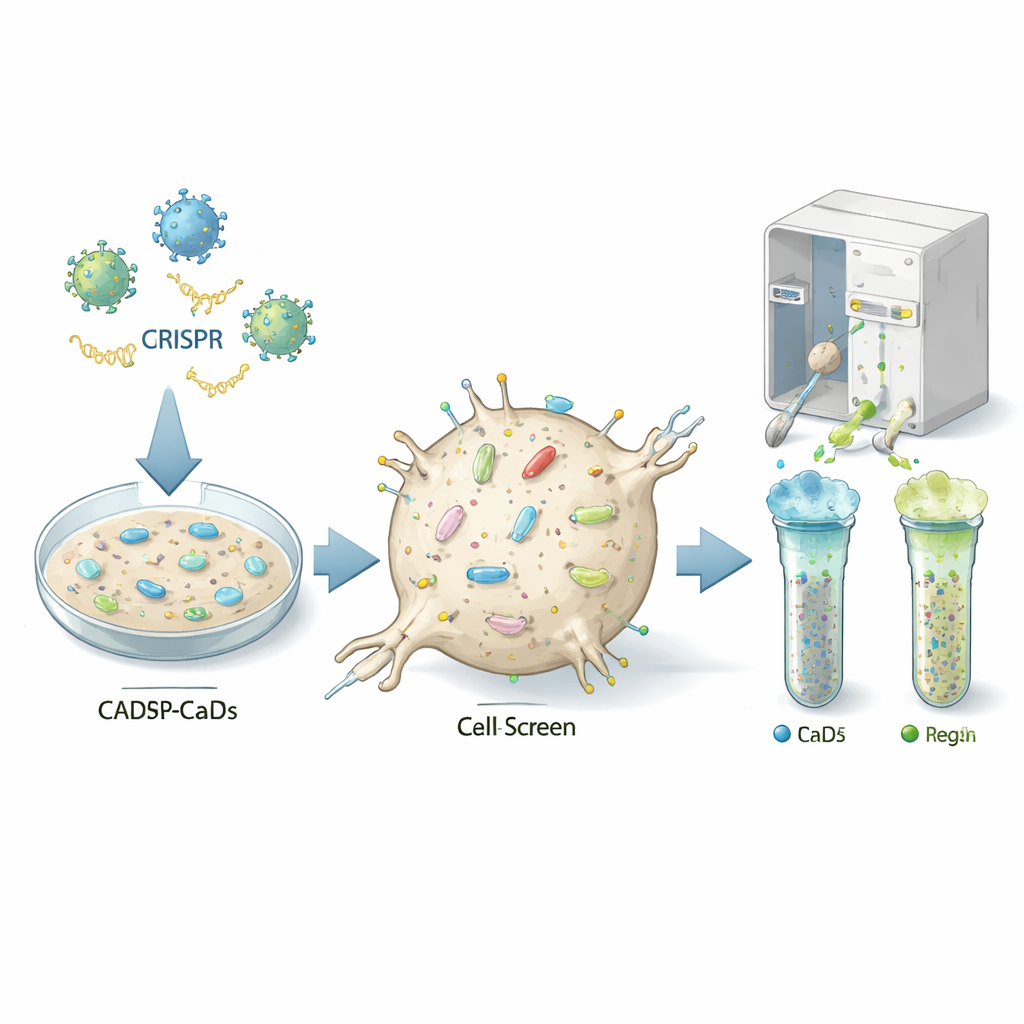
Znajdowanie pokręteł regulacyjnych komórki
Autorzy zastosowali potężne narzędzie edycji genów zwane CRISPR, aby wyłączać niemal każdy gen po kolei w linii komórkowej mysiopodobnej neuronów podatnej na zakażenie prionami (zwanej komórkami CAD5). Każda komórka otrzymała inne „uderzenie” genetyczne, więc populacja zawierała miliony wariantów, z których każdy pozbawiony był konkretnego genu. Następnie zabarwiono komórki przeciwciałami fluorescencyjnymi rozpoznającymi normalne białko prionowe na powierzchni i użyto sortera komórek, by oddzielić komórki o nietypowo niskich lub wysokich poziomach tego białka. Sekwencjonując, które prowadzące RNA (guide RNA) były wzbogacone w grupach z niskim lub wysokim poziomem, badacze mogli wnioskować, które wyłączone geny normalnie działają jak włączniki lub wyłączniki dla obecności białka prionowego na powierzchni komórki.
Dwa stany komórek, pokrywające się odpowiedzi
Neurony nie są identyczne w ciągu życia, więc naukowcy sprawdzili, czy te same geny kontrolują białko prionowe w różnych stanach komórkowych. Komórki CAD5 można utrzymywać w szybko dzielącym się, mniej wyspecjalizowanym stanie lub - przez usunięcie surowicy z medium hodowlanego - skłonić je do przyjęcia bardziej dojrzałej, neuronopodobnej postaci. Zespół przeprowadził to samo przesiewowe badanie CRISPR w obu warunkach. W komórkach niedojrzałych potwierdzili 46 genów, które zwiększają, oraz 21, które zmniejszają powierzchniowy poziom białka prionowego, gdy są obecne. W komórkach zróżnicowanych (bardziej neuronopodobnych) potwierdzono 41 regulatorów dodatnich i 13 ujemnych. Dwudziesty trzy geny — głównie te zaangażowane w przyłączanie lipidowej „kotwicy” do białka — były wspólne dla obu stanów komórkowych, co podkreśla istnienie podstawowego mechanizmu regulacyjnego działającego niezależnie od dojrzałości.
Kluczowe „linie montażowe”, które mają największe znaczenie
Dalsza analiza wykazała, że wiele nowo zidentyfikowanych genów należy do znanych komórkowych „linii montażowych”, które modyfikują białka w miarę ich podróży na powierzchnię komórki. Jedna główna ścieżka buduje kotwicę GPI, małą bogatą w lipidy strukturę, która przytwierdza białko prionowe do zewnętrznej warstwy błony komórkowej. Zakłócenie prawie dowolnego etapu tej ścieżki zmniejszało ilość białka prionowego docierającego na powierzchnię zarówno w komórkach niedojrzałych, jak i dojrzałych. Druga ścieżka dotyczy glikozylacji N-łączonej, w której złożone łańcuchy cukrowe są dodawane do białek podczas przechodzenia przez wewnętrzne błony komórkowe. Geny z tej ścieżki dodającej cukry ujawniły się głównie jako istotne w komórkach mniej dojrzałych. Gdy badacze zastosowali małe cząsteczki blokujące konkretne etapy glikozylacji, poziomy powierzchniowego białka prionowego spadły o około jedną trzecią, nie zabijając przy tym komórek, co potwierdziło wyniki genetyczne.
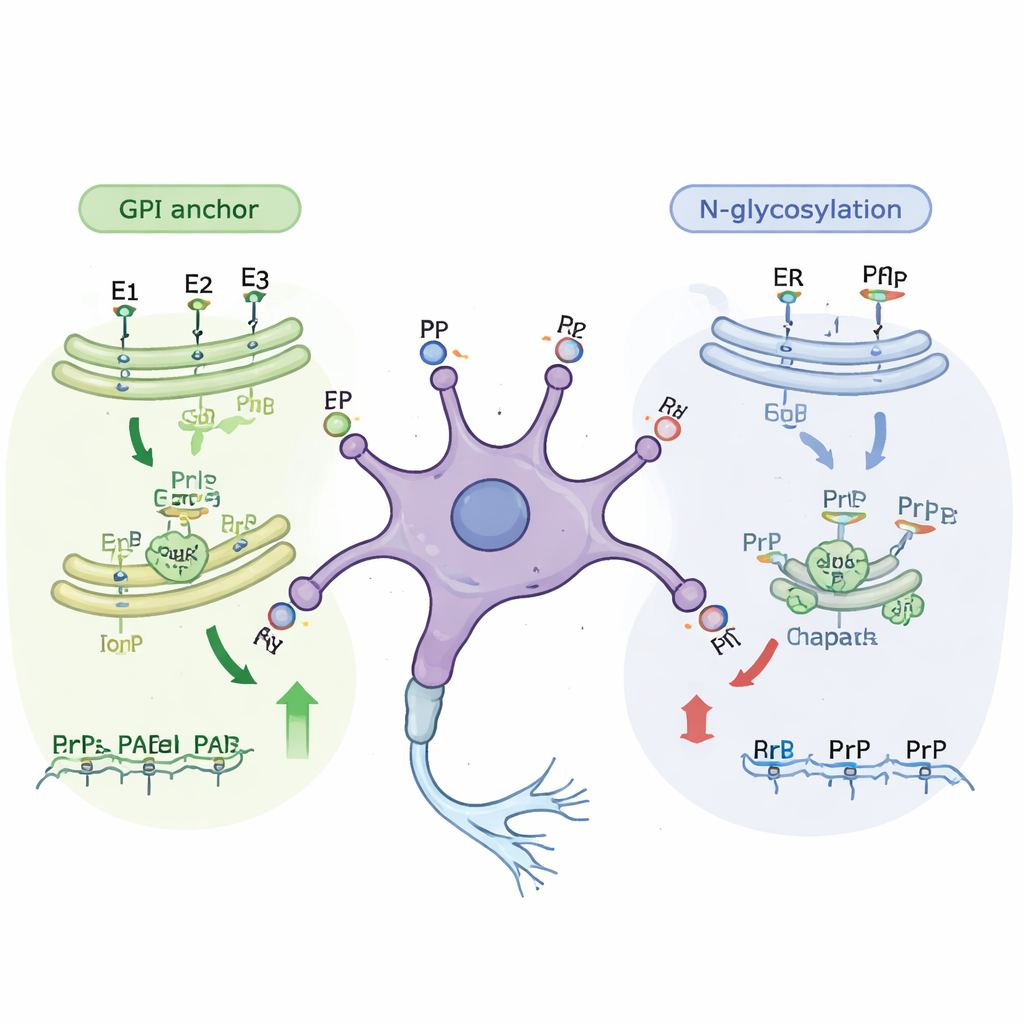
Pomocnicze białka i odpowiedzi na stres
Przesiewy wyróżniły także molekularne chaperony — białka pomagające innym białkom prawidłowo się fałdować — jako ważnych regulatorów prionu. W szczególności Hspa5 (znany także jako BiP), centralny chaperon w komórkowym przedziale odpowiedzialnym za fałdowanie białek, okazał się regulatorem dodatnim w bardziej neuronopodobnych komórkach. Gdy badacze zastosowali lek hamujący Hspa5, poziomy powierzchniowego białka prionowego spadły w obu stanach komórkowych, ponownie bez wyraźnych szkód dla komórek. Inne trafienia obejmowały geny zaangażowane w przemieszczanie białek przez komórkę, kontrolę włączania i wyłączania genów oraz kilka białek związanych z funkcją synaps i innymi chorobami mózgu, takimi jak Alzheimer czy ALS. Razem wyniki te pokazują, że poziomy białka prionowego na powierzchni komórki są kształtowane przez sieć ścieżek obejmujących produkcję, modyfikację, transport i kontrolę jakości białek.
Co to oznacza dla przyszłych terapii
To badanie dostarcza pierwszego kompleksowego katalogu genów kontrolujących ilość białka prionowego pojawiającego się na powierzchni komórek neuronopodobnych podatnych na zakażenie prionami. Niektóre z tych genów, zwłaszcza te z ścieżek kotwicy GPI i N-glikozylacji oraz systemu chaperonowego Hspa5, wydają się obiecującymi punktami wyjścia do odkrywania leków: osłabienie ich aktywności powinno zmniejszyć ilość białka prionowego podatnego na nieprawidłowe fałdowanie, a wcześniejsze badania pokazują, że nawet częściowe redukcje mogą znacząco opóźnić rozwój choroby u zwierząt. Równocześnie wyraźne różnice między komórkami niedojrzałymi i dojrzałymi podkreślają, że stan komórki mózgowej ma znaczenie przy wyborze celów. Choć potrzeba dalszych badań, by sprawdzić, jak manipulowanie tymi genami wpływa na rzeczywiste zakażenie prionami i inne schorzenia neurodegeneracyjne w żywych mózgach, to badanie oferuje mapę dźwigni komórkowych, które naukowcy mogą badać, aby spowolnić lub zapobiec tym wyniszczającym chorobom.
Cytowanie: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Słowa kluczowe: białko prionowe, badanie CRISPR, neurodegeneracja, glikozylacja białek, kotwica GPI