Clear Sky Science · pl
Wzmocnione ciśnieniem chłodzenie ultra-szybkie na dwóch stałych powierzchniach poprawia regenerację po odmrożeniu hepatocytów i precyzyjnie ciętych plastrów wątroby
Dlaczego zamrażanie tkanki wątroby ma znaczenie
Utrzymanie komórek i tkanek przy życiu poza organizmem to jedno z cichych osiągnięć współczesnej medycyny. Zamrożone komórki wątroby pomagają badaczom testować nowe leki, modelować choroby i być może pewnego dnia naprawiać niewydolne organy. Jednak zamrażanie żywej tkanki jest skomplikowane: jeśli kryształy lodu zaczną rosnąć wewnątrz lub między komórkami, niszczą delikatne struktury. W tym badaniu analizuje się nowy sposób zamrażania komórek wątroby i cienkich plastrów wątroby tak szybko i w tak kontrolowanych warunkach, że powstawanie uszkadzających kryształów lodu jest zminimalizowane.
Problem lodu i chemicznych ochroniarzy
Konwencjonalna krioprezerwacja opiera się na dwóch niedoskonałych narzędziach: zimnie i związkach chemicznych. W miarę ochładzania próbki woda ma tendencję do zamarzania, co może przebić błony i zakłócić strukturę tkanek. Aby temu przeciwdziałać, naukowcy dodają środki ochrony kriogenicznej, takie jak dimetylosulfotlenek (DMSO), które pomagają wodzie przejść w stan szklisty zamiast tworzyć kryształy lodu. Jednak przy wysokich stężeniach stosowanych rutynowo te środki same w sobie mogą być toksyczne dla komórek albo powodować szkodliwe pęcznienie i kurczenie się w miarę ich przemieszczania się do wnętrza tkanki i z powrotem. Celem autorów było zmniejszenie ilości DMSO potrzebnej do uniknięcia lodu, przy jednoczesnym zachowaniu bezpieczeństwa i praktyczności przechowywania komórek i tkanek wątroby.
Nowy sposób jednoczesnego ściskania i chłodzenia
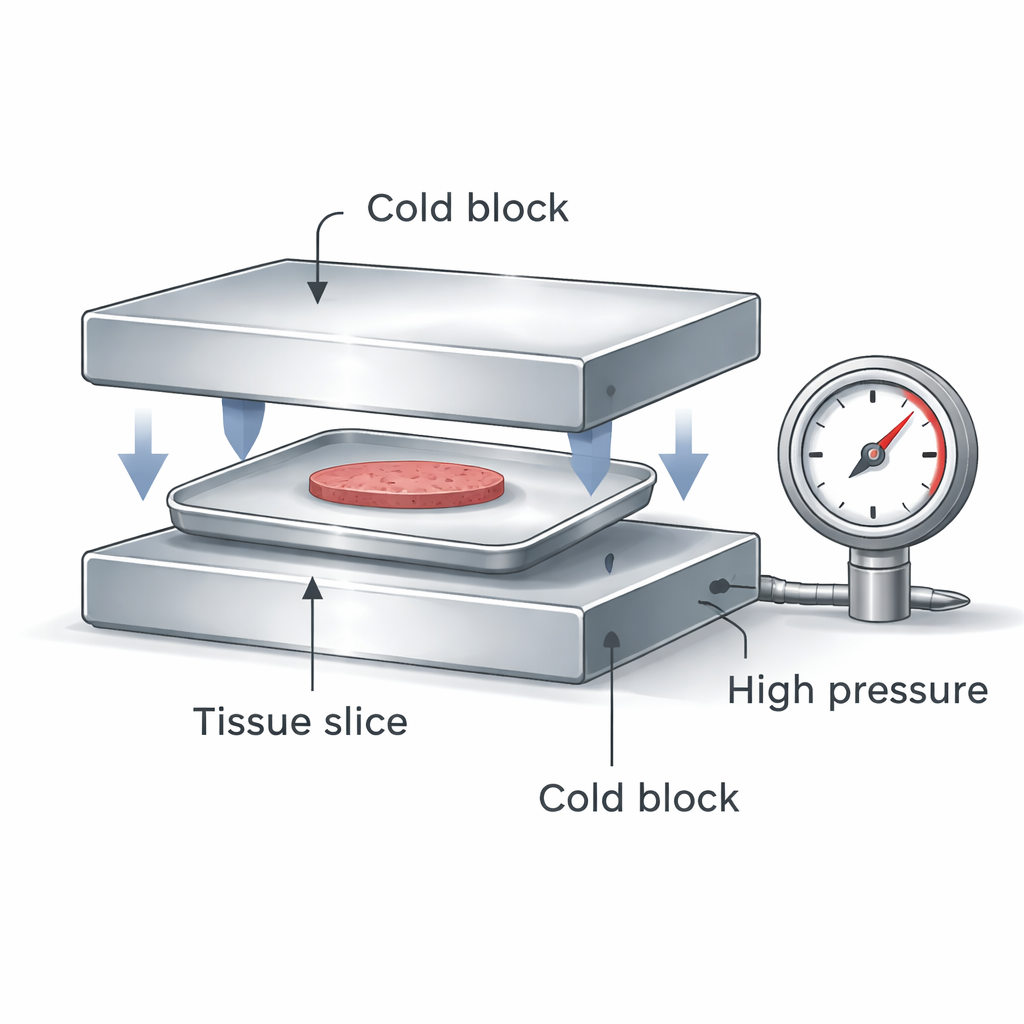
Zespół zaprojektował kompaktowe urządzenie, które umieszcza szczelny, płaski aluminiowy pojemnik z komórkami wątroby lub precyzyjnie ciętymi plastrami między dwoma ekstremalnie zimnymi metalowymi blokami. Gdy bloki się dociskają, dzieją się dwie ważne rzeczy jednocześnie: w szczelnym pojemniku powstaje wysokie ciśnienie, a próbka jest schładzana z góry i z dołu. Wysokie ciśnienie zmienia zachowanie wody tak, że lód tworzy się w niższych temperaturach, a roztwór łatwiej przechodzi w stan szklisty. Kontakt z obu stron daje znacznie szybsze i bardziej jednorodne tempo chłodzenia niż zwykłe zanurzenie plastikowej fiolki w ciekłym azocie, a szczelny pojemnik izoluje próbkę od zanieczyszczeń.
Poszukiwanie optymalnego punktu dla bezpieczeństwa i przeżywalności
Aby sprawdzić, czy podejście jest wystarczająco łagodne dla żywych materiałów, badacze najpierw upewnili się, że sam aluminiowy pojemnik nie szkodzi komórkom pochodzącym z wątroby HepG2 podczas krótkich czasów manipulacji. Przeżywalność komórek pozostała w zasadzie niezmieniona. Następnie eksponowali te komórki na różne poziomy DMSO przed zamrożeniem i potwierdzili znany kompromis: więcej DMSO lepiej hamuje powstawanie lodu, ale staje się wyraźnie toksyczne przy 30%, podczas gdy 20% pozostaje w dużej mierze tolerowalne. Dla mysich plastrów wątroby sprawdzili, ile ciśnienia tkanka może wytrzymać bez zamrażania. Krótkie impulsy do 150 megapaskali miały niewielki wpływ na przeżywalność, ale 200 megapaskali spowodowało około 30% spadek, wyznaczając górną granicę bezpiecznego działania.
Lepiej zachowane plastry wątroby po odmrożeniu
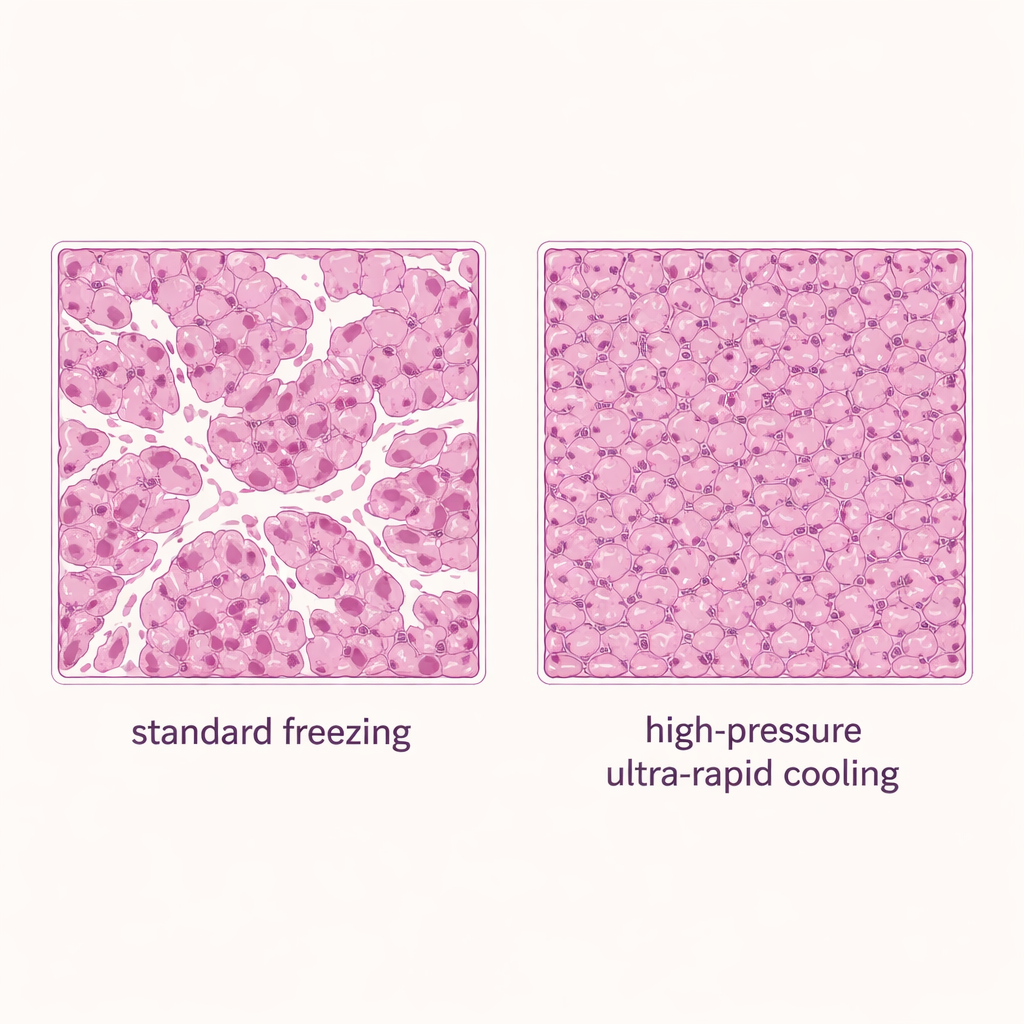
Po ustaleniu bezpiecznych zakresów autorzy porównali trzy metody zamrażania plastrów wątroby: standardowe zanurzenie szczelnego pojemnika w ciekłym azocie (podejście konwekcyjne, oparte na płynie), chłodzenie na stałej powierzchni bez dodatkowego ciśnienia oraz chłodzenie na stałej powierzchni przy wysokim ciśnieniu 150 megapaskali. Wszystkie grupy używały 20% DMSO. Metoda wspomagana ciśnieniem przyniosła najlepsze wyniki: zachowano około 80% pierwotnej żywotności tkanki, co przewyższało zarówno standardowe zamrażanie, jak i samo chłodzenie na stałej powierzchni. Mikroskopia barwionych plastrów tkanek potwierdziła te obserwacje. Próbki zamrożone metodą konwencjonalnego zanurzenia wykazywały wiele otwartych białych przestrzeni — oznak uszkodzeń przez lód — podczas gdy chłodzenie na stałej powierzchni z wysokim ciśnieniem dało gęstszą, bardziej nienaruszoną tkankę z znacznie mniejszą liczbą szczelin.
Co to oznacza dla przyszłego przechowywania tkanek
Ogólnie rzecz biorąc, badanie pokazuje, że ściskanie szczelnie zapakowanego plastra wątroby w aluminiowej obudowie między dwoma ultrazimnymi blokami przy starannie kontrolowanym wysokim ciśnieniu może znacznie poprawić przeżywalność tkanki po odmrożeniu. Poprzez połączenie szybszego, bardziej równomiernego chłodzenia ze zmianą zachowania wody pod wpływem ciśnienia, metoda ogranicza wzrost uszkadzającego lodu przy jednoczesnym zastosowaniu umiarkowanego, klinicznie znanego stężenia DMSO. Dla czytelnika niebędącego specjalistą wniosek jest taki, że sprytniejsze inżynieryjne rozwiązania — sposób pakowania i chłodzenia tkanki — mogą być równie ważne jak stosowane chemikalia. To dwustronne, wysokociśnieniowe podejście może stać się krokiem w kierunku bezpieczniejszego, bardziej niezawodnego przechowywania tkanek wątroby, a ostatecznie także innych organów do badań i terapii.
Cytowanie: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Słowa kluczowe: krioprezerwacja, tkanka wątrobowa, witrifikacja, chłodzenie pod wysokim ciśnieniem, mrożenie bez tworzenia lodu