Clear Sky Science · pl
DANEELpath otwarte narzędzia do cyfrowej analizy do badań histopatologicznych w modelach neuroblastomy
Dlaczego małe guzy w żelu mają znaczenie
Nowotwór to nie tylko masa zbuntowanych komórek; to całe sąsiedztwo, w którym komórki komunikują się między sobą i ze strukturą wspierającą je na zewnątrz. W nowotworach wieku dziecięcego, takich jak neuroblastoma, ta otaczająca struktura wspierająca może sprzyjać wzrostowi guza i oporności na leczenie. W pracy tej przedstawiono DANEELpath — darmowy, otwartoźródłowy zestaw narzędzi cyfrowych, który zamienia obrazy mikroskopowe hodowanych w laboratorium mini-guzów w bogate, ilościowe mapy. Dzięki temu pomaga naukowcom zrozumieć, jak komórki guza się układają, jak reagują na testowane leki i jak te obserwacje mogą przełożyć się na lepsze terapie dla dzieci.
Tworzenie małych światów guzów w laboratorium
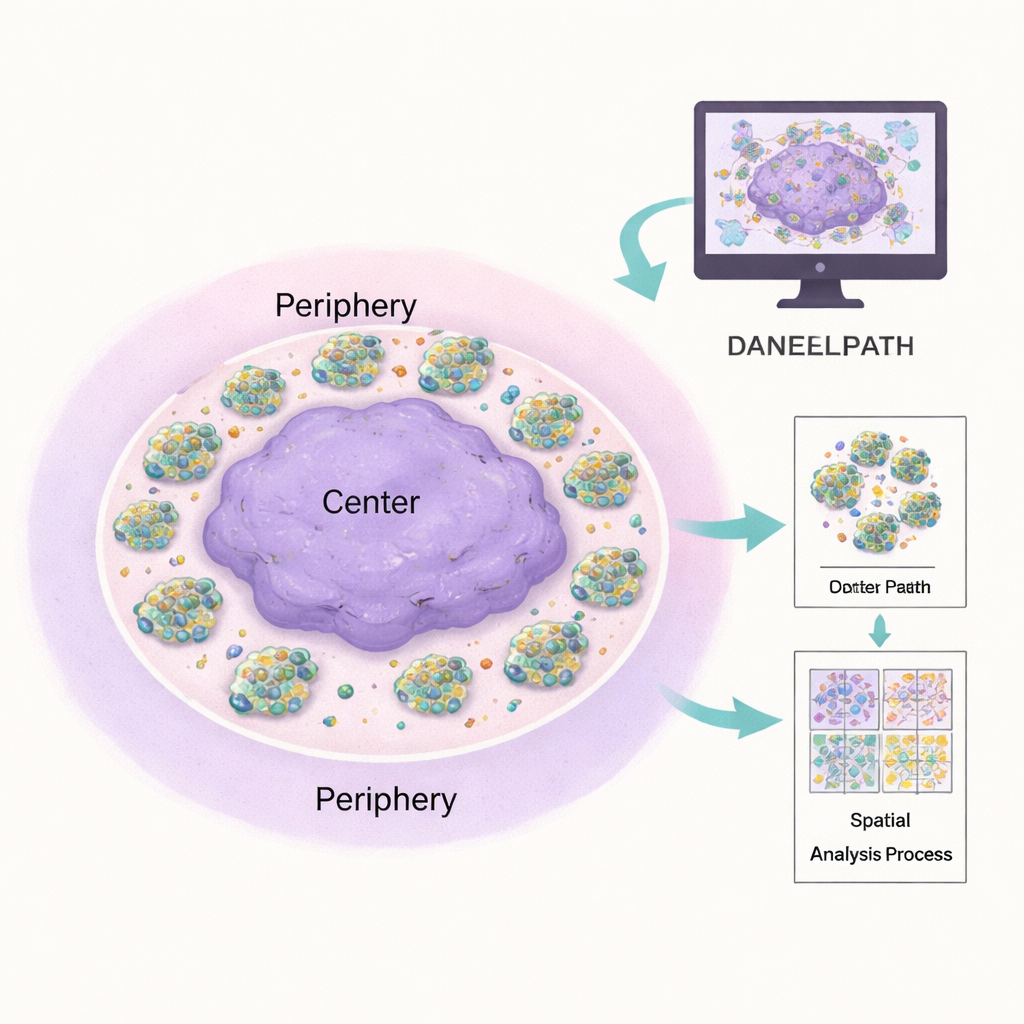
Aby naśladować złożone środowisko prawdziwego guza, badacze hodują komórki neuroblastomy wewnątrz miękkich żeli 3D z żelatyny i jedwabiu. W tym środowisku komórki naturalnie tworzą kuliste skupiska, podobne do mini-guzów. Kluczową rolę odgrywa witronektyna — klejące białko w macierzy zewnątrzkomórkowej, które ułatwia przyleganie komórek i może napędzać bardziej agresywny przebieg choroby. Zespół przygotował żele z dodatkiem witronektyny i bez niej oraz wystawił niektóre próbki na działanie cilengitidu, eksperymentalnego leku blokującego receptory związane z witronektyną. Po tygodniach wzrostu żele zostały pocięte, zabarwione i zeskanowane jako wysokorozdzielcze obrazy całych preparatów, tworząc cyfrową wersję każdego mini-świata guza.
Zmiana złożonych obrazów w miarodajne wzorce
Tradycyjna patologia opiera się na eksperckim oku przy mikroskopie — to potężne podejście, ale trudne do ujednolicenia i skalowania. DANEELpath integruje się z popularną, otwartoźródłową platformą QuPath i automatyzuje dużą część tej pracy. Wykorzystując modele głębokiego uczenia zwane U-Netami, pakiet potrafi dokładnie wyznaczać kontury każdego skupiska komórek na powszechnych barwieniach, nawet gdy skupiska mają od kilku do setek komórek. Następnie stosuje metody matematyczne, by podzielić nieregularnie ukształtowany hydrożel na zrównoważony „środek” i pierścień „obwodu”, co zapewnia uczciwe porównania między wewnętrznymi a zewnętrznymi obszarami niezależnie od kształtu żelu. Dzięki temu autorzy potwierdzili, że skupiska neuroblastomy mają tendencję do większego zagęszczenia w kierunku krawędzi hydrożelu i że ten wzór zmienia się w zależności od zawartości witronektyny i leczenia lekiem.
Pomiary odstępów między komórkami i sąsiedztwa skupisk
Ponad zwykłym zliczaniem skupisk, DANEELpath analizuje, jak komórki i skupiska układają się w przestrzeni. W obrębie każdego skupiska inne narzędzie wykrywa pojedyncze jądra komórkowe i mierzy odległość od najbliższego sąsiada, podsumowując, jak ciasno upakowane są komórki. Pomiędzy skupiskami pakiet oferuje trzy sposoby definiowania „sąsiadów”, w tym metodę opartą na diagramach Voronoi, która rysuje strefy wpływu wokół każdego skupiska. Porównując te miary w różnych warunkach, badacze wykazali, że cilengitid zmienia liczbę sąsiednich skupisk dużego skupiska i sposób ich rozmieszczenia, ale w sposób zależny od tego, czy w żelu dodano witronektynę. To podkreśla, jak macierz otaczająca i leki mechaniczne razem kształtują organizację guza.
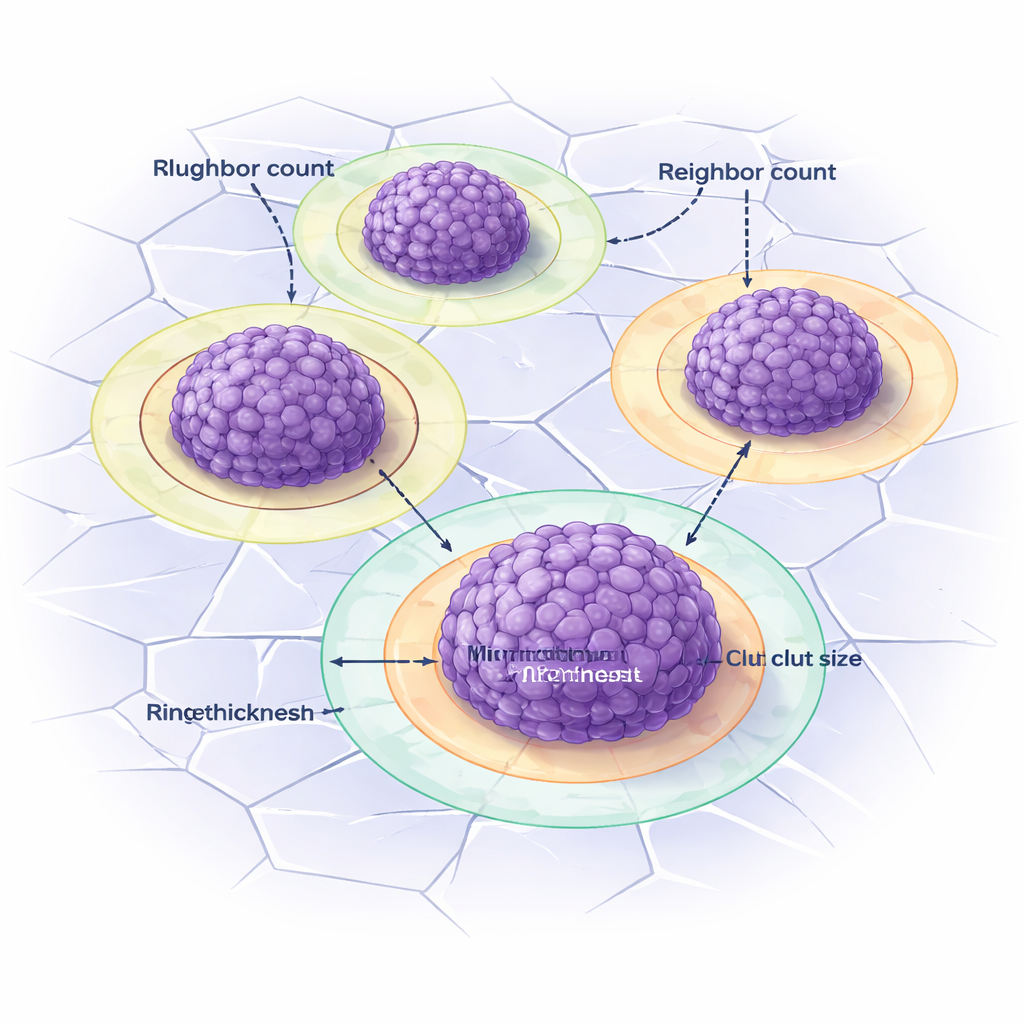
Widzenie halo wokół skupisk guzów
Witronektyna w tych modelach często tworzy uderzające pierścienie wokół skupisk: jasną „koronę”, gdy obecna jest tylko witronektyna produkowana przez komórki, oraz bladą otoczkę, gdy dodatkowa witronektyna jest wbudowana w żel. Oddzielenie tych pierścieni od jądra skupiska jest trudne gołym okiem. DANEELpath rozwiązuje to, rysując najpierw regiony wpływu oparte na Voronoi wokół każdego skupiska, a następnie rozszerzając je na zewnątrz tylko na tyle, by uchwycić pierścień bez nakładania się na sąsiadów. Proste reguły kontrastu obrazu służą do wykrywania koron i otoczek, a narzędzie automatycznie mierzy ich grubość. Podobne strategie zastosowano także do rzeczywistych próbek pacjentów, na przykład mapując komórki odpornościowe na krawędzi obszarów guza lub definiując strefy wokół naczyń krwionośnych, aby badać, jak witronektyna i inne markery układają się w ludzkiej neuroblastomie.
Co to oznacza dla przyszłych badań nad rakiem
W istocie ta praca przekształca statyczne obrazy patomorfologiczne w szczegółowe, powtarzalne pomiary organizacji komórek guza i ich otoczenia. Dla osób spoza specjalności oznacza to, że badacze mogą teraz łatwiej testować, jak nowe leki, materiały rusztowania czy zmiany genetyczne wpływają nie tylko na to, czy guzy rosną, ale jak rosną w przestrzeni. Ponieważ DANEELpath jest otwartoźródłowy, działa przez interfejs graficzny i uruchamia się na zwykłych komputerach, obniża barierę wejścia dla laboratoriów na całym świecie, które chcą przyjąć zaawansowaną analizę obrazów. Z czasem takie narzędzia mogą pomóc łączyć wzorce widziane w modelach 3D i tkankach pacjentów z wynikami klinicznymi, prowadząc do bardziej ukierunkowanych i skutecznych terapii dla dzieci z wysokiego ryzyka neuroblastomą.
Cytowanie: Vieco-Martí, I., López-Carrasco, A., Navarro, S. et al. DANEELpath open source digital analysis tools for histopathological research in neuroblastoma models. Sci Rep 16, 6162 (2026). https://doi.org/10.1038/s41598-026-37134-5
Słowa kluczowe: neuroblastoma, cyfrowa patología, żele 3D, matryca zewnątrzkomórkowa, uczenie głębokie