Clear Sky Science · pl
Powiązane ze starzeniem LncRNA TRMP i TRMP-S promują raka żołądka przez aktywację IGFL4
Dlaczego to badanie ma znaczenie
Rak żołądka pozostaje jednym z najgroźniejszych nowotworów na świecie, głównie dlatego, że często wykrywany jest późno i bywa trudny w leczeniu. To badanie ujawnia, w jaki sposób dwa słabo poznane cząsteczki genetyczne, TRMP i TRMP-S, wspierają wzrost i rozprzestrzenianie się guzów żołądka. Pokazując łańcuch zdarzeń, które wywołują wewnątrz komórek nowotworowych oraz w immunologicznym otoczeniu guza, praca ta wskazuje nowe drogi, które mogą w przyszłości pomóc wcześniej diagnozować pacjentów i projektować skuteczniejsze, ukierunkowane terapie.
Ukryte komunikaty w naszym DNA
Większość ludzi myśli o genach jako o planach budowy białek, ale nasze DNA produkuje też długie RNA niekodujące (lncRNA), które nie kodują białek, a mimo to silnie wpływają na zachowanie komórek. TRMP i jego krótszy wariant splice’owy TRMP-S to dwa takie lncRNA. Wcześniej łączono je ze starzeniem i kontrolą cyklu komórkowego w komórkach płuc i jelita grubego, lecz ich rola w raku żołądka była nieznana. Ponieważ lncRNA mogą służyć jako markery diagnostyczne i cele terapeutyczne, autorzy postanowili ustalić, czy TRMP i TRMP-S promują przemianę komórek żołądka w komórki nowotworowe i w jaki sposób wchodzą w interakcje z innymi molekułami.
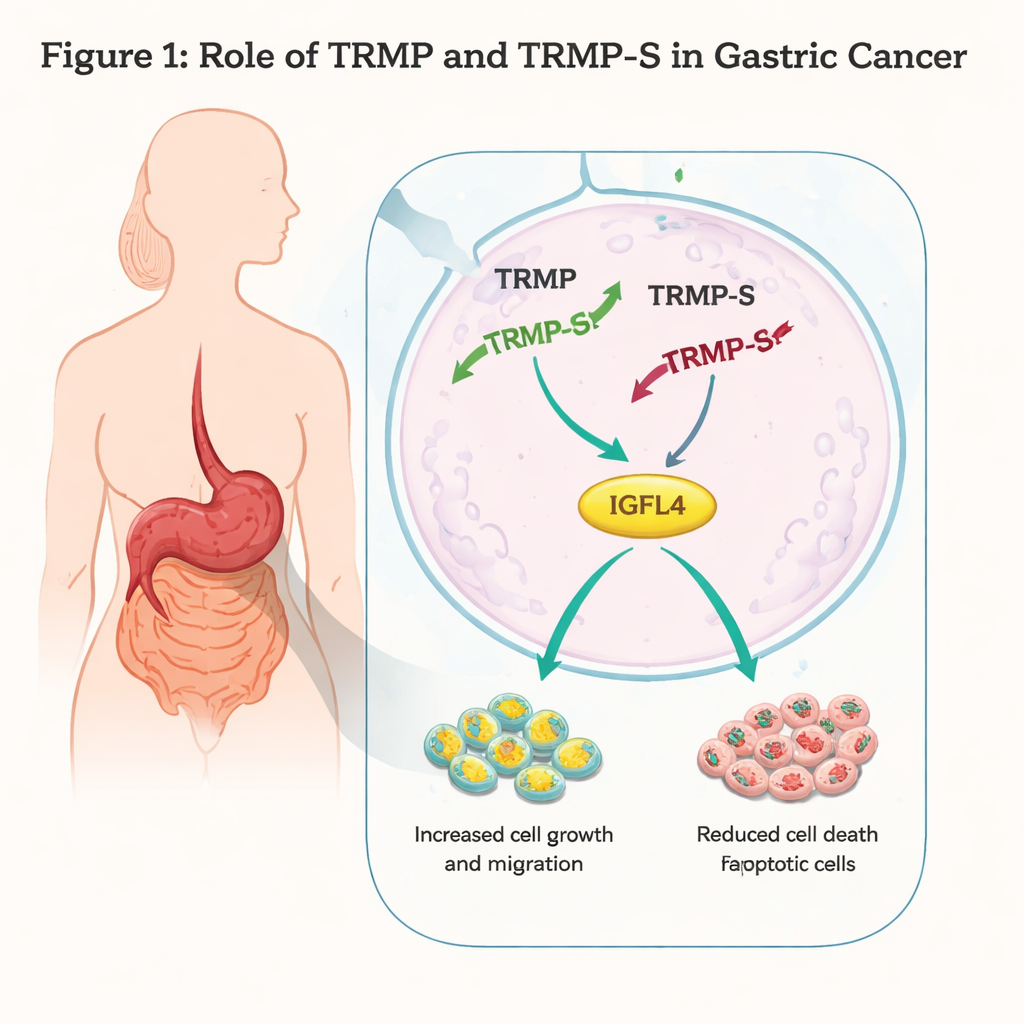
Wyłączanie akceleratora nowotworu
Naukowcy pracowali na dwóch ludzkich liniach komórkowych raka żołądka, AGS i MKN45, i użyli narzędzi genetycznych do zmniejszenia poziomów TRMP-S i TRMP. Gdy uciszono TRMP-S, komórki nowotworowe rosły wolniej, tworzyły mniej kolonii i miały mniejszą zdolność do migracji przez sztuczne bariery lub zamykania „ran” w hodowli. Cytometria przepływowa i analizy białkowe wykazały, że więcej komórek przechodziło zaprogramowaną śmierć (apoptozę) oraz że cykl komórkowy zatrzymywał się w fazie G1 — kluczowym „punkcie kontrolnym” przed replikacją DNA. Poziomy p73, członka rodziny supresorów guza p53, rosły po utracie TRMP-S, co zgadza się z silniejszą kontrolą cyklu komórkowego i większą liczbą zgonów komórek. Wyniki te razem wskazują, że TRMP-S zwykle działa jak pedał przyspieszenia dla komórek raka żołądka.
Kluczowy partner: sygnał IGFL4
Aby zrozumieć, jak TRMP i TRMP-S wywołują swoje efekty, zespół przeanalizował obszerne bazy danych pacjentów z The Cancer Genome Atlas oraz koreańską kohortę raka żołądka. Szukano genów jednocześnie nadmiernie aktywnych w guzach i pozytywnie skorelowanych z poziomami TRMP, a następnie zbudowano sześciogenowy „model ryzyka” przewidujący przeżycie pacjentów — wyższe wyniki wiązały się z gorszym rokowaniem. Wśród tych genów wyróżnił się IGFL4, członek rodziny powiązanej z insulinopodobnymi czynnikami wzrostu, które są znane z napędzania wzrostu i przeżycia w wielu nowotworach. W komórkach raka żołądka zredukowanie TRMP-S wyraźnie obniżało poziomy RNA i białka IGFL4, a test immunoprecypitacji RNA wykazał, że zarówno TRMP, jak i TRMP-S fizycznie wiążą białko IGFL4. Bezpośrednie zmniejszenie TRMP przyniosło ten sam efekt tłumienia IGFL4, co sugeruje, że te lncRNA pomagają stabilizować lub wspierać produkcję tego sygnału promującego wzrost.
Spowalnianie rozprzestrzeniania i przekształcanie scenerii immunologicznej
Gdy badacze zastosowali małe interferujące RNA do uciszenia samego IGFL4, komórki raka żołądka zwolniły wzrost, mniej migrowały oraz miały słabszą zdolność do inwazji przez błony i zamykania ran. Analiza danych pacjentów wykazała, że poziomy IGFL4 były istotnie wyższe w guzach żołądka niż w normalnej tkance żołądka i podwyższone także w wielu innych typach nowotworów. Co ważne, guzy o wysokiej ekspresji IGFL4 wykazywały charakterystyczne wzorce nacieku komórek odpornościowych: więcej niedojrzałych makrofagów (M0) i mniej komórek plazmatycznych, monocytów, eozynofilów i neutrofili. Obliczeniowe oceny immunologiczne sugerowały, że guzy z wysokim IGFL4 mogą lepiej odpowiadać na nowoczesne immunoterapie blokujące punkty kontrolne odporności, co wskazuje, że IGFL4 mogłoby pomóc identyfikować pacjentów będących dobrymi kandydatami do tych terapii.
Małe RNA, które naciska hamulec
Badanie ujawniło także przeciwwagę dla tej prozapalnej ścieżki. Poprzez korelacje między ekspresją microRNA a genów w danych pacjentów, autorzy zidentyfikowali miR-129-5p jako małe RNA negatywnie powiązane z TRMP i IGFL4. W komórkach raka żołądka dodanie miR-129-5p obniżało poziomy IGFL4 i spowalniało wzrost, podczas gdy zablokowanie miR-129-5p zwiększało IGFL4 i przyspieszało proliferację. Inny kandydat, miR-4739, nie wpływał mierzalnie na IGFL4 i został wykluczony. Wyniki te wspierają model regulacyjny, w którym TRMP i TRMP-S, miR-129-5p oraz IGFL4 tworzą sieć, która precyzyjnie dostraja agresywność wzrostu komórek raka żołądka oraz ich interakcje z otoczeniem.
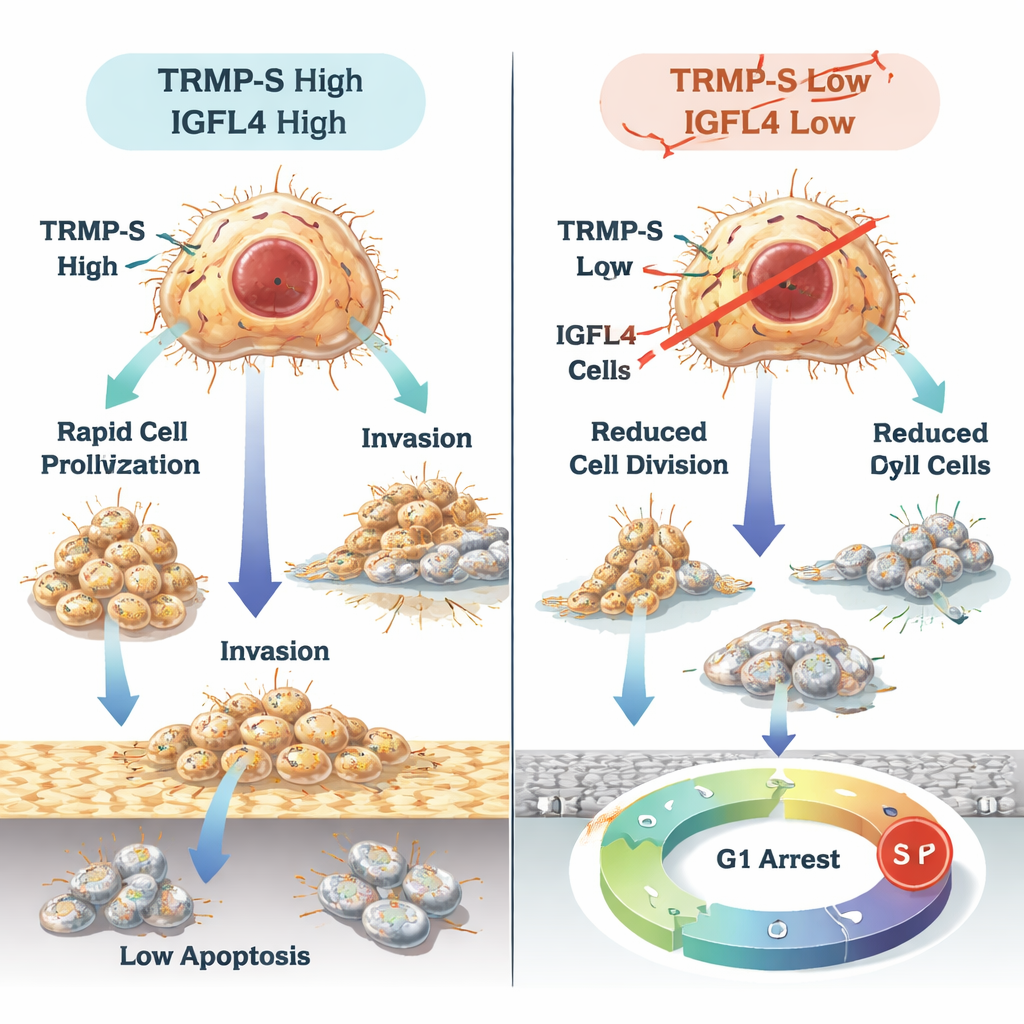
Co to może znaczyć dla pacjentów
Mówiąc prosto, praca ta pokazuje, że TRMP i TRMP-S działają jak reżyserzy zza kulis, włączając IGFL4 i pomagając komórkom raka żołądka rosnąć, rozprzestrzeniać się i omijać naturalne mechanizmy hamujące. Jednocześnie małe RNA miR-129-5p działa jak hamulec dla IGFL4, a sam IGFL4 kształtuje sposób, w jaki komórki odpornościowe gromadzą się wokół guzów i jak skuteczne mogą być terapie pobudzające układ odpornościowy. Chociaż potrzebne są dalsze badania i testy kliniczne, TRMP, TRMP-S, IGFL4 i miR-129-5p razem stanowią obiecujący zestaw markerów prognostycznych i potencjalnych celów terapeutycznych dla leczenia raka żołądka.
Cytowanie: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Słowa kluczowe: rak żołądka, długie RNA niekodujące, TRMP, IGFL4, mikrośrodowisko guza