Clear Sky Science · pl
Identyfikacja RBX1 jako regulatora transkrypcji LIPT1 oraz jego rola w miedzią indukowanej śmierci komórek w komórkach GBM
Dlaczego miedź i guzy mózgu mają znaczenie
Glejnik wielopostaciowy (glioblastoma multiforme) to jedna z najbardziej śmiertelnych postaci raka mózgu — większość pacjentów przeżywa krótko po rozpoznaniu, mimo agresywnego leczenia chirurgicznego, radioterapii i chemioterapii. Niniejsze badanie bada niespodziewanego sprzymierzeńca w walce z tymi nowotworami: metal miedź. Naukowcy analizują nowo rozpoznaną formę śmierci komórkowej wywołanej miedzią i identyfikują szlak molekularny, który może pomóc lekarzom wykorzystać ten proces do osłabienia guzów i potencjalnego wzmocnienia odpowiedzi immunologicznej przeciw komórkom nowotworowym.
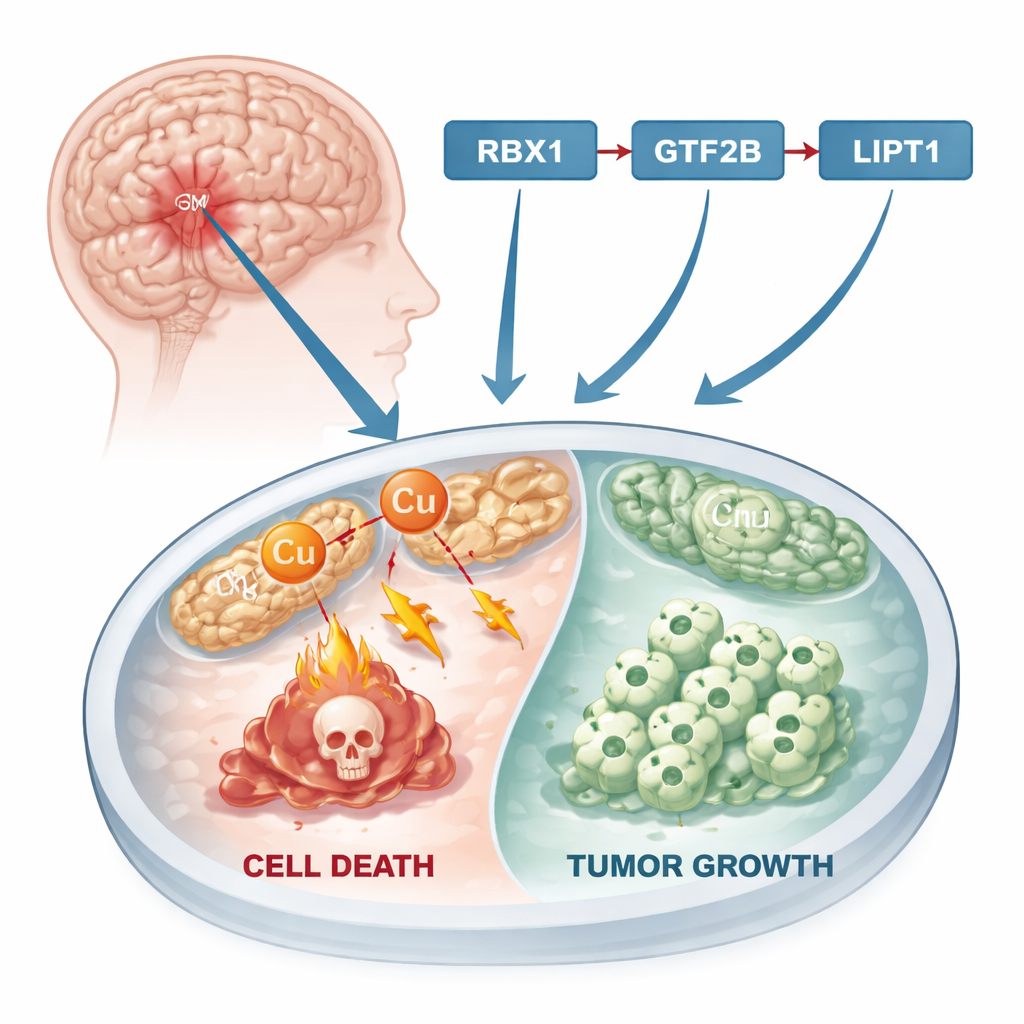
Nowy sposób umierania komórek
Przez dekady badania nad rakiem koncentrowały się na znanych formach śmierci komórkowej, takich jak apoptoza, w której uszkodzone komórki cicho wyłączają swoje funkcje. Niedawno naukowcy odkryli inną drogę nazwaną miedzią indukowaną śmiercią komórek, czyli „cuproptozą”. W tym procesie nadmiar miedzi gromadzi się w mitochondriach, komórkowych „elektrowniach”. Tam zaburza kluczowe białka, powodując tworzenie toksycznych agregatów, co ostatecznie prowadzi do śmierci komórki. Ponieważ wiele guzów ma zmieniony metabolizm metali i wyższe stężenia miedzi niż tkanki zdrowe, cuproptoza stwarza potencjalny punkt nacisku: jeśli badacze będą w stanie skierować komórki nowotworowe w stronę tej miedziowo napędzanej śmierci, mogą spowolnić lub zatrzymać wzrost nowotworu.
Wyróżnienie kluczowego genu w glejaku
Autorzy zaczęli od przeglądu grupy genów już powiązanych z cuproptozą i sprawdzili, jak zachowują się one w próbkach glejaka w porównaniu z tkanką mózgu o prawidłowej strukturze. Jeden gen w szczególności, nazwany LIPT1, wyróżnił się. Był bardziej aktywny w tkance glejakowej i w kilku liniach komórkowych glejaka niż w normalnych komórkach mózgu. Co ważne, pacjenci, których guzy wykazywały wyższą aktywność LIPT1, mieli tendencję do dłuższego czasu bez wznowy choroby po leczeniu. Wysokie poziomy LIPT1 wiązały się także z większą obecnością komórek CD8 T, podstawowych zabójców nowotworu układu odpornościowego, co sugeruje, że ten gen może sprawiać, iż mikrośrodowisko guza jest bardziej podatne na atak immunologiczny.
Co się dzieje, gdy wyłączony zostaje przełącznik śmierci zależnej od miedzi
Aby sprawdzić, czy LIPT1 rzeczywiście wpływa na miedzią napędzaną śmierć komórek, zespół wystawił komórki glejakowe na lek przenoszący miedź, który niezawodnie wywołuje cuproptozę. Następnie zastosowali narzędzia genetyczne do obniżenia poziomów LIPT1. Gdy LIPT1 został stłumiony, komórki nowotworowe stały się bardziej oporne na zabijanie wywołane miedzią, lepiej przeżywały i wykazywały silniejsze zdolności migracji i inwazji — zachowania związane z bardziej agresywnym nowotworem. W hodowlach mieszanych komórek nowotworowych i ludzkich komórek CD8 T, obniżenie LIPT1 zmniejszyło także uwalnianie molekuł sygnalizacyjnych układu odpornościowego i utrudniło T komórkom niszczenie komórek nowotworowych. Razem te eksperymenty wskazują, że LIPT1 zwiększa wrażliwość na miedzią indukowaną śmierć i wspiera aktywność przeciwnowotworową układu odpornościowego.
Śledzenie łańcucha dowodzenia do RBX1
Następnym wyzwaniem było zrozumienie, dlaczego LIPT1 jest podwyższone w glejaku. Łącząc kilka dużych baz danych genów i białek, badacze zidentyfikowali czynnik transkrypcyjny — swego rodzaju główny przełącznik aktywności genów — nazwany GTF2B, który wiąże się w pobliżu genu LIPT1 i prawdopodobnie zwiększa jego ekspresję. Potem sprawdzili, co kontroluje sam GTF2B. Drugie białko, RBX1, okazało się silnym kandydatem. RBX1 jest częścią komórkowego systemu znakowania i usuwania, który oznacza inne białka do degradacji. W komórkach glejakowych poziomy RBX1 były niższe niż w normalnych komórkach mózgu, podczas gdy GTF2B i LIPT1 były wyższe. Testy laboratoryjne wykazały, że RBX1 może przyłączać małe znaczniki „zniszcz mnie” do GTF2B, prowadząc do jego degradacji; gdy RBX1 był zwiększany, poziomy GTF2B i aktywność LIPT1 malały, a zablokowanie maszynerii degradacyjnej komórki odwracało ten efekt.
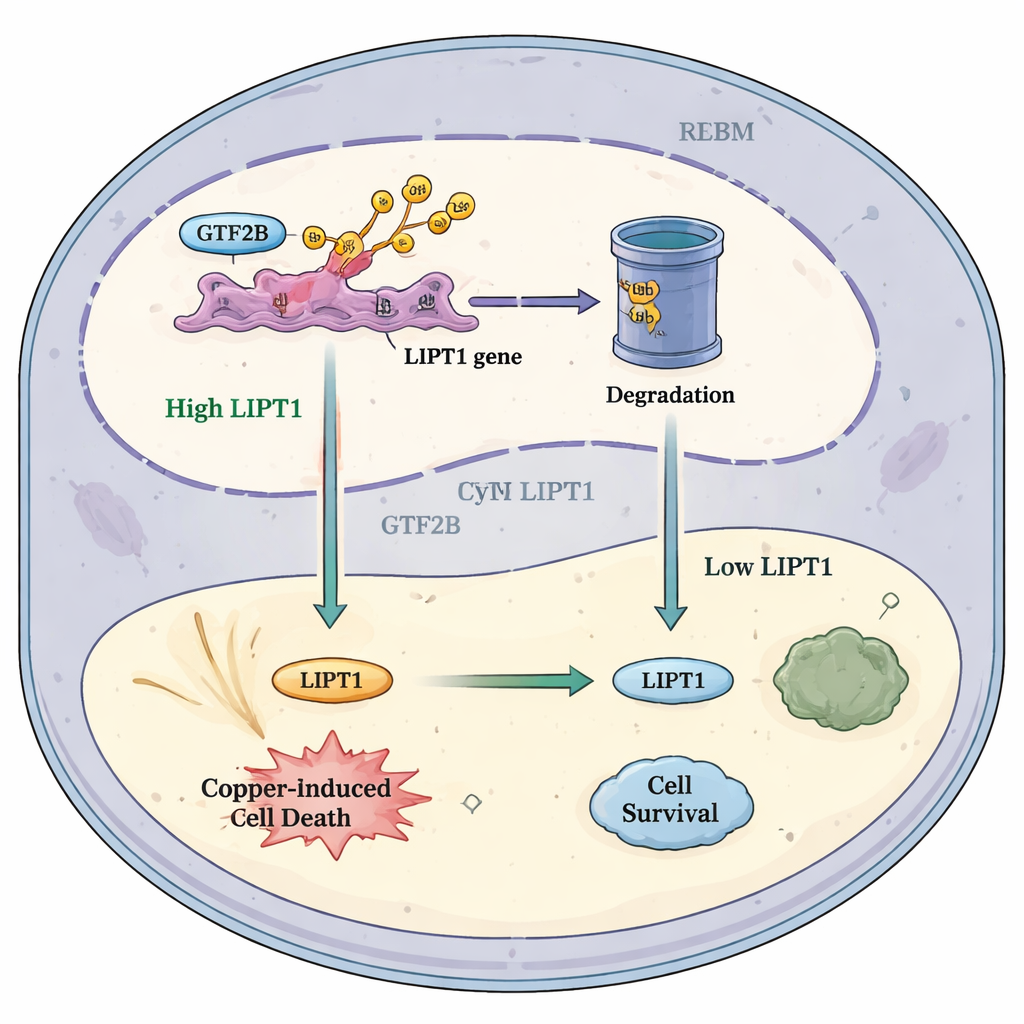
Jak ten szlak mógłby pomóc w przyszłych terapiach
Składając te ustalenia w jedną całość, autorzy proponują prosty model: w warunkach zdrowych RBX1 utrzymuje GTF2B w ryzach, ograniczając, jak mocno aktywuje gen LIPT1. W glejaku zmniejszone poziomy RBX1 oznaczają mniej degradacji GTF2B. Nadmiar GTF2B z kolei zwiększa LIPT1, podwyższając wrażliwość komórek nowotworowych na miedzią indukowaną śmierć i przyciągając więcej komórek odpornościowych walczących z rakiem. Model ten sugeruje, że precyzyjne dostrojenie szlaku RBX1–GTF2B–LIPT1, być może w połączeniu z lekami celującymi w miedź i immunoterapiami, mogłoby przechylić równowagę w obrębie guzów mózgu na stronę autodestrukcji. Choć przed zastosowaniem u pacjentów pozostaje wiele pracy, badanie podkreśla obiecujące przecięcie biologii metali, regulacji genów i immunologii nowotworów, które może otworzyć nowe drogi terapeutyczne dla jednego z najbardziej opornych nowotworów.
Cytowanie: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Słowa kluczowe: glejaki, miedzią indukowana śmierć komórek, LIPT1, immunologia nowotworów, szlak RBX1