Clear Sky Science · pl
MCT1 jako kluczowy regulator sygnalizacji insulinowej, homeostazy energetycznej i funkcji podocytów
Dlaczego wybór paliwa przez komórki nerek ma znaczenie
Nasze nerki po cichu filtrują setki litrów krwi każdego dnia, a wiele z tej pracy zależy od maleńkich komórek zwanych podocytami, które oplatają filtry nerkowe. Komórki te muszą nieustannie zmieniać kształt, by zatrzymywać białka we krwi i przepuszczać odpady do moczu. W badaniu tym zbadano, skąd podocyty czerpią energię, co się dzieje, gdy jedna z ich głównych „drzwi paliwowych” zostaje zablokowana, oraz dlaczego ma to znaczenie w powszechnych stanach, takich jak cukrzyca i choroby nerek. 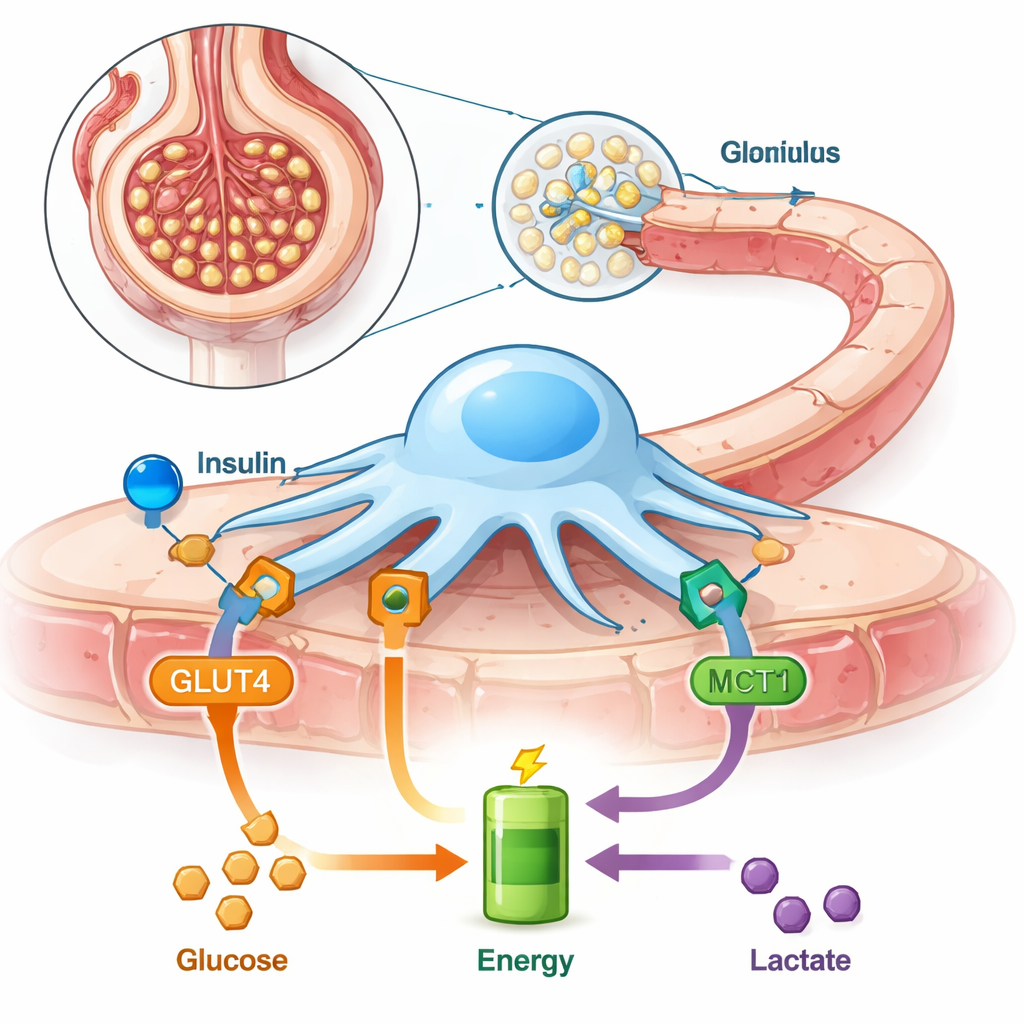
Strażnicy filtra
Podocyty leżą po zewnętrznej stronie każdego filtra nerkowego, wysyłając delikatne, przypominające stopy wypustki, które zazębiają się, tworząc ostateczną barierę przed powstaniem moczu. Ponieważ ciągle dostosowują swój kształt, zużywają dużo energii. W przeciwieństwie do wielu innych komórek, podocyty w dużym stopniu polegają na pozyskiwaniu energii z rozkładu cukru bez udziału tlenu (szlak zwany glikolizą) i są szczególnie wrażliwe na insulinę, która nakazuje im pobierać więcej cukru z krwi przez transporter GLUT4. Autorzy wcześniej wykazali, że podocyty mogą także wykorzystywać mleczan — małą cząsteczkę często uważaną za „odpad” — co sugeruje, że te komórki są bardziej elastyczne metabolicznie, niż sądzono.
Drzwi dla mleczanu: MCT1
Mleczan przemieszcza się do komórek i z nich przez specjalne białka transportowe. Jednym z najważniejszych jest monokarboksylanowy transporter 1 (MCT1), który może przenosić mleczan do wnętrza komórek, by był spalany jako paliwo. W tym badaniu naukowcy użyli hodowanych w szalkach podocytów szczura i zablokowali MCT1 za pomocą chemicznego inhibitora. Następnie sprawdzili, jak to wpływa na zdolność insuliny do pobudzania wychwytu cukru, ile energii komórki mogą wytworzyć, jak wygląda ich wewnętrzne rusztowanie oraz jak „przeciekowy” staje się filtr dla dużego białka krwi, albuminy. Przetestowali także całe izolowane filtry nerkowe (kłębuszki), by zobaczyć, jak mleczan i blokada MCT1 zmieniają przesączanie białka w bardziej zachowanym układzie.
Kiedy drzwi paliwowe się zamykają
Blokada MCT1 miała kilka uderzających efektów. Po pierwsze zmniejszyła ilość glukozy pobieranej przez podocyty, zarówno w warunkach spoczynkowych, jak i po stymulacji insuliną, oraz osłabiła ważny przełącznik w ścieżce insulinowej (białko zwane Akt) bez zaburzania samego receptora insuliny. Równocześnie normalne przemieszczanie transportera GLUT4 w kierunku powierzchni komórki było osłabione. Pomiary metabolizmu komórkowego wykazały, że całkowita produkcja energii spadła po zablokowaniu MCT1, a komórki przesunęły się z glikolizy w stronę większego spalania tlenowego w mitochondriach. Nawet dodanie insuliny lub mleczanu nie skompensowało w pełni tego niedoboru energetycznego, co sugeruje, że MCT1 odgrywa centralną rolę w równoważeniu źródeł energii podocytów. 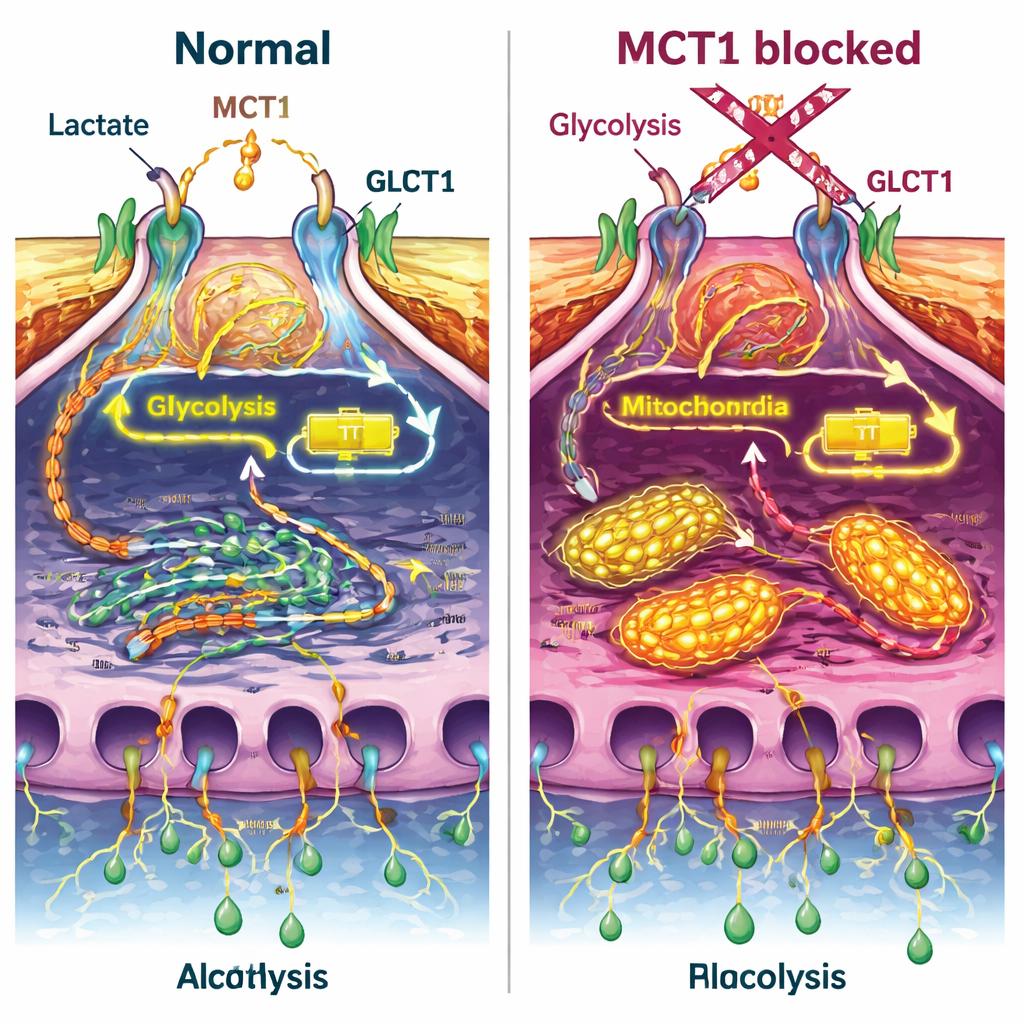
Przeciekające filtry i zestresowane rusztowania
Zmiany energetyczne były ściśle powiązane z uszkodzeniami strukturalnymi. Gdy MCT1 był zablokowany, warstwy podocytów w hodowli przepuszczały więcej albuminy, podobnie jak w odpowiedzi na samą insulinę. Sam mleczan także zwiększał przepuszczalność bariery, a połączenie mleczanu lub insuliny z blokadą MCT1 utrzymywało wysoką przepuszczalność. Wewnątrz komórek włókna aktynowe tworzące ich kształt stały się bardziej zgrupowane i zdezorganizowane — wzorzec związany z utratą cienkich wypustek stóp tworzących filtr. Kolejne kluczowe białko, nephryna, które pomaga scalać filtr i wspiera także działanie insuliny, było zmniejszone lub nieprawidłowo zlokalizowane po zahamowaniu MCT1. W izolowanych, całych filtrach z nerek szczura dodanie mleczanu szybko zwiększyło ucieczkę albuminy, a blokada MCT1 spowodowała podobny wzrost, co wspiera koncepcję, że zaburzona gospodarka mleczanowa bezpośrednio osłabia barierę filtracyjną.
Implikacje dla cukrzycy i zdrowia nerek
Autorzy proponują, że prawidłowy transport mleczanu przez MCT1 jest niezbędny, aby podocyty utrzymywały preferowany program energetyczny, reagowały na insulinę i zachowywały szczelność bariery filtracyjnej. Gdy „drzwi” dla mleczanu są zaburzone — przez blokadę MCT1 lub przewlekle podwyższony poziom cukru we krwi, który zmienia równowagę mleczanową — podocyty tracą elastyczność metaboliczną, spalają mniej glukozy, nadmiernie polegają na mitochondriach i stają się strukturalnie niestabilne i przeciekające. Dla ludzi praca ta sugeruje, że subtelne zmiany w sposobie, w jaki komórki nerek gospodarują mleczanem, mogą przyczyniać się do insulinooporności i wczesnych uszkodzeń nerek na długo przed pojawieniem się wyraźnych zaburzeń funkcji nerek. Zrozumienie, a w dalszej perspektywie ukierunkowanie tego systemu transportu mleczanu, może otworzyć nowe możliwości ochrony filtrów nerkowych w cukrzycy i innych chorobach metabolicznych.
Cytowanie: Szrejder, M., Audzeyenka, I., Rachubik, P. et al. MCT1 as a critical regulator of insulin signaling, energy homeostasis and podocyte function. Sci Rep 16, 5906 (2026). https://doi.org/10.1038/s41598-026-37093-x
Słowa kluczowe: podocyty nerkowe, metabolizm mleczanu, oporność na insulinę, bariery filtracji kłębuszkowej, transporter MCT1