Clear Sky Science · pl
Zautomatyzowana kwantyfikacja limfocytów naciekających guz przy użyciu uczenia maszynowego ujawnia cechy prognostyczne i immunogenomiczne w raku płuca
Dlaczego liczenie maleńkich komórek układu odpornościowego w guzach płuca ma znaczenie
Rak płuca wciąż należy do najgroźniejszych nowotworów, ale nie wszystkie guzy zachowują się tak samo. Niektóre są mocno patrolowane przez komórki odpornościowe, które wnikają do wnętrza guza, podczas gdy inne pozostają niemal nietknięte. Te limfocyty naciekające guz, zwane TIL, mogą wskazywać, jak pacjent poradzi sobie z chorobą i czy może odnieść korzyść z nowoczesnych leków immunoterapeutycznych. Problem polega na tym, że dziś TIL zwykle zlicza się wzrokowo pod mikroskopem, co jest powolne i subiektywne. W tym badaniu postawiono aktualne pytanie: czy można wykorzystać uczenie maszynowe do automatycznego pomiaru tych komórek na rutynowych preparatach histologicznych i co to ujawnia o biologii raka płuca oraz przeżyciu pacjentów?
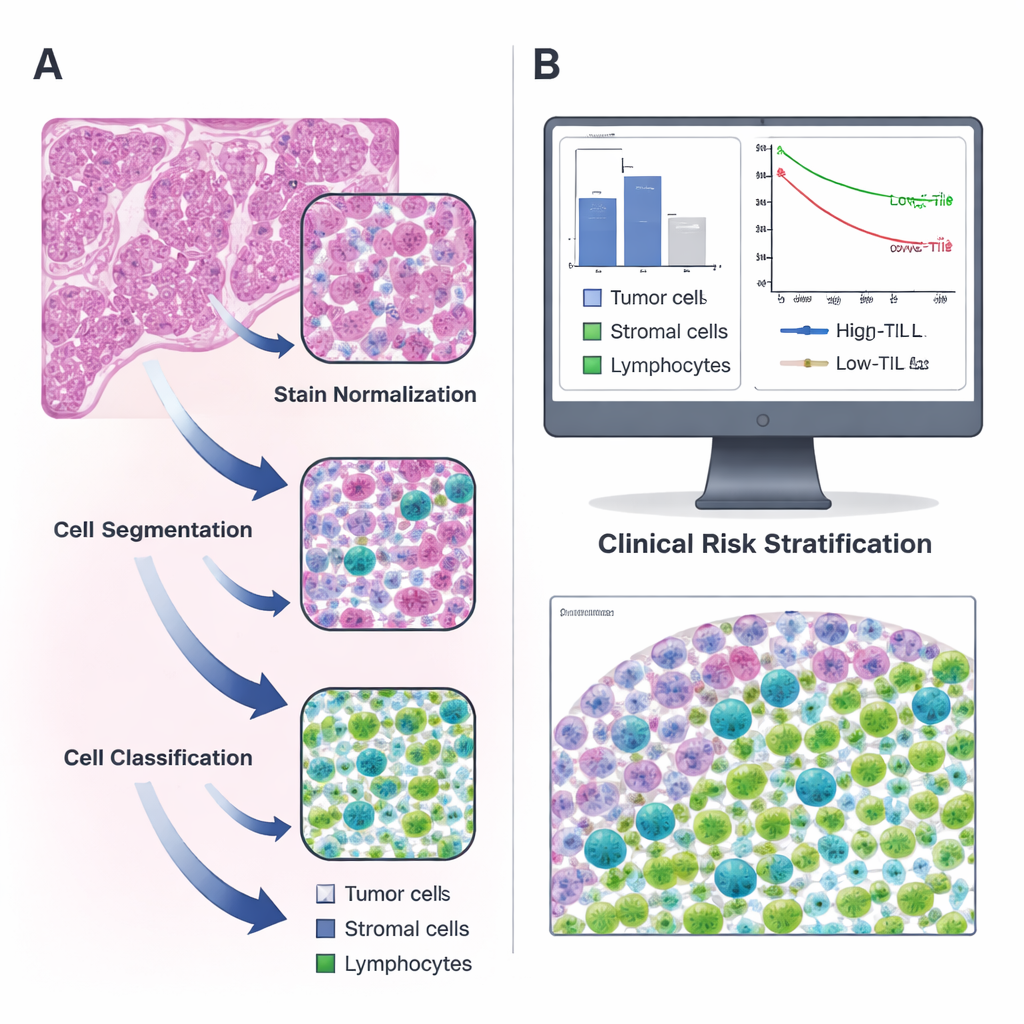
Przekształcanie zwykłych preparatów w mapy cyfrowe
Naukowcy skupili się na gruczolakoraku płuca, powszechnym typie raka płuca, wykorzystując publiczne dane z The Cancer Genome Atlas oraz niezależny zbiór pacjentów z własnego ośrodka. Dla każdego pacjenta analizowali standardowe barwione hematoksyliną i eozyną (H&E) szkiełka — różowo‑fioletowe obrazy dobrze znane każdemu patologowi. Przy użyciu otwartego oprogramowania QuPath zbudowali etapowy pipeline: najpierw skorygowali różnice kolorystyczne między preparatami; następnie zastosowali algorytm watershed do oddzielenia zachodzących na siebie jąder komórkowych; wreszcie wytrenowany klasyfikator komputerowy oznaczył każdą wykrytą komórkę jako komórkę nowotworową, tkankę podtrzymującą (tzw. stroma) lub limfocyt. Dwóch ekspertów‑patologów wielokrotnie przeglądało i korygowało pracę maszyny, aż ta była w stanie rozpoznawać różne typy komórek niezawodnie samodzielnie.
Łączenie liczby komórek odpornościowych z wynikami pacjentów
Gdy system potrafił już pewnie identyfikować komórki, zespół obliczył, ile limfocytów przypada na milimetr kwadratowy tkanki nowotworowej dla ponad 300 pacjentów. Stwierdzili, że poziomy TIL różnią się znacznie i przeciętnie stanowią tylko niewielki ułamek wszystkich komórek. Zastosowawszy podejście statystyczne w celu znalezienia najbardziej informatywnego progu, wybrali 135 TIL na mm² jako granicę między guzami o „wysokim” i „niskim” nasileniu nacieku. Pacjenci, których guzy przekraczały ten próg, żyli dłużej niż ci z niewielkim napływem komórek odpornościowych, a wzorzec ten utrzymał się zarówno w grupie odkrywczej, jak i walidacyjnej. Innymi słowy, prosta liczba wygenerowana przez narzędzie automatyczne odzwierciedliła istotne różnice w przeżyciu, potwierdzając wcześniejsze, bardziej pracochłonne badania bazujące na ręcznym liczeniu.
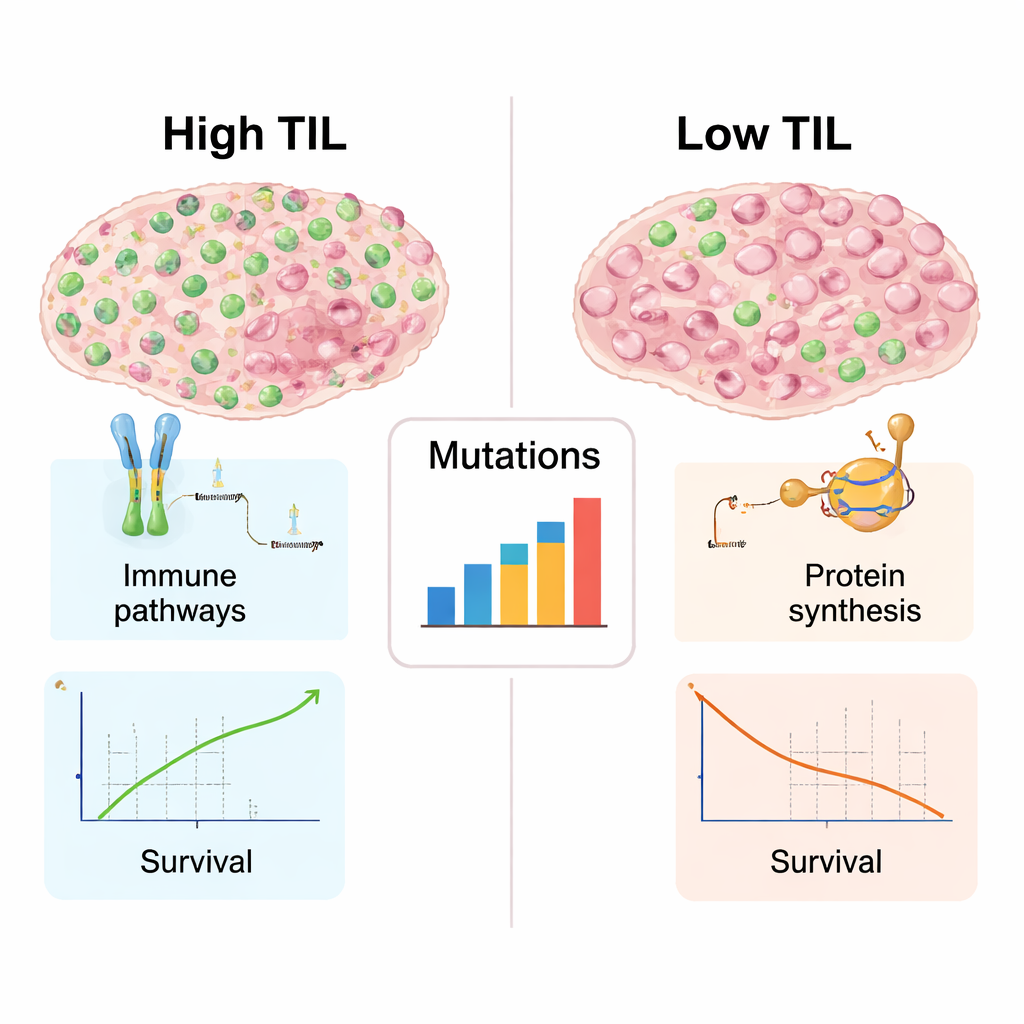
Jak wyglądają guzy bogate w komórki odpornościowe „pod maską”
Ponieważ dla wielu z tych guzów dostępne były dane genetyczne i molekularne, autorzy mogli zbadać, co odróżnia nowotwory o wysokim TIL od tych o niskim poza samą liczbą komórek. Guzy pełne limfocytów wykazywały silniejsze sygnatury aktywności immunologicznej: geny zaangażowane w rozpoznawanie nieprawidłowych białek, prezentację ich limfocytom T i koordynację ataku immunologicznego były bardziej aktywne. Te guzy miały też szerszy wachlarz mutacji DNA, które mogą tworzyć nowe cele dla układu odpornościowego. Natomiast guzy o niskim TIL faworyzowały geny związane z budową rybosomów i syntezą białek — znak intensywnej maszyny wzrostu przy stosunkowo cichej aktywności immunologicznej. Ten podział odzwierciedla dobrze znany kontrast między „gorącymi” guzami, bogatymi w komórki odpornościowe i bardziej podatnymi na immunoterapię, a „zimnymi” guzami, które system odpornościowy w dużej mierze ignoruje.
Nauczanie komputera przewidywania statusu immunologicznego
Zespół posunął się dalej i zapytał, czy kompaktowy zestaw cech obrazowych może przewidzieć, czy guz znajdzie się w kategorii wysokiego czy niskiego TIL bez konieczności ręcznego zliczania każdego limfocytu. Skompresowali subtelne wzory tekstury na preparatach — jak intensywność pikseli zmienia się w małych sąsiedztwach — do tzw. cech Haralicka i połączyli je ze stadium klinicznym guza w modelu lasu losowego. W walidacji krzyżowej klasyfikator ten poprawnie odróżniał guzy o wysokim i niskim TIL z wysoką dokładnością, a w niezależnej kohorcie szpitalnej zachował rozsądną wydajność. Co istotne, cały proces działa na standardowych komputerach z użyciem ogólnodostępnego oprogramowania, co sugeruje, że wiele pracowni patologicznych mogłoby w praktyce przyjąć tę metodę bez specjalistycznego sprzętu.
Co to oznacza dla przyszłej opieki nad chorymi na raka płuca
Dla osób spoza specjalności kluczowy wniosek jest taki, że komputer może nauczyć się czytać rutynowe preparaty raka płuca w sposób ukazujący, jak silnie układ odpornościowy zaangażował się w walkę z guzem. Wysoki poziom limfocytów naciekających sygnalizuje bardziej aktywną odpowiedź immunologiczną, bogatsze spektrum mutacji i lepsze ogólne przeżycie. Chociaż potrzeba więcej badań — zwłaszcza u pacjentów leczonych faktycznie immunoterapią — ta zautomatyzowana metoda mogłaby ostatecznie pomóc lekarzom szybko i spójnie zaklasyfikować guzy jako immunologicznie „gorące” lub „zimne”. To z kolei mogłoby ukierunkować decyzje o tym, kto najbardziej skorzysta na leczeniu immunologicznym, oraz zainspirować nowe strategie, by „ochłodzić” guzy przekształcić w bardziej podatne na immunoterapię.
Cytowanie: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Słowa kluczowe: gruczolakorak płuca, limfocyty naciekające guz, uczenie maszynowe, patologia cyfrowa, immunoterapia nowotworów