Clear Sky Science · pl
Badania mechanizmu molekularnego celastrolu kierującego CTNNB1/STAT3 w celu hamowania czerniaka naczyniówki oparte na farmakologii sieciowej i analizie multi-omicznej
Tradycyjna medycyna spotyka raka oka
Czerniak naczyniówki to rzadki, lecz śmiertelny nowotwór rozwijający się wewnątrz oka. Gdy dojdzie do przerzutów, dostępne dziś terapie niewiele zmieniają rokowania. W niniejszym badaniu sprawdzono, czy celastrol — związek wyizolowany z rośliny wykorzystywanej w tradycyjnej medycynie chińskiej — można ponownie wykorzystać do zwalczania tego nowotworu. Łącząc analizy dużych zbiorów danych biologicznych, symulacje komputerowe i eksperymenty laboratoryjne, autorzy wyjaśniają, jak celastrol może wyłączać kluczowe molekularne przełączniki wspierające wzrost i rozprzestrzenianie się czerniaka naczyniówki.
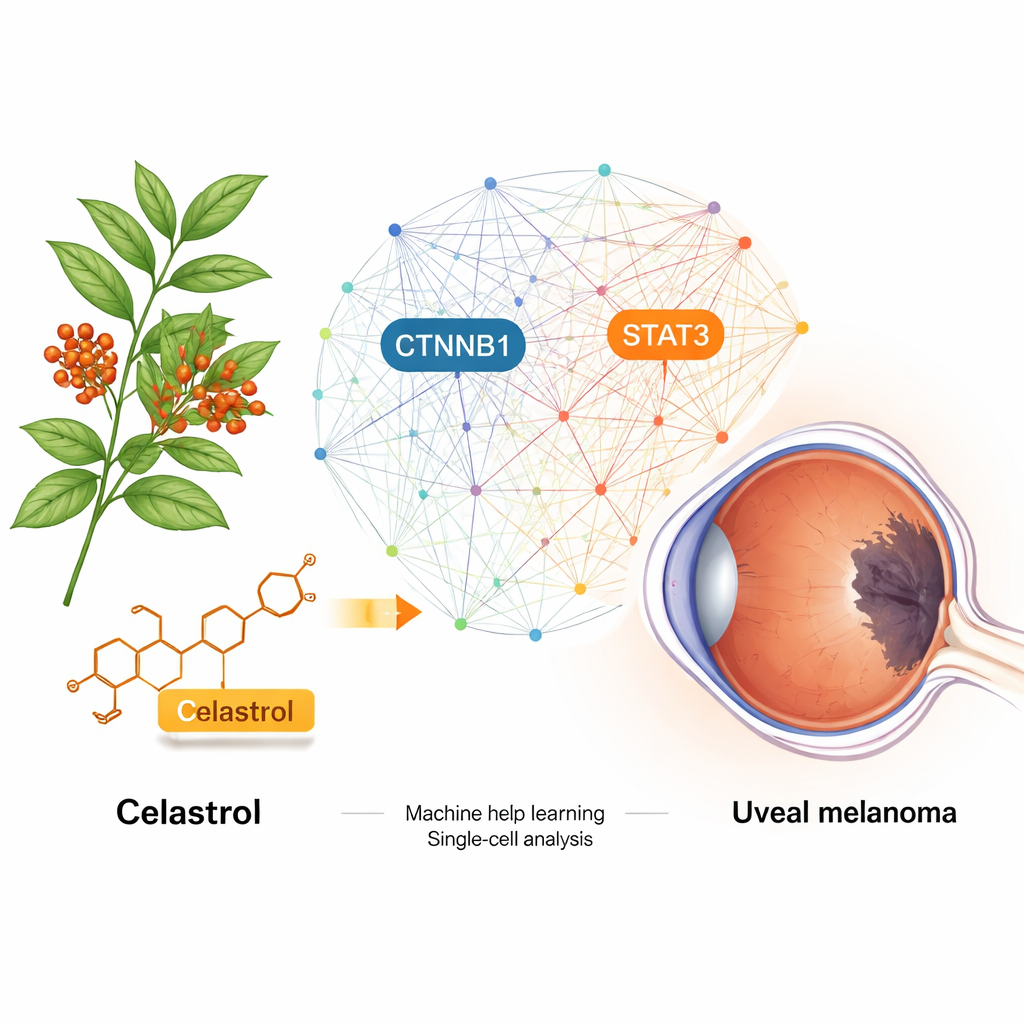
Co sprawia, że ten guz oka jest tak groźny
Czerniak naczyniówki jest najczęstszym pierwotnym nowotworem oka u dorosłych, a około połowa pacjentów ostatecznie rozwija przerzuty, zwykle w wątrobie. Na tym etapie przeżycie często mierzy się miesiącami. Standardowe terapie, takie jak zabieg chirurgiczny, radioterapia i leczenie miejscowe, mogą kontrolować pierwotny guz oka, ale leki działające ogólnoustrojowo przyniosły ograniczone korzyści i mogą powodować poważne skutki uboczne. Naukowcy szukają więc leków, które jednocześnie hamują wzrost guza i są lepiej tolerowane — obszar, w którym naturalne produkty, takie jak celastrol, budzą duże zainteresowanie.
Związek naturalny pod lupą
Celastrol pochodzi z Tripterygium wilfordii, rośliny długo stosowanej w tradycyjnej medycynie chińskiej. Wcześniejsze badania wykazały, że może spowalniać wzrost różnych nowotworów, ale jego działanie w czerniaku naczyniówki było niejasne. Zespół rozpoczął od przeszukania licznych baz danych biomedycznych, aby przewidzieć, z którymi białkami w komórkach człowieka celastrol może wiązać się oraz które białka są silnie związane z czerniakiem naczyniówki. Porównanie tych list ujawniło 46 nakładających się kandydatów. Korzystając z narzędzi komputerowych mapujących wzajemne interakcje białek, zawęzili listę do kilku „węzłowych” cząsteczek, które znajdują się w punktach kontrolnych głównych szlaków wzrostu i przeżycia komórek nowotworowych.
Skupienie na dwóch głównych przełącznikach
Aby określić najistotniejszych graczy, badacze połączyli dane genowe guzów pacjentów z The Cancer Genome Atlas z trzema różnymi metodami uczenia maszynowego. Wszystkie trzy podejścia zbiegały się na dwóch genach: CTNNB1, kluczowym elemencie szlaku sygnalizacji Wnt napędzającego wzrost komórek, oraz STAT3, istotnym regulatorze zapalenia, przeżycia i unikania układu odpornościowego. Dalsze analizy próbek guzów jako całości i sekwencjonowania RNA pojedynczych komórek wykazały, że te geny są wysoce aktywne w komórkach czerniaka naczyniówki, szczególnie w agresywniejszych podgrupach komórkowych, i wiążą się ze zmianami w otaczających komórkach układu odpornościowego. Krótko mówiąc, CTNNB1 i STAT3 wyglądały na główne przełączniki, które pomagają nowotworowi przetrwać, jednocześnie tłumiąc odpowiedź immunologiczną.
Z modeli komputerowych do żywych komórek
Zespół następnie zastosował dokowanie molekularne i długie symulacje dynamiki molekularnej, aby sprawdzić, czy celastrol może fizycznie przyłączyć się do CTNNB1 i STAT3. Wirtualne eksperymenty sugerowały silne i stabilne wiązanie, wspierane przez liczne wiązania wodorowe i ciasne upakowanie wokół leku. Kolejnym krokiem były badania laboratoryjne: traktowano ludzkie komórki czerniaka naczyniówki i powiązaną mysią linię komórkową celastrolem. W obu przypadkach celastrol wyraźnie zmniejszał przeżywalność komórek i tworzenie kolonii, spowalniał migrację w testach zagojenia rany i wywoływał zaprogramowaną śmierć komórkową. Powodował też zatrzymanie komórek w określonych fazach cyklu komórkowego, uniemożliwiając ich podział. Pomiar aktywności genów i poziomów białek wykazał, że celastrol znacząco obniża CTNNB1 i STAT3, potwierdzając, że uderza w przewidywane cele w żywych komórkach.
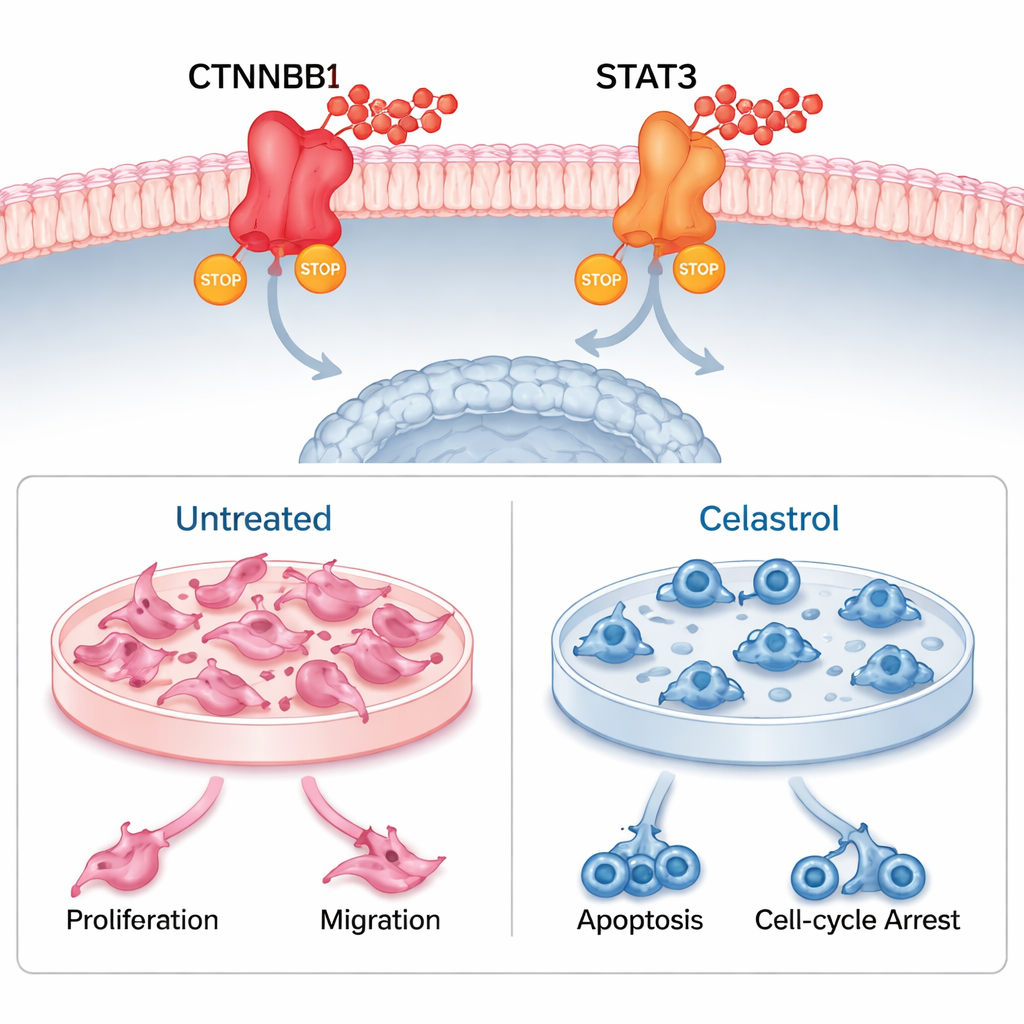
Co to może znaczyć dla przyszłych terapii
W sumie wyniki sugerują, że celastrol zwalcza czerniaka naczyniówki poprzez jednoczesne wyłączanie CTNNB1 i STAT3. Ta podwójna akcja nie tylko spowalnia wzrost i rozprzestrzenianie się guza, lecz także może przekształcać mikrośrodowisko nowotworu w sposób sprzyjający odpowiedzi przeciwnowotworowej. Chociaż badania przeprowadzono na komórkach i w modelach komputerowych — jeszcze nie na pacjentach ani w modelach zwierzęcych — stanowią one solidną podstawę do dalszych testów. Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że związek wywodzący się z medycyny tradycyjnej stał się naukowo wiarygodnym kandydatem do nowej klasy terapii raka oka, celującej zarówno w sam guz, jak i w jego ekosystem komórkowy.
Cytowanie: Li, Z., Xi, R., Han, X. et al. Research on the molecular mechanism of celastrol targeting CTNNB1/STAT3 to inhibit uveal melanoma based on network pharmacology and multi-omics analysis. Sci Rep 16, 6140 (2026). https://doi.org/10.1038/s41598-026-37061-5
Słowa kluczowe: czerniak naczyniówki, celastrol, nowotwór oka, sygnalizacja nowotworowa, mikrośrodowisko guza