Clear Sky Science · pl
Opracowanie i wstępna ocena testów PCR w czasie rzeczywistym dla sześciu bakterii kwasu mlekowego
Przyjazne mikroby stojące za produktami codziennego użytku
Wiele produktów dostępnych na sklepowych półkach — od jogurtów i serów po ogórki kiszone i fermentowane warzywa — zawdzięcza smak i potencjalne korzyści zdrowotne przyjaznym bakteriom określanym jako probiotyki. Aby jednak korzystać z tych „dobrych bakterii” w sposób bezpieczny i przewidywalny, firmy muszą mieć absolutną pewność, jakie gatunki bakterii rzeczywiście występują w ich produktach. Niniejsze badanie opisuje nowe testy laboratoryjne, które mogą szybko i dokładnie identyfikować sześć obiecujących bakterii probiotycznych stosowanych w żywności, pomagając zbliżyć zaawansowaną mikrobiologię do codziennych produktów, które spożywamy.
Dlaczego te bakterie probiotyczne są ważne
Sześć bakterii będących przedmiotem tego badania należy do szerszej grupy zwanej bakteriami kwasu mlekowego, od dawna wykorzystywanych w fermentacji. Najnowsze badania sugerują, że robią więcej niż tylko zakwaszają mleko czy kapustę. Niektóre szczepy Ligilactobacillus agilis i Ligilactobacillus salivarius mogą pomagać w zwalczaniu szkodliwych drobnoustrojów jelitowych, łagodzić stan zapalny i wspierać integralność bariery jelitowej. Limosilactobacillus fermentum wiązano z lepszą kontrolą ciśnienia krwi i działaniem przeciwutleniającym w badaniach na zwierzętach. Lactobacillus johnsonii wydaje się pomagać w równoważeniu mikroflory jelitowej w sposób, który może chronić różne narządy. Pediococcus pentosaceus i Weissella cibaria wykazują potencjał w obniżaniu poziomu cholesterolu, zwalczaniu psucia się produktów, a nawet we wspieraniu zdrowia jamy ustnej. Przy tak szerokim spektrum możliwych korzyści przemysł spożywczy chętnie używałby tych gatunków częściej — pod warunkiem, że można je zidentyfikować z pewnością.
Wyzwanie w rozróżnianiu podobnych mikroorganizmów
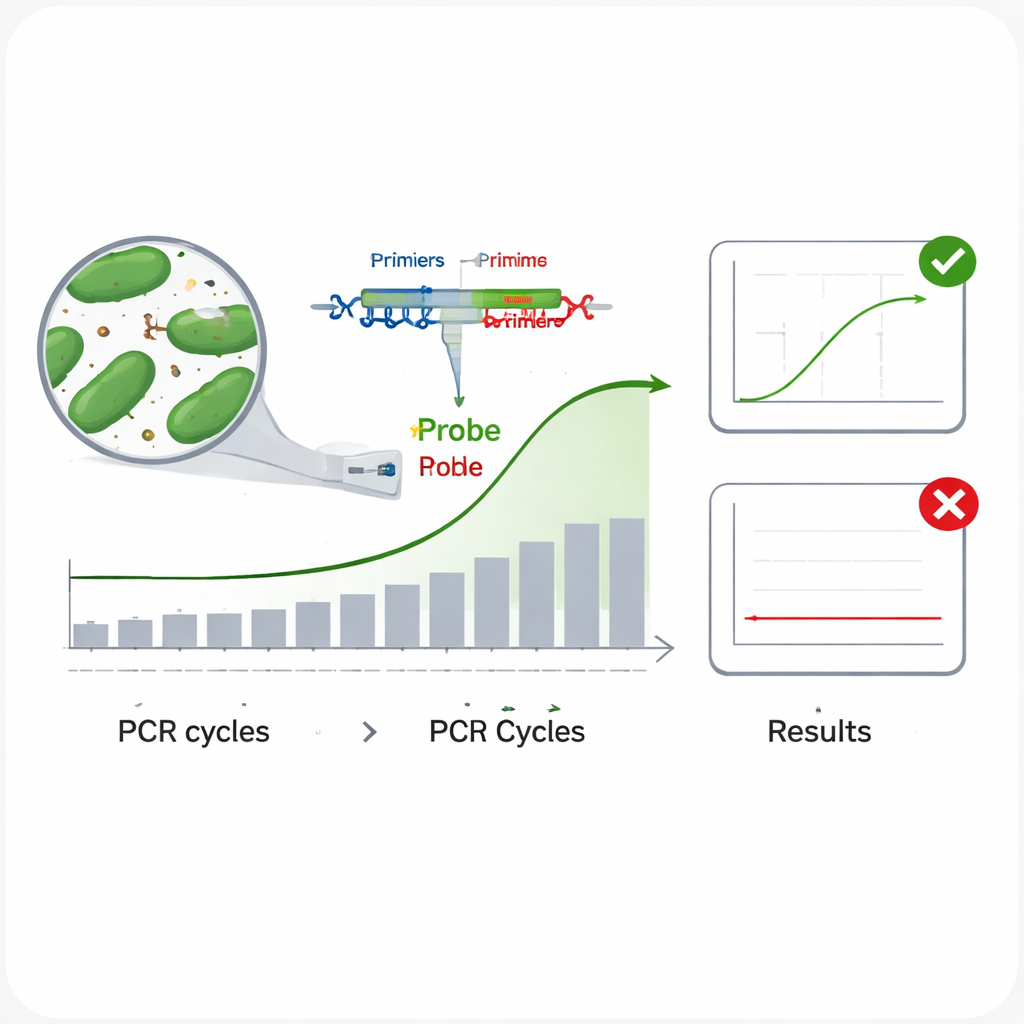
Tradycyjne metody identyfikacji bakterii — hodowla w laboratorium i testy biochemiczne — są powolne i pracochłonne. Nowoczesne metody oparte na DNA, zwłaszcza PCR w czasie rzeczywistym, są znacznie szybsze. W PCR w czasie rzeczywistym krótkie odcinki DNA zwane starterami oraz sondą fluorescencyjną celują w unikalny fragment kodu genetycznego mikroba; gdy obecny jest właściwy mikroorganizm, aparat wykrywa świecący sygnał w miarę kopiowania DNA w kolejnych cyklach. Problem polega na tym, że blisko spokrewnione bakterie mogą mieć bardzo podobne sekwencje DNA, więc powszechnie używane regiony genetyczne, takie jak gen 16S rRNA, czasami nie rozróżniają gatunków. Może to prowadzić do testów, które pomijają cel (fałszywe negatywy) lub reagują na niewłaściwy gatunek (fałszywe pozytywy) — oba przypadki są nieakceptowalne przy etykietowaniu produktów i zapewnianiu bezpieczeństwa.
Projektowanie ostrzejszych molekularnych „kodów kreskowych”
Aby to obejść, badacze przeanalizowali kompletne sekwencje genomowe w poszukiwaniu krótkich regionów DNA, które były zarówno silnie zachowane w obrębie każdego docelowego gatunku, jak i wyraźnie różne od innych bakterii. Dla każdego z sześciu probiotyków zaprojektowali dopasowany zestaw starterów i sondę o starannie dobranej długości, składzie zasad, temperaturze topnienia oraz minimalnej skłonności do tworzenia struktur drugorzędowych lub przywierania do siebie. Kontrole komputerowe przy użyciu bazy BLAST i oprogramowania do wyrównywania sekwencji potwierdziły, że wybrane regiony DNA są stabilne w obrębie gatunku, a jednocześnie różne od nie‑celów. Zespół opracował także standardowy skład reakcji i program temperaturowy, tak aby wszystkie testy można było przeprowadzać w jednakowych i praktycznych warunkach na tym samym typie aparatu do PCR w czasie rzeczywistym.
Testowanie nowych oznaczeń w praktyce
Naukowcy następnie ocenili, jak każdy test sprawdza się w praktyce. Aby sprawdzić inkluzywność — czy test potrafi wykryć wiele różnych szczepów tego samego gatunku — uruchamiali każdy test na wielu próbkach DNA pochodzących od docelowej bakterii. We wszystkich przypadkach wszystkie badane szczepy wykazały wyraźną krzywą amplifikacji, co sugeruje niskie ryzyko pominięcia autentycznych celów. Aby sprawdzić swoistość — czy test ignoruje gatunki nie‑docelowe — poddali każdy test wyzwaniu w postaci DNA od 13 innych bakterii jelitowych, w tym spokrewnionych bakterii kwasu mlekowego i powszechnych drobnoustrojów jelitowych, takich jak Escherichia coli. Żaden z nich nie dał sygnału, co wskazuje na bardzo niskie ryzyko fałszywych alarmów. Zespół zbadał również wydajność amplifikacji, przeprowadzając serię rozcieńczeń DNA o dziesięciokrotnym stopniu i potwierdził, że wszystkie sześć testów kopiowało cele z efektywnością około 95–100%, zbliżoną do ideału. Wreszcie zmierzyli precyzję, powtarzając przebiegi przy dwóch poziomach DNA i stwierdzili, że niewielkie różnice między powtórzeniami i między oddzielnymi eksperymentami pozostawały daleko poniżej przyjętych granic.
Co to oznacza dla przyszłych produktów spożywczych
Mówiąc wprost, autorzy stworzyli sześć precyzyjnie dopasowanych testów DNA‑owych „odcisków palców”, które potrafią szybko, dokładnie i wiarygodnie rozróżnić kluczowe gatunki probiotyczne. Zastrzegają jednak, że przed rutynowym wdrożeniem przemysłowym potrzebne są szersze badania obejmujące więcej szczepów, więcej gatunków nie‑docelowych oraz dodatkowe aparaty PCR. Wstępne wyniki są jednak obiecujące. Dla konsumentów postępy takie jak te pomagają upewnić się, że produkty reklamowane jako zawierające określone probiotyki rzeczywiście zawierają właściwe mikroby, co z kolei wspiera rzetelne etykietowanie, lepszą kontrolę jakości i bardziej wiarygodne badania nad tym, jak ci mali partnerzy wpływają na nasze zdrowie.
Cytowanie: Li, SJ., Cui, B., Li, W. et al. Development and preliminary evaluation of real-time PCR assays for six lactic acid bacteria. Sci Rep 16, 6165 (2026). https://doi.org/10.1038/s41598-026-37047-3
Słowa kluczowe: probiotyki, bakterie kwasu mlekowego, PCR w czasie rzeczywistym, mikrobiologia żywności, identyfikacja mikroorganizmów