Clear Sky Science · pl
Predykcja krwotocznej transformacji po trombektomii z użyciem ilościowej DSA wspomagana uczeniem maszynowym
Dlaczego to ma znaczenie dla chorych po udarze
Gdy ktoś doznaje ciężkiego udaru, lekarze czasem potrafią usunąć skrzeplinę z głównej tętnicy mózgu za pomocą niewielkiego urządzenia w zabiegu nazywanym mechaniczną trombektomią. Zmieniło to opiekę nad chorymi po udarze, ale wielu pacjentów nadal ma złe rokowanie, ponieważ u niektórych pojawia się nowe krwawienie w mózgu. Badanie opisane w tym artykule stawia proste, lecz istotne pytanie: czy można wykorzystać informacje, które lekarze już zbierają na sali operacyjnej, wraz z nowoczesnym uczeniem maszynowym, do przewidzenia, którzy pacjenci są najbardziej narażeni na krwawienie i wymagają dodatkowej ochrony?
Patrząc dalej niż „tętnica otwarta czy zamknięta”
Obecnie sukces po trombektomii zwykle ocenia się na podstawie tego, czy zamknięta tętnica wygląda na ponownie udrożnioną w angiografii — rodzaj filmowego prześwietlenia naczyń. Jednak to zgrubne kryterium nie ujawnia, co dzieje się w drobnych naczyniach mózgu położonych dalej w „dole”, gdzie faktycznie dochodzi do uszkodzeń i krwawień. Niektórzy pacjenci z pozornie idealnie udrożnionymi dużymi naczyniami i tak rozwijają groźne krwawienie mózgowe, zjawisko nazywane krwotoczną transformacją. Autorzy przypuszczali, że bardziej szczegółowe pomiary przepływu w tych małych naczyniach, wyciągnięte z tej samej angiografii, mogą kryć ukryte wskazówki dotyczące ryzyka.
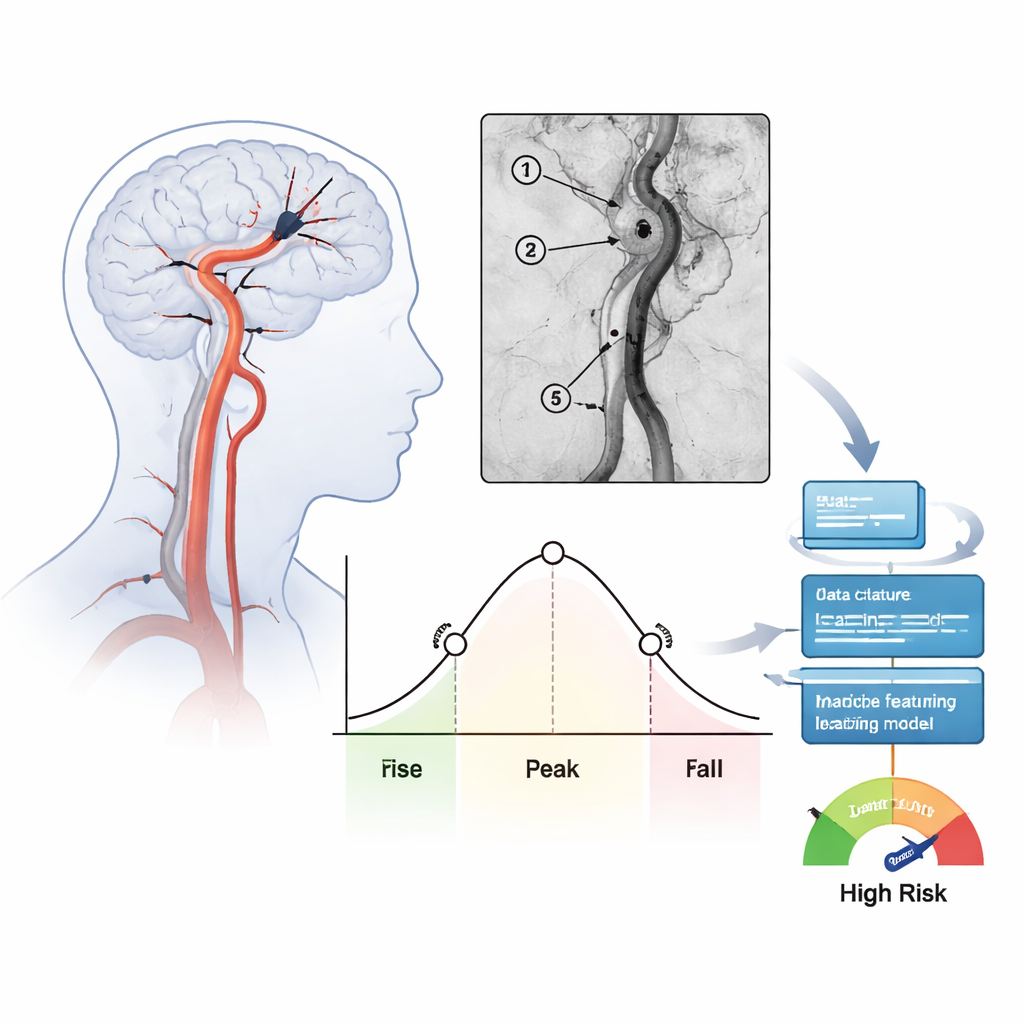
Przekształcanie filmów angiograficznych w liczby
Zespół przeanalizował 171 osób leczonych z powodu ciężkich udarów w przedniej części mózgu w ciągu roku w jednym szpitalu. Po usunięciu skrzepliny i przywróceniu przepływu zarejestrowano standardowe projekcje angiograficzne, a następnie analizowano, jak wstrzyknięty kontrast wchodził i wypływał z kilku kluczowych miejsc wzdłuż leczonej tętnicy. Dla każdego regionu obliczono miary czasowe, takie jak średni czas tranzytu (mean transit time) i szerokość głównego impulsu kontrastu na pół wysokości (full width at half maximum). Te liczby podsumowują, czy krew przesuwa się powoli i równomiernie, czy przelatuje szybko w wąskim impulsie. Łącznie z każdego pacjenta wyekstrahowano 39 takich cech przepływu i sprawdzono ich spójność między niezależnymi oceniającymi.
Nauczanie komputera rozpoznawania ryzykownych wzorców
Naukowcy zastosowali zestaw popularnych metod uczenia maszynowego, aby sprawdzić, czy te cechy przepływu same w sobie lub w połączeniu z podstawowymi danymi klinicznymi, takimi jak wiek i ciężkość udaru, potrafią odróżnić pacjentów, u których później rozwinęło się krwawienie mózgowe, od tych bez tego powikłania. Aby uniknąć nadmiernego dopasowania, najpierw użyto pięciu różnych technik wyboru cech, by wybrać najbardziej informatywne miary, oraz wielokrotnie dzielono dane na zbiory uczące i testowe przy użyciu walidacji krzyżowej. Spośród wielu sprawdzonych kombinacji najlepiej wypadł relatywnie prosty model — regresja logistyczna, dostrojona z użyciem filtra cech „Elastic Net”. Gdy polegał wyłącznie na miarach przepływu pochodzących z angiografii, poprawnie rozdzielał pacjentów z i bez krwawienia z przeciętnym polem pod krzywą ROC około 0,81. Po dodaniu czynników klinicznych wydajność wzrosła do około 0,86, co sugeruje, że model mógłby być silnym narzędziem wspomagającym decyzje.
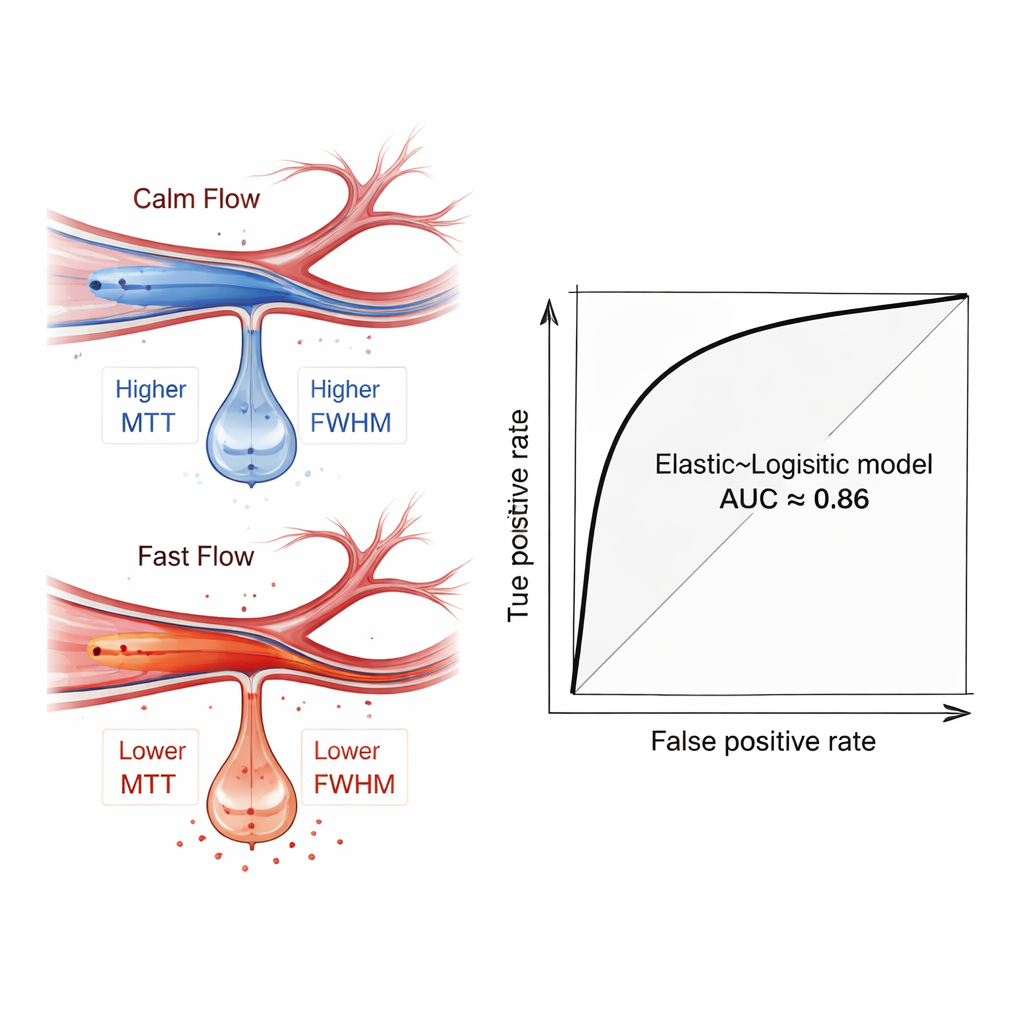
Co ujawniły sygnały przepływu krwi
Analizując wytrenowane modele, autorzy użyli techniki interpretowalności zwanej SHAP, aby zobaczyć, które cechy miały największe znaczenie. Na czoło wysunęły się miary oddające, jak długi i jak rozciągnięty był impuls przepływu — szczególnie w dalszym odgałęzieniu tętnicy środkowej mózgu. Pacjenci, u których później wystąpiło krwawienie, mieli skłonność do szybszego, bardziej skupionego przepływu w tych dystalnych naczyniach, co odzwierciedlały krótsze czasy tranzytu i węższe piki. Ten wzorzec jest hemodynamicznym odciskiem palca „hiperperfuzji” — stanu, w którym kruche tkanki mózgu, nagle napełnione szybkim strumieniem krwi po okresie niedokrwienia, częściej przeciekają i krwawią. Co ważne, sygnał ten ujawnił się nawet wtedy, gdy proste porównania grupowe nie wykazywały dramatycznych różnic statystycznych, podkreślając wartość analizy wielocechowej prowadzonej przez maszyny.
Jak to może zmienić opiekę przy łóżku pacjenta
Ponieważ metoda wykorzystuje obrazy już pozyskiwane podczas trombektomii, nie wymaga dodatkowych badań, kontrastu ani promieniowania. Po zaznaczeniu obszarów zainteresowania — kroku, który obecnie zajmuje kilka minut — komputer może automatycznie obliczyć miary przepływu i wygenerować spersonalizowaną ocenę ryzyka krwawienia. W praktyce mogłoby to pomóc lekarzom w dopasowaniu celów ciśnienia krwi, decyzjach o agresywności podawania leków przeciwkrzepliwych oraz planowaniu wcześniejszych badań CT u pacjentów oznaczonych jako wysokiego ryzyka. Autorzy zastrzegają, że ich badanie jest retrospektywne i pochodzi z jednego ośrodka, więc przed wprowadzeniem narzędzia do rutynowej praktyki potrzebne są większe, wieloośrodkowe próby. Mimo to daje ono jasny dowód koncepcji: przekształcając angiogramy w bogate dane liczbowe i pozwalając uczeniu maszynowemu je przesiać, możemy pójść dalej niż pytanie „Czy tętnica jest otwarta?” — do pytania „Czy mikrokrążenie mózgu jest bezpieczne?” — zmiany, która może w efekcie uchronić więcej pacjentów przed niebezpiecznym krwawieniem po leczeniu.
Cytowanie: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Słowa kluczowe: udar, mechaniczna trombektomia, krwotok mózgowy, uczenie maszynowe, angiografia