Clear Sky Science · pl
Elektrochemiczny biosensor z wykorzystaniem zmodyfikowanego fagowego M13 i rGO do szybkiego wykrywania białka wirusa w złożonych matrycach
Dlaczego szybkie testy wirusowe wciąż mają znaczenie
Pandemia COVID-19 uwypukliła, jak ważne jest szybkie wykrywanie wirusów — nie tylko u pacjentów, lecz także w miejscach takich jak ścieki czy linie produkcji żywności. Współczesne testy laboratoryjne są potężne, ale mogą być wolne, kosztowne i zależne od kruchych składników biologicznych, które trudno transportować i przechowywać. W tym badaniu przedstawiono nowy rodzaj miniaturowego czujnika elektronicznego, który wykorzystuje zaprojektowane wirusy oraz warstwę zaawansowanego materiału węglowego do wykrywania kluczowego fragmentu białka S SARS-CoV-2 w mniej niż sekundę, nawet w zanieczyszczonych próbkach rzeczywistych, takich jak surowica krwi, mleko czy ścieki.
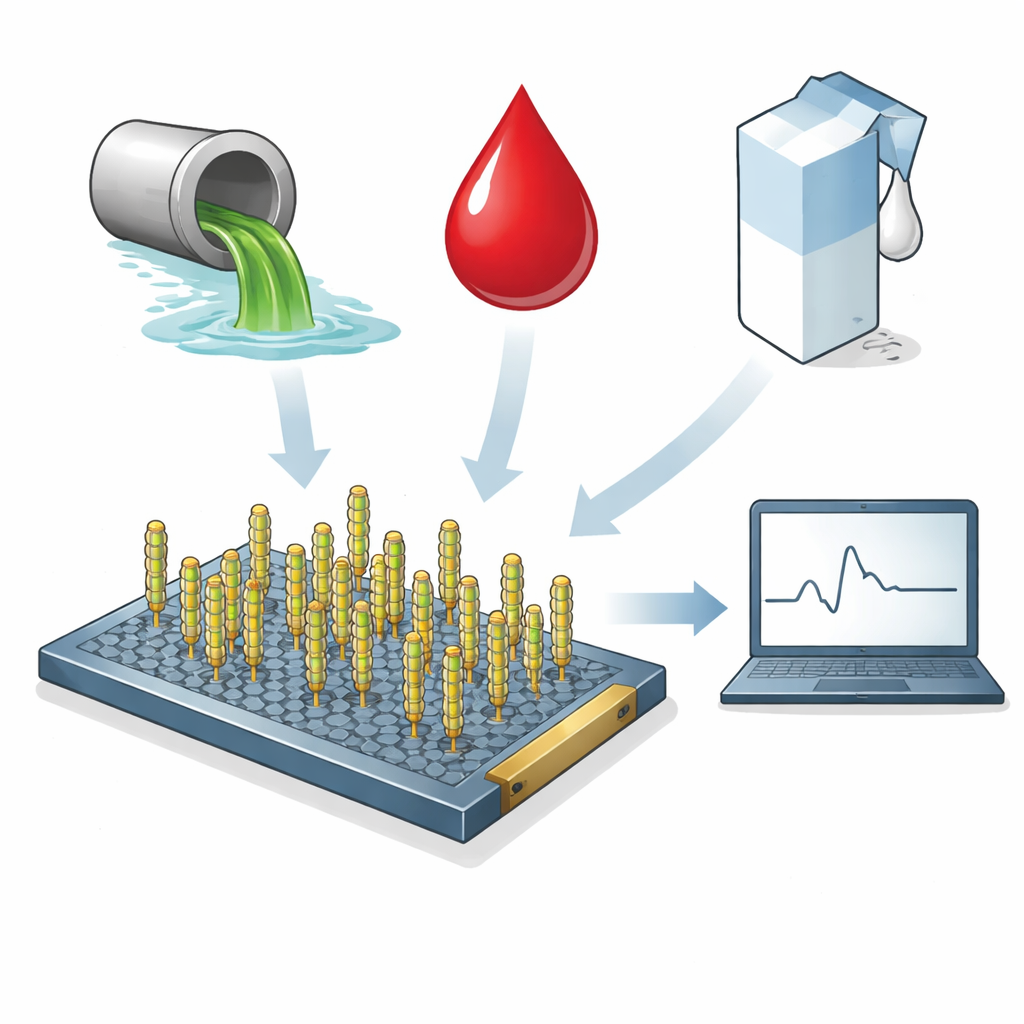
Przekształcenie niegroźnego wirusa w inteligentny detektor
W sercu urządzenia znajduje się M13, niegroźny wirus, który na ogół infekuje bakterie. Jego długie, cylindryczne ciało pokryte jest wieloma identycznymi białkami osłonkowymi, które naukowcy mogą modyfikować genetycznie. Zespół wstawił krótki, zaprojektowany peptyd na jedno z tych białek, tak aby cząstki M13 rozpoznawały i wiązały fragment S1 białka kolca koronawirusa. Druga wersja wirusa, niosąca „pogrubiony” (scrambled) peptyd, posłużyła jako kontrola, by pokazać, że odpowiedź wynika z rzeczywistego rozpoznania, a nie przypadkowego przylegania.
Budowa na atomowo cienkiej warstwie węgla
Aby przekształcić programowalny wirus w czujnik, badacze przytwierdzili go do płaskiej folii zredukowanego tlenku grafenu — wysoko przewodzącej formy węgla otrzymywanej przez chemiczną obróbkę grafitu. Po naniesieniu tlenku grafenu na małe szklane płytki i podgrzaniu w celu przekształcenia go w zredukowany tlenek grafenu, dodano cząsteczkę łącznika, która przylega do powierzchni węglowej i jednocześnie wiąże grupy aminowe na wirusie. W ten sposób powstała gęsta warstwa cząstek M13 zakotwiczonych na przewodzącej warstwie. Mikroskopia elektronowa i sił atomowych potwierdziły, że każdy etap wytwarzania zmienia powierzchnię zgodnie z oczekiwaniami, a pomiary elektryczne wykazały, że dodanie łącznika, a następnie wirusa stopniowo zwiększało oporność — znak, że powierzchnia została skutecznie pokryta.
Odczytywanie wiązania wirusa jako impulsu elektrycznego
W przeciwieństwie do wielu biosensorów, które potrzebują dodatków chemicznych lub ruchomych elementów, ta platforma działa jako prosty rezystor przy niewielkim stałym napięciu. Gdy białko S1 osiada na powierzchni pokrytej wirusem i wiąże się z prezentowanym peptydem, nieznacznie zmienia sposób, w jaki ładunek przemieszcza się przez warstwę grafenu. Objawia się to jako krótkotrwały pik w prądzie elektrycznym, który pojawia się mniej więcej 300 milisekund po naniesieniu kropli próbki na układ, a następnie zanika, gdy system się stabilizuje. Poprzez strojenie przyłożonego napięcia zespół znalazł optymalne warunki przy około −0,8 milivolta, gdzie sygnał pochodzący z rzeczywistego wiązania S1 był silny, podczas gdy szum tła i reakcje na niepowiązane białka, takie jak albumina surowicy wołowej, pozostawały niskie.
Praca w złożonych próbkach rzeczywistych
Następnie badacze poddali sensor próbom z rodzajami złożonych mieszanin, które często zawodzą delikatne odczynniki laboratoryjne. Testowali urządzenie w buforze, ściekach komunalnych, płodowej surowicy wołowej (jako zamiennik krwi) oraz mleku pasteryzowanym, z dodatkiem i bez dodatku białka S1. Używając statystycznie określonego progu do oznaczania wyniku pozytywnego, sensor wykrywał niezwykle niskie poziomy białka w prostym buforze — aż do około 10⁻⁴ pikograma na mililitr — porównywalnie z lub lepiej niż wiele systemów opartych na przeciwciałach. W ściekach urządzenie niezawodnie sygnalizowało wyższe poziomy S1, natomiast w surowicy i mleku konsekwentnie wykrywało także niższe stężenia, wszystko w ułamku sekundy. Co ważne, sensor kontrolny z wirusem ze „scrambled” peptydem wykazywał słabą odpowiedź na S1, potwierdzając, że sygnał zależy od zaprojektowanej sekwencji wiążącej. Równoległy sensor wykorzystujący konwencjonalne przeciwciało na tej samej platformie grafenowej działał podobnie, co sugeruje, że system oparty na wirusie może dorównać czułości przeciwciał przy jednoczesnym potencjale niższych kosztów i łatwiejszej produkcji.

Co to może znaczyć dla codziennych testów
Przeciwciała, podstawowe narzędzie wielu diagnostyk, są kosztowne w produkcji, wrażliwe na temperaturę i zazwyczaj wymagają chłodnego łańcucha dostaw od fabryki do gabinetu. W przeciwieństwie do nich wirusy M13 można hodować w bakteriach jak prostą kulturę, tolerują one surowsze warunki i można je przeprogramowywać przez modyfikację ich kodu genetycznego. Łącząc tę odporność i elastyczność z szybkim, niskomocowym odczytem elektronicznym na grafenie, badanie kreśli drogę do przenośnych, niskokosztowych urządzeń, które można by dostosowywać do wykrywania wielu różnych markerów chorób lub zanieczyszczeń po prostu przez zmianę prezentowanego peptydu. Praca pozostaje na etapie dowodu koncepcji i nie była jeszcze testowana na próbkach klinicznych od ludzi, ale wskazuje na przyszłość, w której przenośne sensory mogłyby w ciągu sekund przesiewać obecność białek wirusowych i innych biomarkerów w przychodniach, kanałach ściekowych czy produktach spożywczych, bez logistycznego obciążenia tradycyjnych testów opartych na przeciwciałach.
Cytowanie: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Słowa kluczowe: biosensor, grafen, bakteriofag, SARS-CoV-2, detekcja elektrochemiczna