Clear Sky Science · pl
Obrazowanie czasu życia fluorescencji bez znaczników pozwala odróżnić nowotwór od tkanki zdrowej w spontanicznie występujących psich nowotworach jamy ustnej
Widzieć raka w nowym świetle
Nowotwory jamy ustnej zarówno u ludzi, jak i u zwierząt domowych są wyjątkowo trudne do całkowitego usunięcia. Chirurdzy muszą wycinać szerokie „bezpieczne” marginesy wokół guza, aby nie pozostawić ukrytych komórek nowotworowych, ale w obrębie jamy ustnej może to oznaczać utratę istotnej kości, zębów i tkanek miękkich wpływających na jedzenie i mowę. W tym badaniu wykorzystano metodę obrazowania opartą na świetle stosowaną podczas operacji u psów domowych, która mogłaby pomóc chirurgom w czasie rzeczywistym odróżniać tkankę nowotworową od zdrowej — potencjalnie oszczędzając więcej prawidłowej tkanki przy jednoczesnym utrzymaniu kontroli nad rakiem.
Dlaczego krawędzie guzów są tak trudne do zlokalizowania
W chirurgii głowy i szyi dziś lekarze często polegają na szybkiej analizie zamrożonych wycinków, aby ocenić, czy brzegi usuniętego guza są naprawdę wolne od nowotworu. Ten proces jest powolny, obejmuje jedynie małe obszary i może przeoczyć chorobę. Podobne wyzwania dotykają leczenia psów z guzami jamy ustnej, gdzie lokalne nawroty pozostają częste. Ponieważ nie ma wiarygodnego sposobu „zobaczenia” mikroskopowego raka podczas operacji, chirurdzy zwykle usuwają szerokie marginesy, co może upośledzać żucie, połykanie i wygląd. Autorzy postanowili przetestować nieinwazyjne podejście obrazowe, które mogłoby wyznaczyć wyraźniejszą granicę między rakiem a tkanką normalną bezpośrednio na sali operacyjnej.
Wykorzystanie naturalnego blasku jako przewodnika chirurgicznego
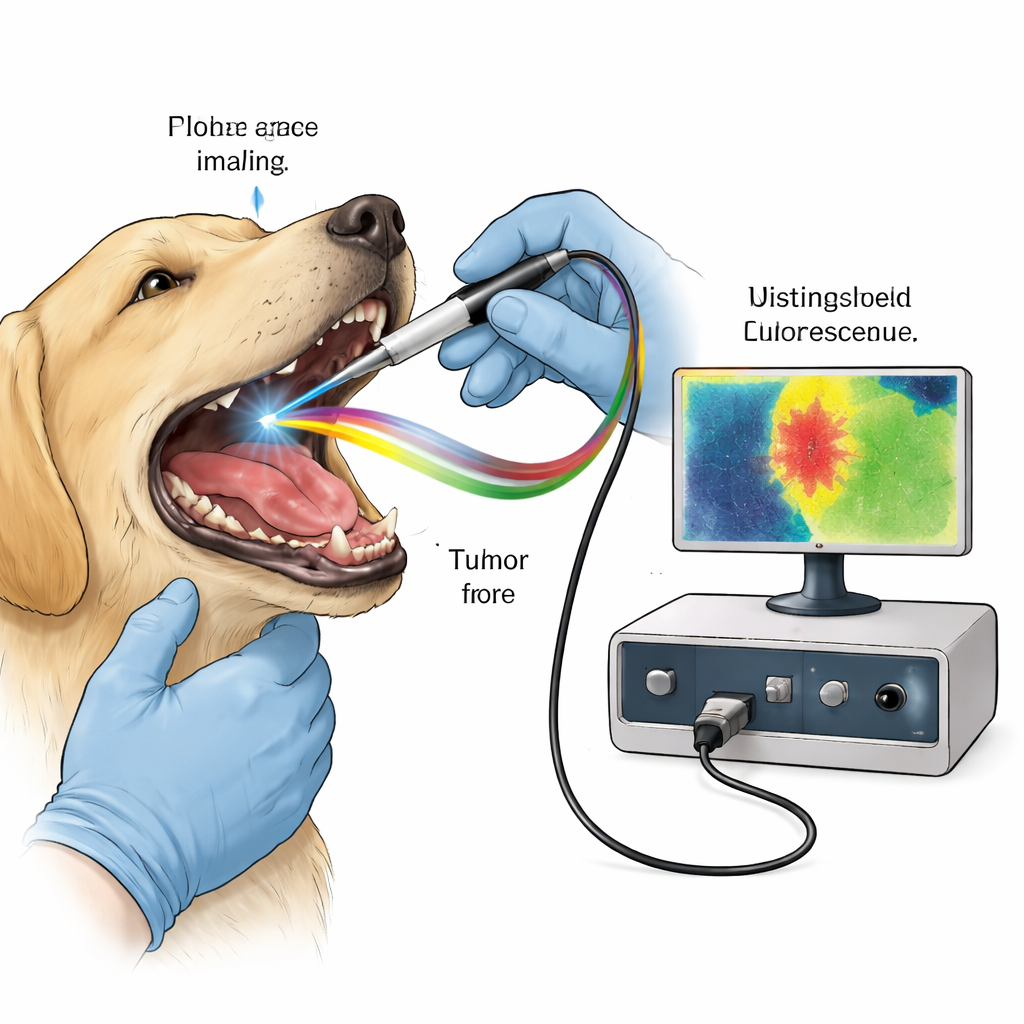
Wiele cząsteczek w naszych tkankach naturalnie emituje słabe światło fluorescencyjne po wzbudzeniu krótkim impulsem lasera. Kolagen w tkance łącznej oraz cząsteczki związane z metabolizmem komórkowym, takie jak NADH i FAD, mają charakterystyczne barwy i czasy zaniku tego blasku. Rak zaburza strukturę tkanki i zużycie energii, subtelnie zmieniając ten fluorescencyjny odcisk palca. Obrazowanie czasu życia fluorescencji (FLIm) mierzy nie tylko jak jasno tkanka świeci, ale także jak długo ten blask trwa w nanosekundach (czyli miliardowych częściach sekundy) — właściwość mniej zależną od warunków oglądania. Zespół użył spersonalizowanej ręcznej sondy, która kieruje szybkie ultrafioletowe impulsy w obszar guza u uśpionych psów i rejestruje powracającą fluorescencję w trzech kanałach spektralnych dostrojonych do kolagenu, związków metabolicznych i czerwono emitującego związku zwanego protoporfiryną IX (PpIX).
Dodawanie barwnika celującego w raka: pomoc czy szum?
PpIX może kumulować się w wielu guzach po podaniu pacjentowi doustnego proleku, kwasu 5-aminolewulinowego (5-ALA). Pod niebieskim światłem obszary bogate w PpIX często świecą jaskrawym różem i są wykorzystywane przez chirurgów do wykrywania nowotworu. Badacze najpierw potwierdzili w liniach komórkowych psiego raka jamy ustnej, że 5-ALA prowadzi do silnej fluorescencji PpIX i wykazali, że geny zaangażowane w produkcję i import 5-ALA są bardziej aktywne w komórkach nowotworowych. Następnie zrekrutowali 15 psów domowych z naturalnie występującymi guzami jamy ustnej i podali im 5-ALA na kilka godzin przed operacją. Na sali operacyjnej większość guzów widocznie fluorescencjonowała, ale niektóre zmiany zapalne lub wirusowe niebędące nowotworem również się świeciły, co sugeruje, że sama widoczna barwa może nie być niezawodnym wskaźnikiem granic guza.
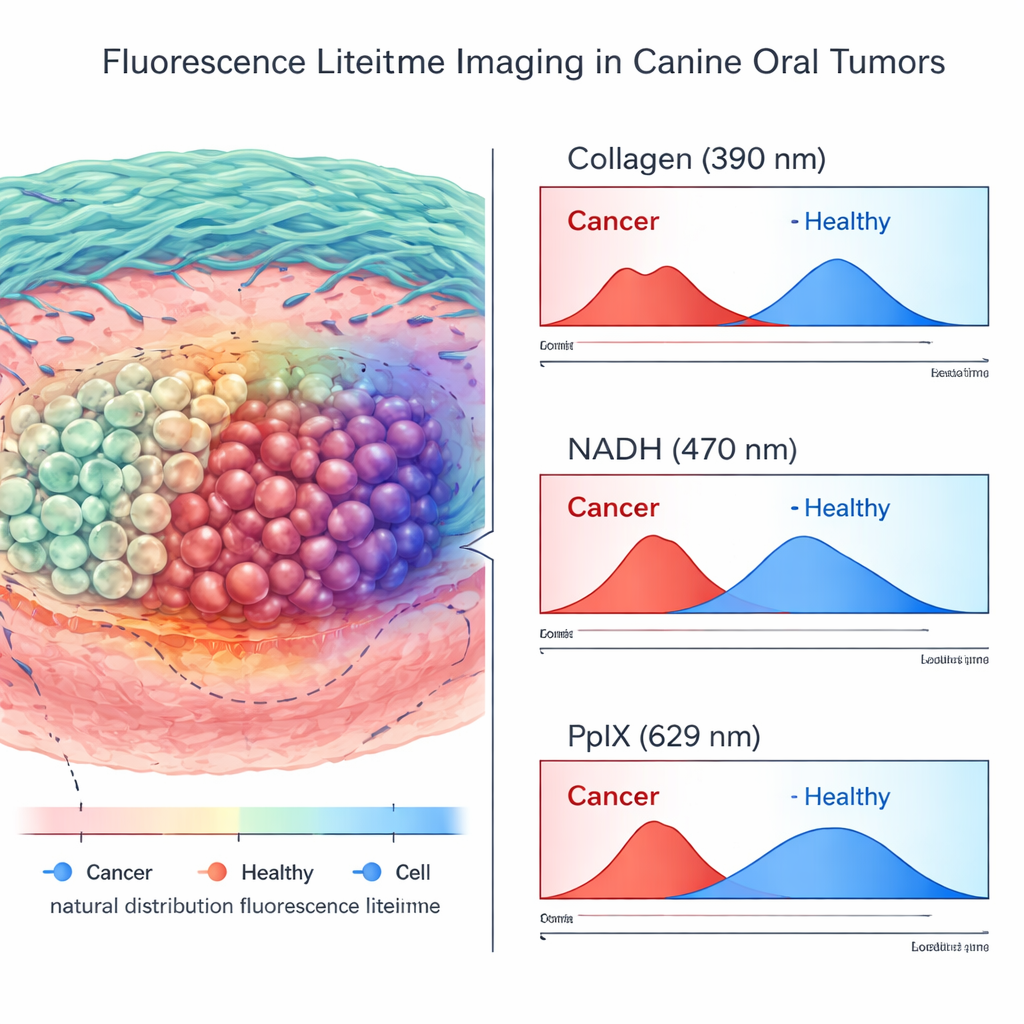
Co ujawniły obrazy czasu życia
Na podstawie ponad 200 000 wysokiej jakości punktów pomiarowych pochodzących z guzów i pobliskich tkanek prawidłowych zespół porównał sygnały FLIm ze szczegółowymi mapami patologicznymi. Stwierdzili, że wiele cech związanych z czasem życia i intensywnością różniło się istotnie między tkanką nowotworową a zdrową. Jednak najsilniejsze i najbardziej spójne rozróżnienie pochodziło z kanałów bez znaczników: krótsze czasy życia w paśmie czułym na kolagen oraz charakterystyczne przesunięcia w paśmie czułym na NADH były ściśle powiązane z obecnością raka. Natomiast kanał PpIX — ten wzmacniany przez podany 5-ALA — dostarczał mniej wiarygodnych informacji in vivo. Jego pomiary wykazywały dużą zmienność w obszarach normalnych, prawdopodobnie dlatego, że zapalone dziąsła i błony śluzowe albo kumulowały 5-ALA, albo zawierały naturalnie fluorescencyjne porfiryny naśladujące sygnał guza.
Od sali operacyjnej do stołu i z powrotem
Gdy badacze obrazowali usunięte próbki na stole przygotowawczym, obraz nieco się zmienił. Poza ciałem niektóre cechy oparte na PpIX stały się bardziej użyteczne do rozróżniania tkanki nowotworowej od zdrowej, co sugeruje potencjalną rolę w „przykrzesłowych” (chairside) kontrolach marginesów. Mimo to, po zastosowaniu zaawansowanych modeli statystycznych i uczenia maszynowego, najlepiej działające klasyfikatory zarówno dla danych pozyskanych w trakcie zabiegu, jak i poza nim, opierały się głównie na naturalnych sygnałach autofluorescencji, a nie na dodanym barwniku. FLIm bez znaczników osiągnęło przyzwoitą dokładność w odróżnianiu raka od tkanki normalnej samodzielnie, podczas gdy dodanie PpIX wniosło niewiele, a czasem wprowadzało zamieszanie.
Co to oznacza dla przyszłych operacji
Dla właścicieli zwierząt, a ostatecznie dla pacjentów ludzkich, kluczowy przekaz jest taki, że chirurdzy mogą kiedyś dysponować narzędziem świetlnym pomagającym zobaczyć, gdzie kończy się rak, a zaczyna tkanka zdrowa, bez polegania na dodatkowych lekach czy barwnikach. Prace na psach — realistycznym modelu dużego zwierzęcia dla ludzkiego raka jamy ustnej — pokazują, że własne sygnatury fluorescencyjne organizmu mogą wystarczyć do kierowania decyzjami na sali operacyjnej. Dodanie 5-ALA i PpIX w tym kontekście nie poprawiło na tyle dokładności, by uzasadnić dodatkowe koszty, złożoność i potencjalne skutki uboczne. Autorzy wnioskują, że przyszłe wysiłki powinny skoncentrować się na udoskonalaniu samego bezznacznikowego obrazowania czasu życia fluorescencji — możliwie z dopasowaniem analizy do konkretnych miejsc anatomicznych — zamiast polowania na kolejne środki kontrastowe. Jeśli się powiedzie, taka technologia mogłaby zmniejszyć liczbę powtórnych operacji i zachować więcej prawidłowej tkanki przy jednoczesnym utrzymaniu kontroli nad rakiem.
Cytowanie: Goldschmidt, S., Marcu, L., Ehrlich, K. et al. Label-free fluorescence lifetime imaging can distinguish cancer from healthy tissue in spontaneously occurring canine oral tumors. Sci Rep 16, 6077 (2026). https://doi.org/10.1038/s41598-026-37001-3
Słowa kluczowe: obrazowanie nowotworów jamy ustnej, psie guzy jamy ustnej, czas życia fluorescencji, marginesy chirurgiczne, 5-ALA PpIX