Clear Sky Science · pl
Sekwencjonowanie ampliconów za pomocą technologii Oxford Nanopore jako alternatywa diagnostyczna dla małych lentivirusów przeżuwaczy u owiec
Ukryte zakażenia w codziennym stadzie owiec
Owce na całym świecie skrycie noszą wirusy, które mogą osłabiać ich kondycję, skracać życie i powodować straty finansowe dla hodowców — często bez wyraźnych objawów przez lata. Badanie to bada nową metodę wykrywania tych ukrytych zakażeń przy użyciu przenośnej technologii sekwencjonowania DNA, oferując potencjalny przełom w ochronie dobrostanu zwierząt, dochodów gospodarstw, a nawet bezpieczeństwa żywnościowego.
Wolna, kosztowna choroba trudna do zauważenia
Praca koncentruje się na małych lentivirusach przeżuwaczy (SRLV), grupie wirusów zakażających owce i kozy. U owiec wywołują one chorobę Maedi-Visna — przewlekłe zakażenie, które może prowadzić do problemów z oddychaniem, zapalenia stawów, chorób mózgu oraz przewlekłego zapalenia wymion. Wiele zakażonych zwierząt nigdy nie wykazuje wyraźnych objawów, a mimo to wirus obniża produkcję mleka, zwiększa śmiertelność jagniąt i wymusza przedwczesne ubój. W niektórych europejskich stadach mlecznych, w tym w Hiszpanii i Grecji, około połowa zwierząt może być zakażona, co czyni to jedną z najważniejszych chorób owiec w intensywnych gospodarstwach.
Dlaczego obecne testy nie wykrywają wielu zakażonych zwierząt
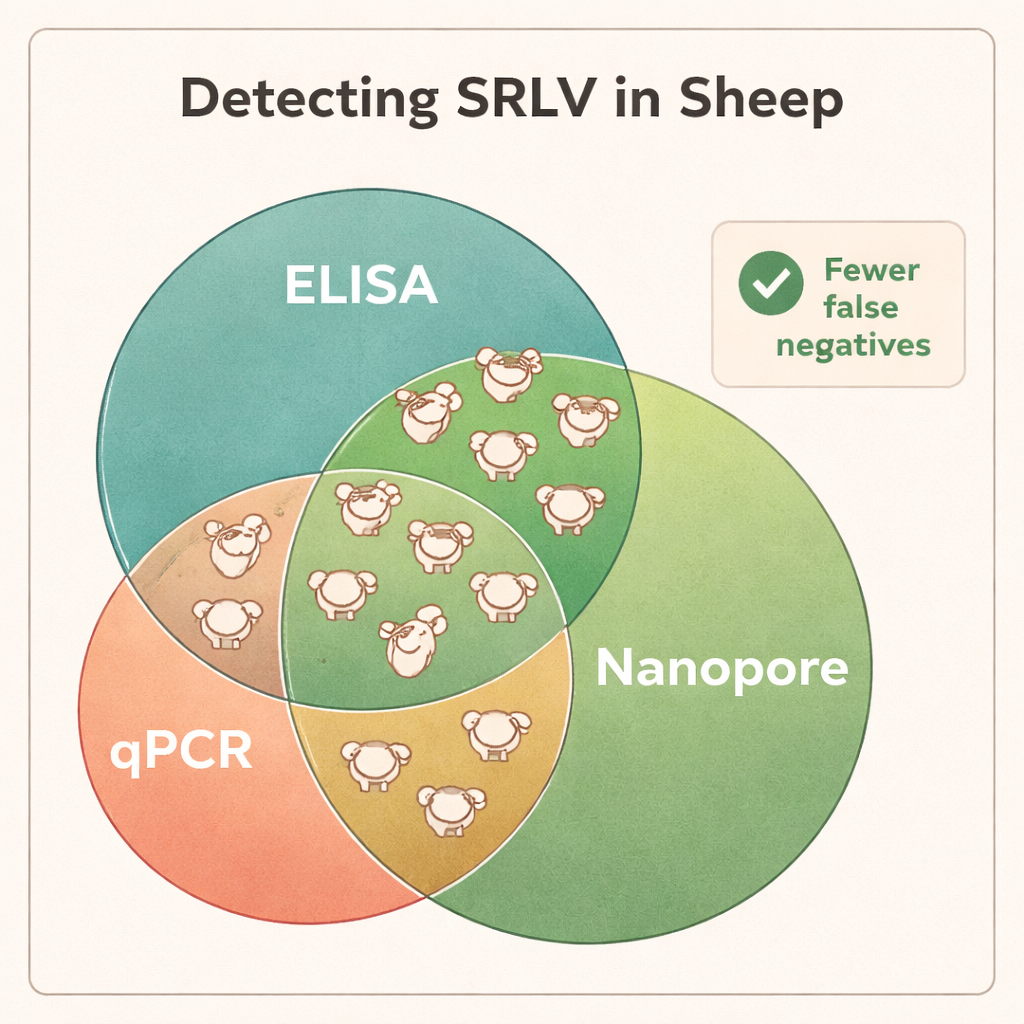
Obecnie gospodarstwa głównie polegają na badaniach krwi wykrywających przeciwciała (ELISA) lub na standardowych testach DNA (qPCR), aby ustalić, które zwierzęta są zakażone i powinny zostać usunięte z stada. Jednak SRLV szybko mutują i rekombinują, tworząc wiele nieco różnych wariantów wirusa. Niektóre warianty są słabo rozpoznawane przez testy serologiczne, a niektóre zakażone owce w ogóle nie rozwijają silnej odpowiedzi przeciwciał. qPCR, który celuje w krótkie i bardzo specyficzne fragmenty DNA wirusa, także może zawieść, jeśli te docelowe regiony ulegną zmianie. W efekcie wiele rzeczywiście zakażonych zwierząt daje wynik ujemny i pozostaje w stadzie, cicho rozprzestrzeniając wirusa.
Wykorzystanie sekwencjonowania w czasie rzeczywistym do wykrywania wirusa
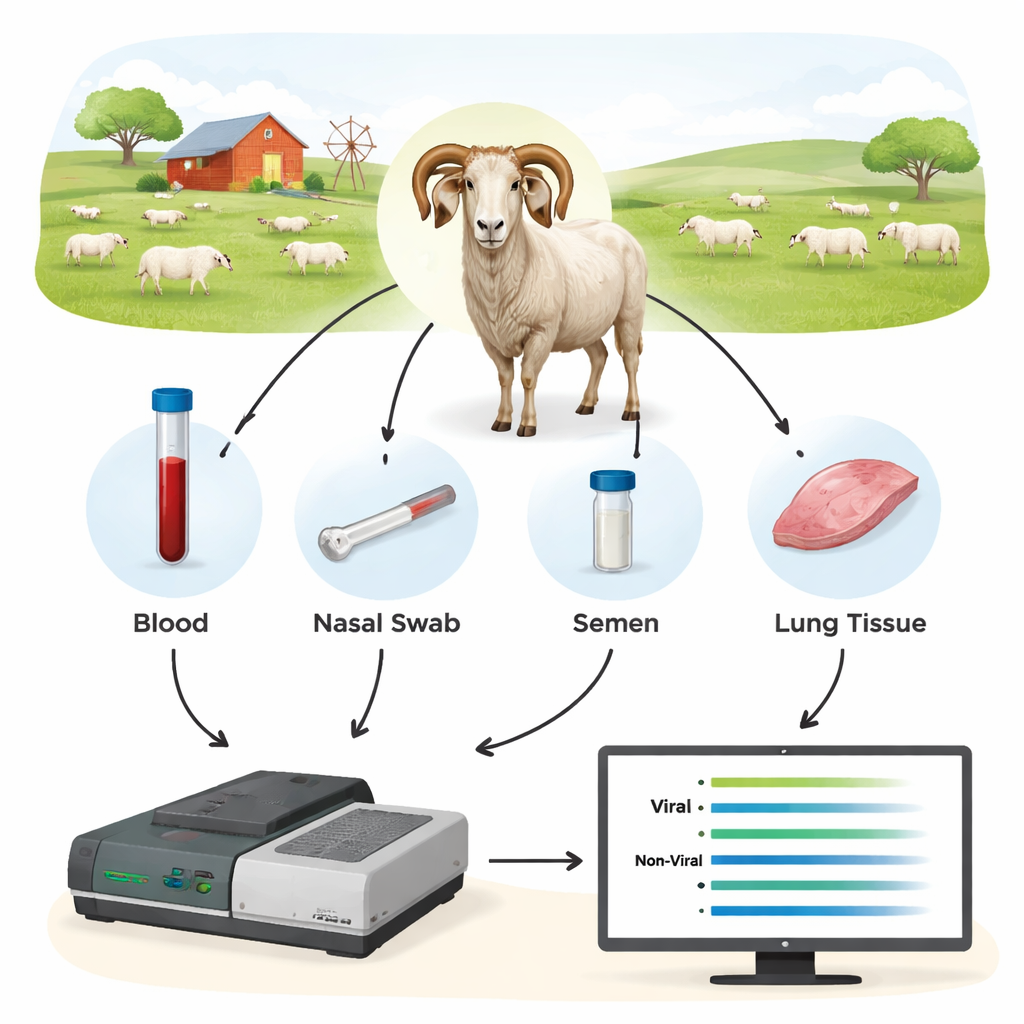
Naukowcy przetestowali trzecią generację metody DNA, zwaną sekwencjonowaniem Oxford Nanopore, jako nowy rodzaj narzędzia diagnostycznego. Zamiast szukać jednego, małego fragmentu DNA wirusa, najpierw amplifikowali dłuższe odcinki kluczowych genów wirusowych z prób zwierząt, a następnie sekwencjonowali te fragmenty w czasie rzeczywistym na urządzeniu Nanopore. Zebrali krew, wymazy z nosa, nasienie oraz komórki z krwi i płuc od 44 tryków i dodatkowych owiec, z których wiele było już testowanych metodami konwencjonalnymi. Skupiając się na regionach wirusa, które są stosunkowo zachowane, ale wystarczająco długie, by ujawnić dokładny szczep, zespół mógł zarówno wykryć zakażenie, jak i zidentyfikować, jakie typy wirusa występują.
Krew sprawdza się najlepiej — i wykrywa to, co pomijają inne testy
Sekwencjonowanie wykazało, że DNA z pełnej krwi było najbardziej wiarygodnym materiałem do wykrywania SRLV, mimo że wirus żyje głównie w niewielkiej podgrupie białych krwinek. Tkanka płuc od silnie zakażonych zwierząt dawała bardzo duże ilości DNA wirusowego, lecz takie próbki są dostępne dopiero po uboju. W przeciwieństwie do tego wymazy z nosa, nasienie i oczyszczone białe krwinki dostarczały zbyt mało materiału wirusowego do konsekwentnej diagnostyki. Porównując wyniki Nanopore z standardowymi testami ELISA i qPCR, różnice były uderzające: sekwencjonowanie Nanopore potwierdziło zakażenie u wszystkich tryków z wynikiem ELISA pozytywnym, ale także ujawniło, że wiele zwierząt z wynikiem ELISA negatywnym było w rzeczywistości zakażonych. W różnych stadach około 40–45% zwierząt oznaczonych przez ELISA jako „ujemne” okazało się nosicielami wirusa, a qPCR przegapił jeszcze większą część. Dane sekwencyjne ujawniły też współzakażenia różnymi typami SRLV u niektórych tryków — informacji, której tradycyjne testy łatwo nie dostarczają.
Od prostych odpowiedzi tak/nie do głębszych wniosków
Ponieważ Nanopore odczytuje rzeczywiste sekwencje wirusowe, może pójść dalej niż prosta diagnoza tak/nie. Zespół użył danych do porównania szczepów wirusa, budowy drzew filogenetycznych wirusów krążących w stadach oraz badania subtelnych różnic w białkach wirusowych, które mogą wyjaśniać, dlaczego niektóre zwierzęta umykają wykryciu przez standardowe testy ELISA. Wykazali, że pewne wersje kluczowego białka wirusowego, celowanego przez komercyjne testy przeciwciał, różnią się istotnie między zwierzętami z wynikiem ELISA pozytywnym i negatywnym. Z czasem takie informacje mogłyby pomóc udoskonalić zarówno testy serologiczne, jak i programy hodowlane mające na celu wybór zwierząt naturalnie bardziej odpornych na zakażenie.
Co to oznacza dla hodowców i zdrowia zwierząt
Dla osób niezajmujących się specjalistycznie tematem przekaz jest prosty: poprzez odczytywanie dłuższych fragmentów DNA wirusowego bezpośrednio, sekwencjonowanie Nanopore może wykryć więcej zakażonych owiec, wcześniej i dokładniej niż obecne rutynowe testy. Dodatkowo informuje, jakie dokładnie szczepy wirusa występują w stadzie. Chociaż podejście to jest nadal bardziej skomplikowane i kosztowne niż pojedyncie badanie krwi, technologia staje się coraz szybsza, tańsza i bardziej przenośna. Jeśli zostanie włączona do programów kontroli, może znacząco zmniejszyć liczbę „ukrytych” nosicieli, poprawić projekt szczepionek i testów oraz wspierać hodowlę odporniejszych zwierząt — czyniąc hodowlę owiec bardziej zrównoważoną i humanitarną.
Cytowanie: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Słowa kluczowe: zdrowie owiec, lentivirus, sekwencjonowanie nanopore, diagnostyka weterynaryjna, Maedi-Visna