Clear Sky Science · pl
Szerokospektralne nanocząstki przeciwmikrobowe o niskiej toksyczności zapobiegające tworzeniu biofilmu na urządzeniach urologicznych
Dlaczego implanty medyczne czasem odwracają się przeciwko nam
Nowoczesna medycyna opiera się na plastikowych rurkach i implantach do odprowadzania moczu, podpierania zablokowanych nerek i przywracania funkcji seksualnych. Te same urządzenia mogą jednak przyciągać bakterie, które budują śliskie, ochronne społeczności zwane biofilmami. Gdy biofilm się uformuje, infekcje są trudne do wyleczenia, często zmuszając lekarzy do usunięcia lub wymiany urządzenia. W tym badaniu opisano nowy rodzaj mikroskopijnej powłoki, zbudowanej ze złota i srebra pokrytych węglową otoczką, zaprojektowanej tak, by zapobiegać powstawaniu biofilmów już na wczesnym etapie.
Ukryty problem lepkich zarazków
Cewniki, stenty moczowodowe i nadmuchiwane protezy prącia pomagają setkom tysięcy pacjentów, ale także stanowią idealne miejsce dla drobnoustrojów. Bakterie przylegają do powierzchni urządzenia i wydzielają kleisto przypominającą matrycę z cukrów, białek i lipidów, tworząc twierdzę chroniącą je przed antybiotykami i układem odpornościowym. W rezultacie infekcje związane z urządzeniami stanowią ponad jedną czwartą wszystkich zakażeń szpitalnych i kosztują setki milionów dolarów rocznie. Obecne powłoki ochronne oparte na antybiotykach lub prostym srebrze mają trudności z długoterminowym zapobieganiem biofilmom i mogą przyczyniać się do rosnącej oporności na antybiotyki.
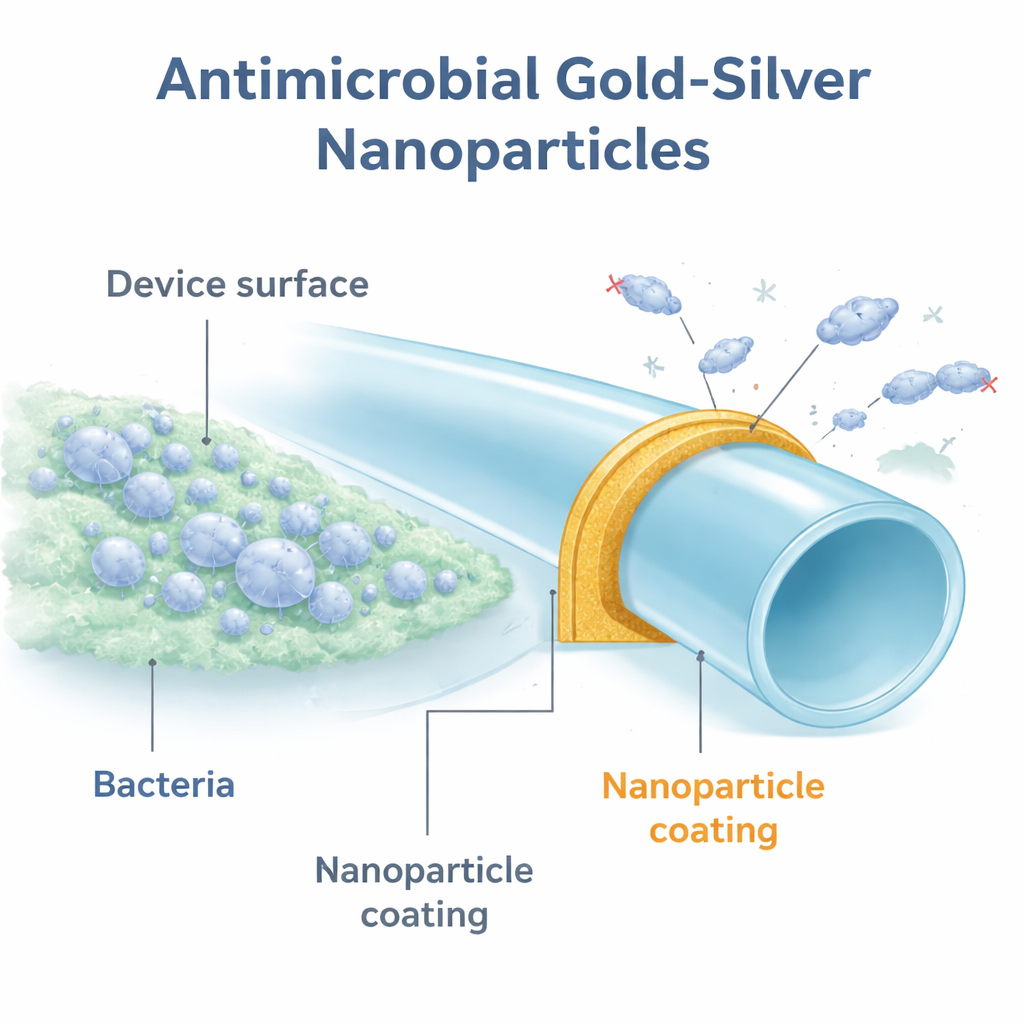
Nowy rodzaj ochronnej zbroi
Naukowcy skupili się na drobnych cząstkach metalu o rozmiarach zaledwie kilku miliardowych części metra. Te nanocząstki zostały zbudowane wokół węglowej klatki zwanej polihydroksy-fullerenem, znanej z niskiej toksyczności i zdolności do poprawiania właściwości niektórych metali. Stworzono kilka wersji z różnymi metalami, a następnie pokryto nimi małe dyski z poliuretanu — plastiku powszechnie stosowanego w urządzeniach urologicznych. Testy powleczonych dysków przeciwko standardowemu szczepowi Escherichia coli wykazały, że tylko cząstki zawierające srebro mają silne działanie bakteriobójcze. Wyraźnie wyróżniała się kombinacja złota i srebra, określana jako GSNP, która zmniejszała liczbę bakterii nawet do 100 000 razy w porównaniu z niepowleczonym plastikiem.
Powstrzymywanie rzeczywistych drobnoustrojów z urologii
Aby sprawdzić, czy efekt utrzymuje się poza szczepem laboratoryjnym, zespół przetestował najlepszą powłokę przeciw sześciu rodzajom bakterii pobranych bezpośrednio z zakażonych stentów moczowodowych i protez prącia. Były to zarówno gatunki Gram-dodatnie, jak i Gram-ujemne, znane z powodowania uporczywych zakażeń. Przy poziomach bakterii zbliżonych do tych obserwowanych u pacjentów powierzchnie powleczone GSNP osiągnęły 100% redukcję zarówno bakterii pływających w cieczy, jak i przylegających do powierzchni dla każdego badanego szczepu. W oddzielnych eksperymentach badacze wystawili bakterie na różne stężenia nanocząstek w zawiesinie i oszacowali, ile GSNP potrzeba do zahamowania wzrostu. Wszystkie szczepy były całkowicie zahamowane przy dawce równej lub niższej niż 3 mikrogramy GSNP na mililitr, przy czym niektóre organizmy Gram-dodatnie wymagały nieco wyższych ilości.
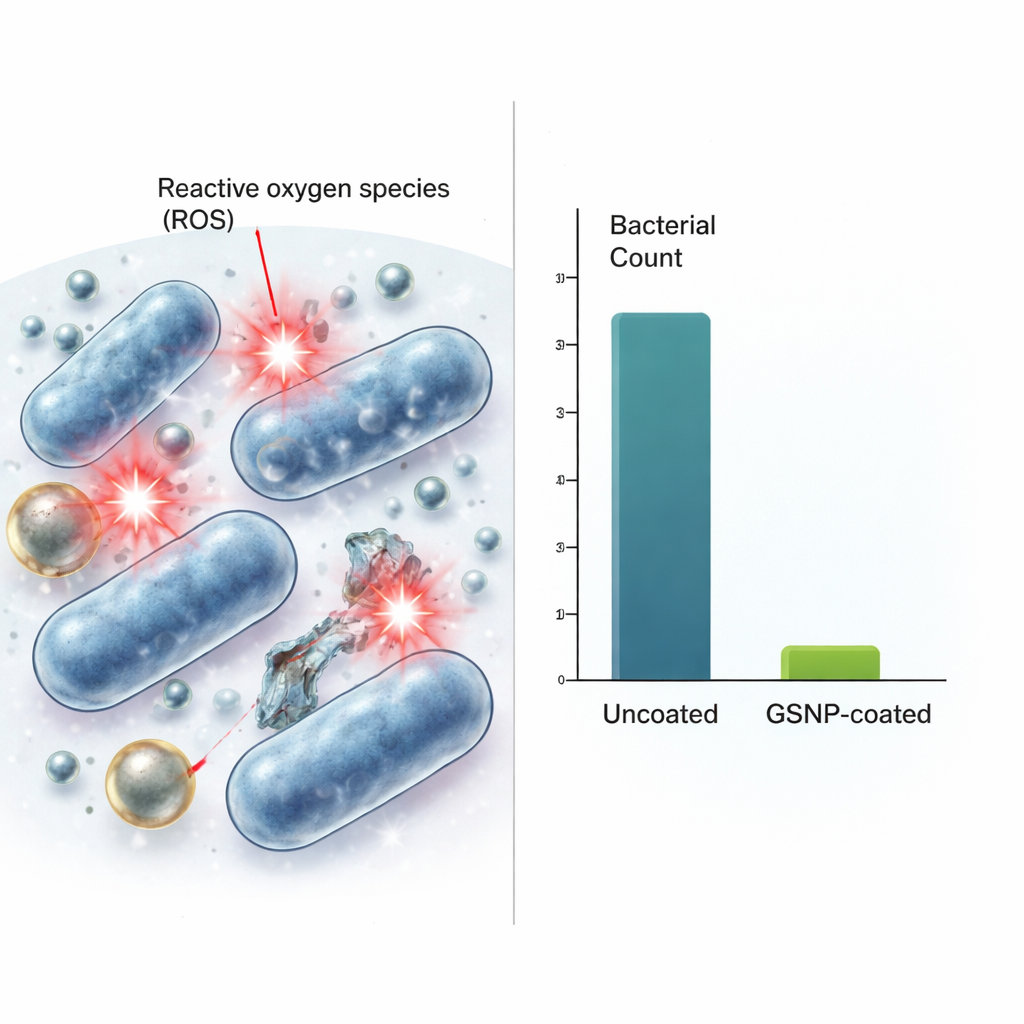
Jak działają i jak są bezpieczne
Zespół następnie badał, w jaki sposób te powłoki zabijają bakterie i czy mogą także szkodzić komórkom ludzkim. Dane wskazują na reaktywne formy tlenu — chemicznie reaktywne warianty tlenu — jako kluczowy element mechanizmu zabijania. Choć same nanocząstki nie generowały tych reaktywnych cząsteczek, bakterie wystawione na działanie GSNP wytwarzały znacznie wyższe poziomy niż bakterie nieleczone, co sugeruje, że cząstki wywołują szkodliwą chemię wewnątrz lub w pobliżu mikroorganizmów. Gdy komórki fibroblastów mysich były narażone na podobne lub wyższe stężenia GSNP, ponad 80% komórek przeżyło nawet przy najgorszej zbadanej dawce bakteriobójczej. Innymi słowy, poziomy zabijające bakterie miały jedynie umiarkowany wpływ na komórki ssacze. GSNP okazały się także dramatycznie skuteczniejsze niż porównywany komercyjny produkt z nanocząstkami złota–srebra, osiągając przy równoważnych dawkach około milion razy większą redukcję bakterii.
Co to może znaczyć dla pacjentów
Chociaż badania przeprowadzono w laboratorium, a nie jeszcze na zwierzętach czy ludziach, wyniki wskazują obiecującą nową strategię dla bezpieczniejszych implantów medycznych. Cienka warstwa GSNP na cewniku czy protezie mogłaby zapewnić szeroką ochronę przed wieloma różnymi bakteriami, zmniejszyć potrzebę usuwania urządzeń i zrobić to bez polegania na tradycyjnych antybiotykach. Powłoka wykorzystuje niewielkie ilości metalu, wykazuje stosunkowo niską toksyczność w testach inicjalnych i jest prosta w produkcji. Po dalszym dopracowaniu stabilności długoterminowej i starannym przebadaniu w realistycznych modelach, te powłoki z nanocząstek złota–srebra mogą pomóc utrzymać działanie istotnych urządzeń urologicznych dla pacjentów, zamiast stać się siedliskiem zakażeń.
Cytowanie: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Słowa kluczowe: biofilm, urządzenia urologiczne, powłoka przeciwdrobnoustrojowa, nanocząstki, złoto-srebro