Clear Sky Science · pl
Iloczynowa analiza proteomiczna osocza po zdalnym uwarunkowaniu niedokrwiennym w ostrym udarze niedokrwiennym
Dlaczego ściskanie ramienia może chronić mózg
Gdy ktoś ma udar spowodowany zatkaniem naczynia krwionośnego, każda minuta utraconego przepływu krwi zagraża komórkom mózgu. Standardowe leczenie ma na celu przywrócenie światła zablokowanej tętnicy, ale wielu pacjentów trafia do szpitala zbyt późno lub nie kwalifikuje się do niego. Naukowcy badają zaskakująco prostą terapię dodatkową: krótkotrwałe zatrzymanie przepływu krwi w ramieniu lub nodze za pomocą mankietu do mierzenia ciśnienia — strategię zwaną zdalnym uwarunkowaniem niedokrwiennym (remote ischemic conditioning, RIC). W tym badaniu postawiono kluczowe pytanie dla przekształcenia tej idei w realną terapię: co dokładnie RIC zmienia we krwi pacjentów po udarze i czy te zmiany mogą wskazać, kto mógłby najbardziej skorzystać?
Łagodny sygnał stresu wysyłany z kończyny do mózgu
RIC polega na wielokrotnym nadmuchiwniu mankietu na kończynie przez kilka minut, a następnie jego spuszczaniu, co tworzy krótkie, niegroźne epizody ograniczonego przepływu krwi. Badania na zwierzętach i wczesne próby kliniczne sugerują, że ten „kontrolowany stres” może wysyłać sygnały do odległych narządów, w tym mózgu, aktywując programy ochronne. W dużym badaniu klinicznym o nazwie RICAMIS pacjenci z umiarkowanym udarem niedokrwiennym, którzy otrzymali RIC oprócz standardowej opieki, mieli lepsze wyniki w 90. dobie niż ci otrzymujący tylko standardowe postępowanie. Jednak inne badanie (RESIST) nie wykazało takiej korzyści, co pozostawia lekarzy w niepewności, kiedy i dla kogo RIC działa. Aktualne badanie zagląda w krew pacjentów w poszukiwaniu molekularnych wskazówek — mierzalnych białek, czyli biomarkerów, które zmieniają się w czasie pod wpływem RIC.
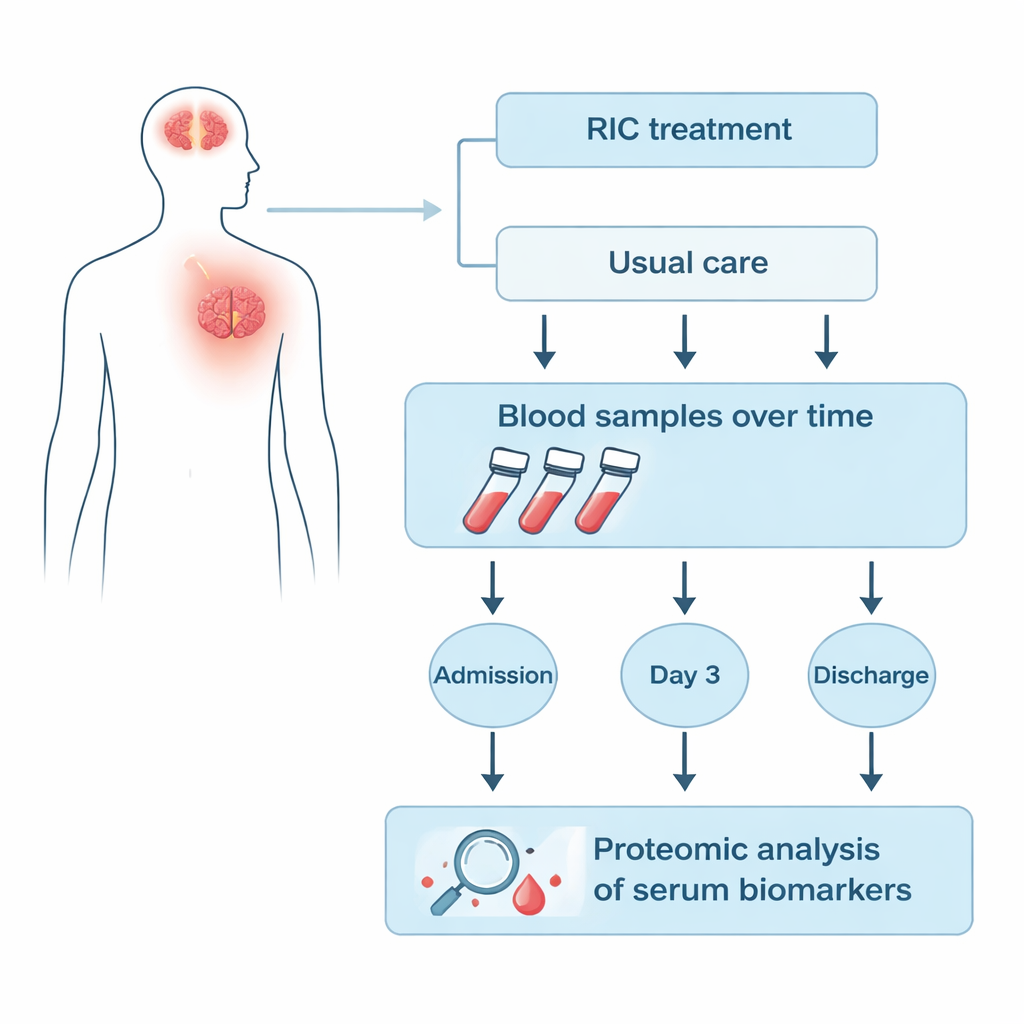
Śledzenie krwi pacjentów w trakcie pobytu w szpitalu
Naukowcy skupili się na 25 pacjentach z badania RICAMIS, u których pobierano próbki krwi w trzech punktach: przy przyjęciu, trzy dni po przypisaniu leczenia oraz przy wypisie ze szpitala. Dziewięciu pacjentów otrzymało RIC wraz z opieką standardową, a szesnastu — tylko opiekę standardową. Zastosowano technikę zwaną ilościową proteomiką, dzięki której zespół jednocześnie zmierzył setki białek w frakcji surowicy krwi, zamiast badać jedynie kilka uprzednio wybranych markerów. Następnie porównano, jak poziom każdego białka wzrastał lub spadał w czasie w grupie RIC w porównaniu z grupą kontrolną, aby odnaleźć sygnatury specyficzne dla RIC.
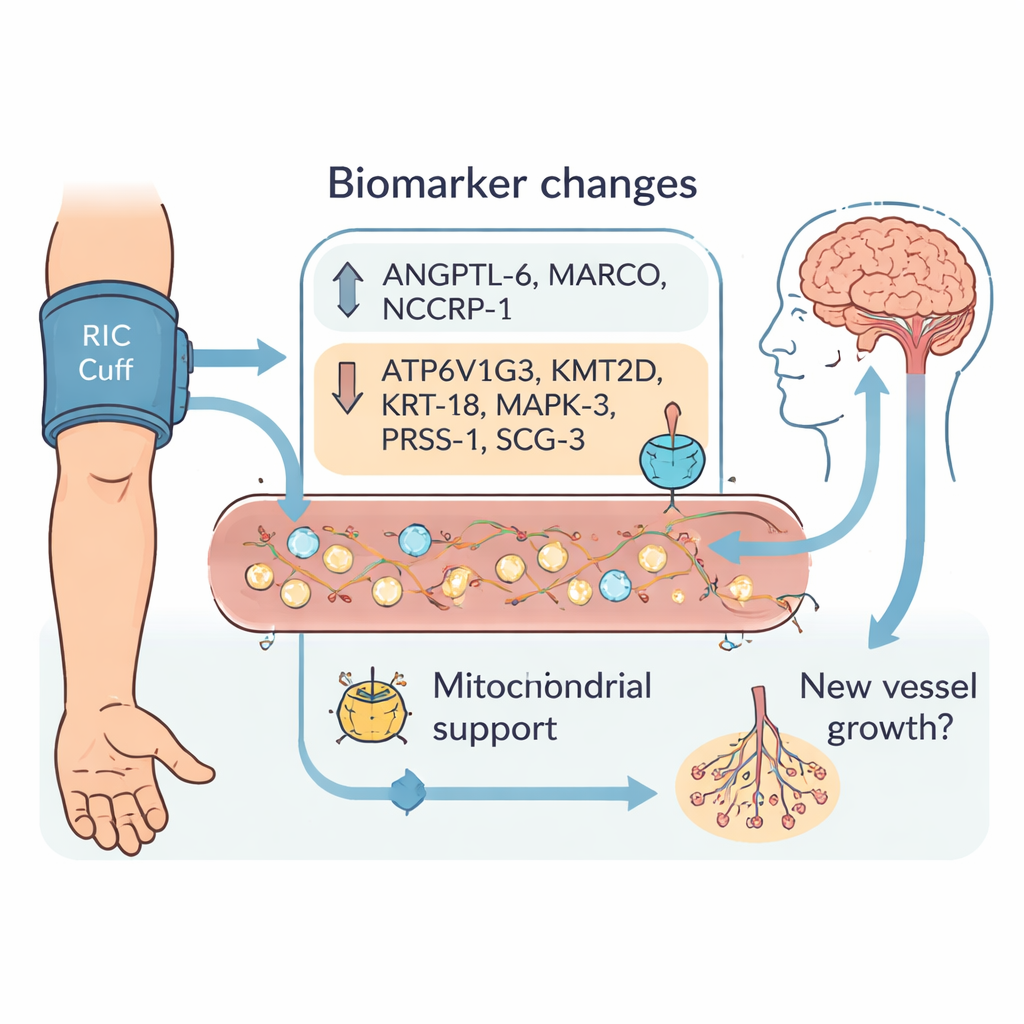
Dziewięć wyróżniających się sygnałów we krwi
W trakcie pobytu w szpitalu dziesiątki białek zmieniały się inaczej między obiema grupami. Po starannym przefiltrowaniu zespół wyróżnił dziewięć biomarkerów, których zmiany od przyjęcia do 3. dnia i do wypisu wyraźnie rozdzielały pacjentów poddanych RIC od kontrolnych. Trzy białka — ANGPTL‑6, MARCO i NCCRP‑1 — wzrosły silniej po RIC. Sześć innych — ATP6V1G3, KMT2D, KRT‑18, MAPK‑3, PRSS‑1 i SCG‑3 — miało tendencję do spadku. Wiele z tych cząsteczek bierze udział w regulacji gospodarki energetycznej komórek w mitochondriach oraz w procesach wzrostu i przebudowy naczyń. Zgadza się to z hipotezą, że RIC nie tylko chroni neurony przed uszkodzeniem, lecz także może pomagać uszkodzonym obszarom mózgu w reorganizacji, naprawie układu naczyniowego i przywracaniu funkcji w ciągu dni i tygodni.
Wskazówki dotyczące wykorzystania energii i wzrostu naczyń
Aby lepiej zrozumieć rolę tych dziewięciu białek, autorzy odwzorowali je na znanych ścieżkach biologicznych. Dwa z nich, KMT2D i MAPK‑3, są powiązane z tym, jak pakowane jest DNA i jak geny są włączane lub wyłączane, zwłaszcza w programach związanych ze wzrostem naczyń. Inne, jak ATP6V1G3 i KRT‑18, zostały wcześniej powiązane z utrzymaniem zdrowych mitochondriów i ochroną tkanki serca po urazie. Razem te wzorce sugerują, że RIC skłania organizm do bardziej efektywnego wykorzystania energii oraz sprzyja wzrostowi lub przebudowie naczyń — co może poprawiać przepływ krwi wokół obszaru uszkodzonego przez udar. Jednocześnie niektóre markery, takie jak NCCRP‑1 i MARCO, mogą odzwierciedlać ostry stres i odpowiedź immunologiczną organizmu na sam zabieg nadmuchiwania mankietu, podkreślając, że RIC wywołuje złożoną, ogólnoustrojową reakcję.
Co to znaczy dla przyszłej opieki nad udarami
To niewielkie badanie eksploracyjne nie może dowieść dokładnego mechanizmu ochrony mózgu przez RIC i obejmowało tylko 25 pacjentów z jednego kraju, więc wyniki wymagają potwierdzenia w dużo większych i bardziej zróżnicowanych grupach. Mimo to identyfikacja krótkiej listy dziewięciu białek, które konsekwentnie zmieniają się w przeciwnych kierunkach przy zastosowaniu RIC i bez niego, to ważny krok. W przyszłości takie biomarkery mogłyby pomóc lekarzom szybko ocenić, czy RIC „działa” u danego pacjenta, kierować wyborem osób, które powinny je otrzymać, a nawet zainspirować leki naśladujące korzystne efekty bez potrzeby stosowania mankietu. Na razie praca ta wzmacnia prostą, ale silną ideę: poprzez bezpieczne wywołanie stresu w jednej części ciała możemy skłonić mózg do stanu bardziej odpornego i lepiej zdolnego do regeneracji po udarze.
Cytowanie: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Słowa kluczowe: ostry udar niedokrwienny, zdalne uwarunkowanie niedokrwienne, biomarkery surowicy, analiza proteomiczna, neuroprotekcja