Clear Sky Science · pl
Prozapalna subpopulacja neutrofili napędza uszkodzenie jelit przy niedokrwieniu–reperfuzy za pośrednictwem szlaku stresu retikulum endoplazmatycznego zależnego od ATF4
Kiedy przepływ krwi rani jelito
Chirurdzy i lekarze intensywnej opieki od dawna zastanawiają się nad niebezpiecznym paradoksem: gdy dopływ krwi do jelita zostaje przerwany, a następnie przywrócony, samo przywrócenie przepływu może poważnie uszkodzić wyściółkę jelita. Proces ten, nazywany uszkodzeniem jelita wskutek niedokrwienia i reperfuzji, może prowadzić do zagrażających życiu powikłań, takich jak sepsa i niewydolność wielonarządowa. Streszczenie badania przedstawionego tutaj pokazuje, że nie wszystkie komórki układu odpornościowego, które przybywają na miejsce zdarzenia, są takie same — jedna szczególnie agresywna podgrupa białych krwinek odgrywa kluczową rolę w przemianie ratunkowej reakcji w szkodliwą.
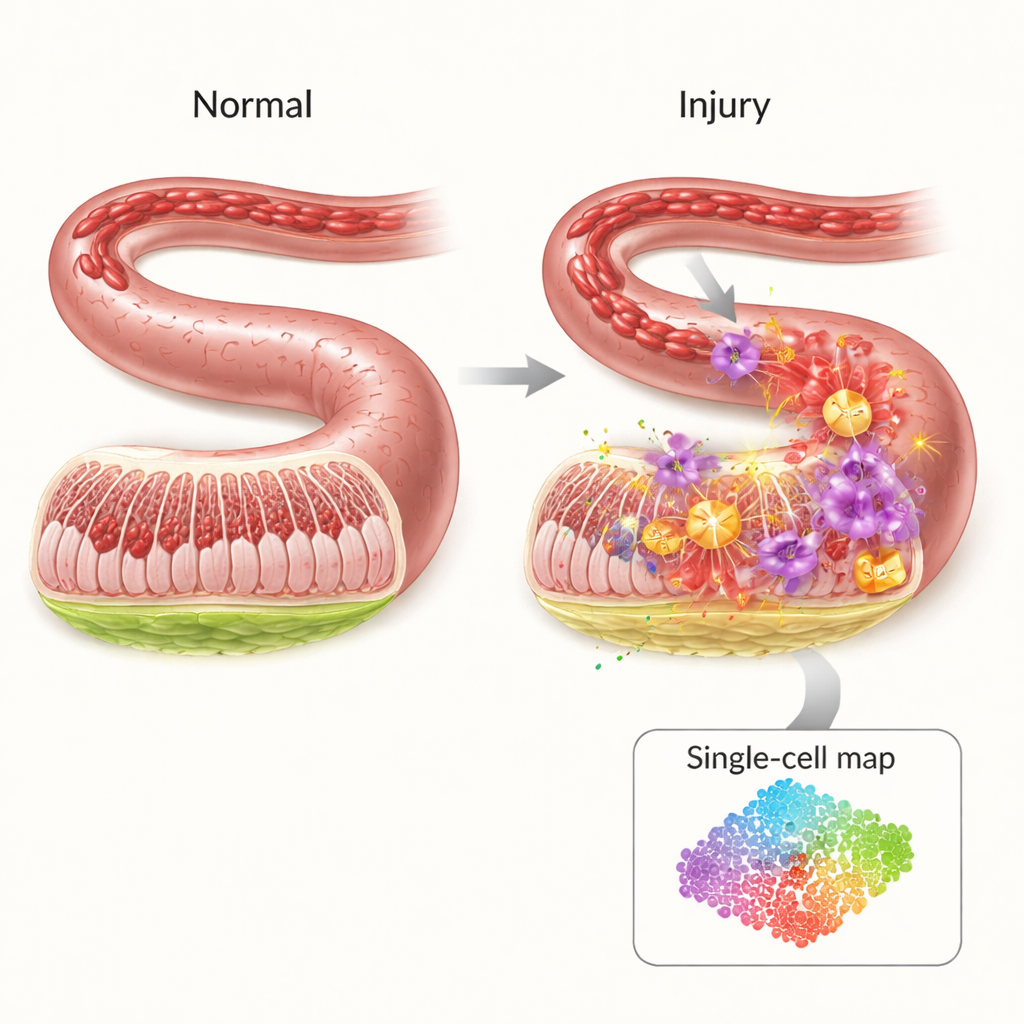
Krucha ochrona jelita
Wnętrze jelita wyłożone jest cienką, lecz wysoce zorganizowaną barierą, która utrzymuje bakterie i toksyny w świetle jelita, jednocześnie przepuszczając składniki odżywcze. Gdy przepływ krwi zostaje przerwany — na przykład podczas wstrząsu, dużej operacji czy ciężkiej traumy — bariera ta pozbawiona jest tlenu. Co zaskakujące, większość uszkodzeń nie zachodzi podczas samego braku dopływu krwi, lecz po przywróceniu krążenia. Nagły napływ tlenu i komórek odpornościowych wyzwala burzę sygnałów zapalnych i reaktywnych cząsteczek, które mogą powstawić ubytki w ścianie jelita, umożliwiając przenikanie drobnoustrojów do krwiobiegu. Pomimo klinicznego znaczenia, lekarze dysponują dziś niewieloma ukierunkowanymi metodami zapobiegania tej kaskadzie.
Przybliżenie na poziomie pojedynczych komórek
Aby ustalić, kto co robi podczas tego kryzysu, badacze zastosowali sekwencjonowanie RNA pojedynczych komórek, technikę odczytującą, które geny są aktywne w tysiącach pojedynczych komórek jednocześnie. W modelu myszy z niedokrwieniem i reperfuzją jelit porównali uszkodzone jelita z zdrowymi i zmapowali 19 głównych typów komórek. Stwierdzili, że niektóre komórki odpornościowe — szczególnie neutrofile i zapalne monocyty — znacznie się rozrosły po urazie, podczas gdy komórki ochronne, takie jak limfocyty T, B i komórki NK, zmalały. Sieci komunikacyjne między typami komórek również się przesunęły, z neutrofilami wyłaniającymi się jako centralne węzły wysyłające i odbierające liczne sygnały zapalne, co wskazuje na ich kluczową rolę w powodowaniu uszkodzeń.
Szkodliwa podgrupa komórek pierwszej linii
Neutrofile należą do najszybszych komórek reagujących, pędząc przez krwioobieg, by zwalczać infekcje i usuwać szczątki. Jednak to badanie pokazuje, że w populacji neutrofili istnieje szczególnie agresywna podgrupa odpowiedzialna za dużą część szkód wokół jelita. Gdy naukowcy usunęli neutrofile u myszy przed wywołaniem niedokrwienia i reperfuzji, zwierzęta miały mniejsze skrócenie jelita, niższe poziomy markerów uszkodzenia we krwi, lepszy wygląd tkanek w mikroskopie i bardziej szczelne białka uszczelniające w wyściółce jelita. W eksperymentach ko‑hodowli neutrofile pobrane od uszkodzonych myszy bezpośrednio szkodziły komórkom jelitowym, obniżając ich przeżywalność, zwiększając śmierć komórek i zaburzając kluczowe „zamkowe” białka, które utrzymują integralność bariery jelitowej.
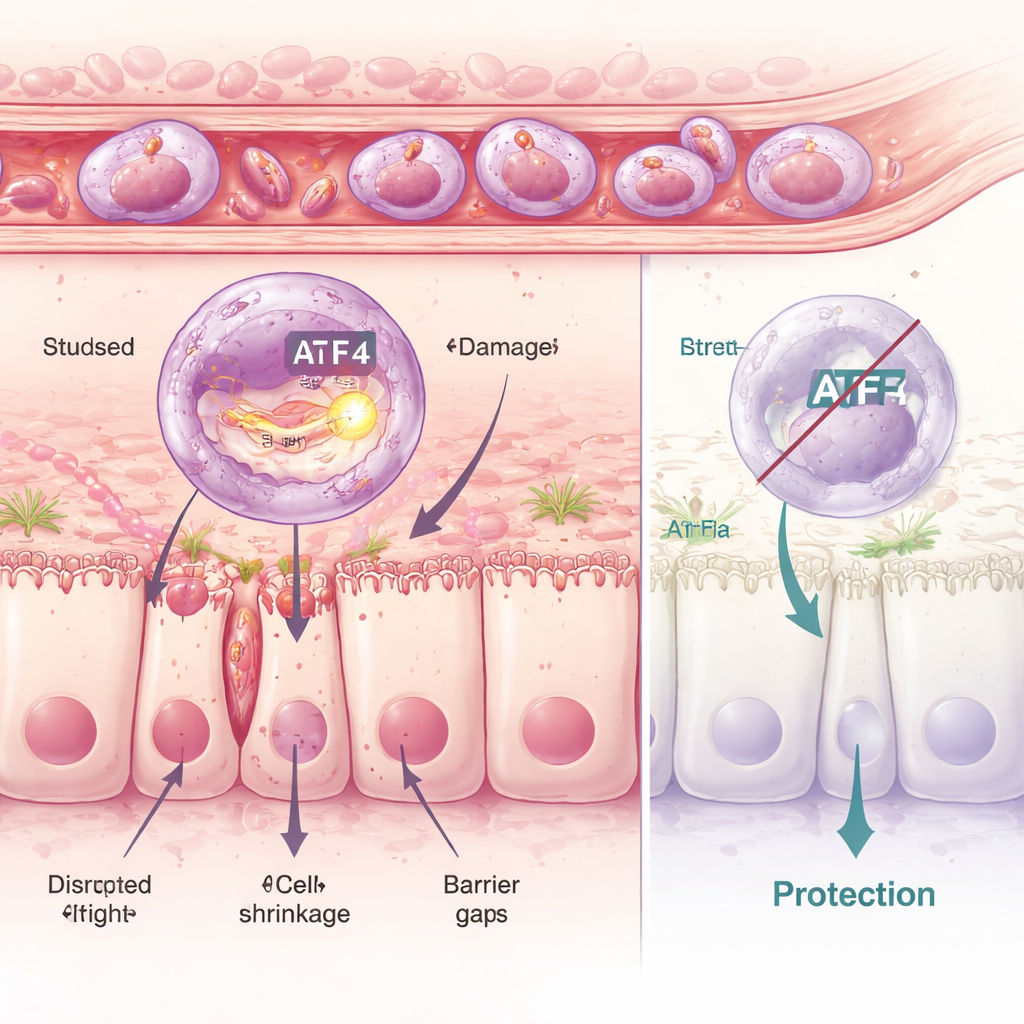
Stres wewnątrzkomórkowy: kiedy kontrola jakości zawodzi
Wnikliwiej badacze przyjrzeli się neutrofilom pojedynczo i zidentyfikowali sześć odrębnych podgrup. Jedna z nich, nazwana klastrem C5, wyróżniała się silnym profilem zapalnym i uruchomieniem molekularnego programu stresowego wewnątrz struktury zwanej retikulum endoplazmatycznym, warsztatu fałdowania białek w komórce. Kluczowym regulatorem tego programu jest białko o nazwie ATF4. W szkodliwych komórkach C5 ATF4 i jego geny docelowe były silnie aktywne. Stosując leki, które albo zwiększają, albo tłumią tę wewnętrzną odpowiedź stresową, zespół wykazał, że większy stres oznaczał więcej uszkodzeń jelita, podczas gdy jego blokada chroniła barierę jelitową. Myszy genetycznie zmodyfikowane tak, by nie miały ATF4, były w dużej mierze chronione: nawet po podaniu leków wywołujących stres, ich neutrofile nie mogły w pełni zrealizować swojego szkodliwego programu, a wyściółka jelita pozostawała znacznie bardziej nienaruszona.
Co to oznacza dla przyszłych terapii
W sumie te odkrycia kreślą klarowny obraz dla szerokiej publiczności: wśród tłumu komórek odpornościowych napływających do jelita po przywróceniu przepływu krwi, specyficzna, uprzednio zestresowana podgrupa neutrofili działa jak nadgorliwa ekipa sprzątająca, która burzy budynek razem z gruzem. Ich destrukcyjna siła zależy od wbudowanego szlaku stresowego kontrolowanego przez ATF4 wewnątrz komórek. Stłumienie tego szlaku — bez całkowitego zlikwidowania wszystkich neutrofili — mogłoby stanowić sposób ochrony jelita podczas sytuacji wysokiego ryzyka, takich jak duże operacje, ciężkie infekcje czy urazy. Choć potrzeba dalszych badań, by potwierdzić te wyniki u ludzi i znaleźć bezpieczne, precyzyjne leki, badanie otwiera obiecującą drogę do terapii, które utrzymają integralność bariery jelitowej, gdy pacjenci najbardziej tego potrzebują.
Cytowanie: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Słowa kluczowe: bariera jelitowa, niedokrwienie reperfuzja, neutrofile, stres retikulum endoplazmatycznego, ATF4