Clear Sky Science · pl
Peptyd CKAAKN sprzężony z długocirkulującymi nanoliposomami do celowanego dostarczania oridoniny do raka trzustki
Dlaczego te badania są ważne
Rak trzustki należy do najbardziej śmiertelnych nowotworów, częściowo dlatego, że zwykle wykrywany jest późno i często oporny na standardową chemioterapię. W tym badaniu zbadano inteligentniejszy sposób dostarczania pochodnej ziołowej o działaniu przeciwnowotworowym, oridoniny, bezpośrednio do guzów trzustki za pomocą maleńkich pęcherzyków tłuszczowych zwanych nanoliposomami. Dzięki zwiększeniu ilości leku docierającego do guza przy jednoczesnym oszczędzaniu tkanek zdrowych, praca ta wskazuje drogę do łagodniejszych i bardziej skutecznych opcji leczenia dla nowotworu, który ich pilnie potrzebuje.
Śmiertelny nowotwór trudny do leczenia
Rak trzustki zyskał ponury przydomek „króla nowotworów”, ponieważ wskaźniki przeżycia pozostają jednocyfrowe u większości pacjentów. Tylko niewielka część osób kwalifikuje się do operacji, a nawet wtedy wiele guzów nawraca. Leki chemioterapeutyczne, takie jak paklitaksel i cisplatyna, mogą spowalniać chorobę, ale wywołują silne skutki uboczne, a guzy często rozwijają oporność. Naukowcy poszukują więc leków bardziej precyzyjnych i mniej toksycznych oraz systemów dostarczania, które skoncentrują substancję czynna wewnątrz guza zamiast rozlewać ją po całym organizmie.
Przekształcanie ziołowej cząsteczki w nowoczesny lek
Oridonina to naturalny związek wyekstrahowany z tradycyjnej chińskiej rośliny leczniczej Rabdosia rubescens. Badania laboratoryjne wykazały, że może zabijać lub hamować wzrost wielu typów komórek nowotworowych, w tym z trzustki, poprzez zakłócanie podziału komórek i wywoływanie ich apoptozy. Jednak sama oridonina jest trudna do zastosowania jako lek: słabo rozpuszcza się w wodzie, jest słabo wchłaniana i przy wyższych dawkach może być toksyczna. Aby wykorzystać jej potencjał, autorzy postanowili zapakować oridoninę w nanoliposomy — maleńkie sfery z lipidów podobnych do tych w błonach komórkowych — zaprojektowane tak, by bezpiecznie przenosić lek przez krwiobieg i uwalniać go stopniowo w miejscu guza.
Projekt „stealth” z mechanizmem kierowania dla leku
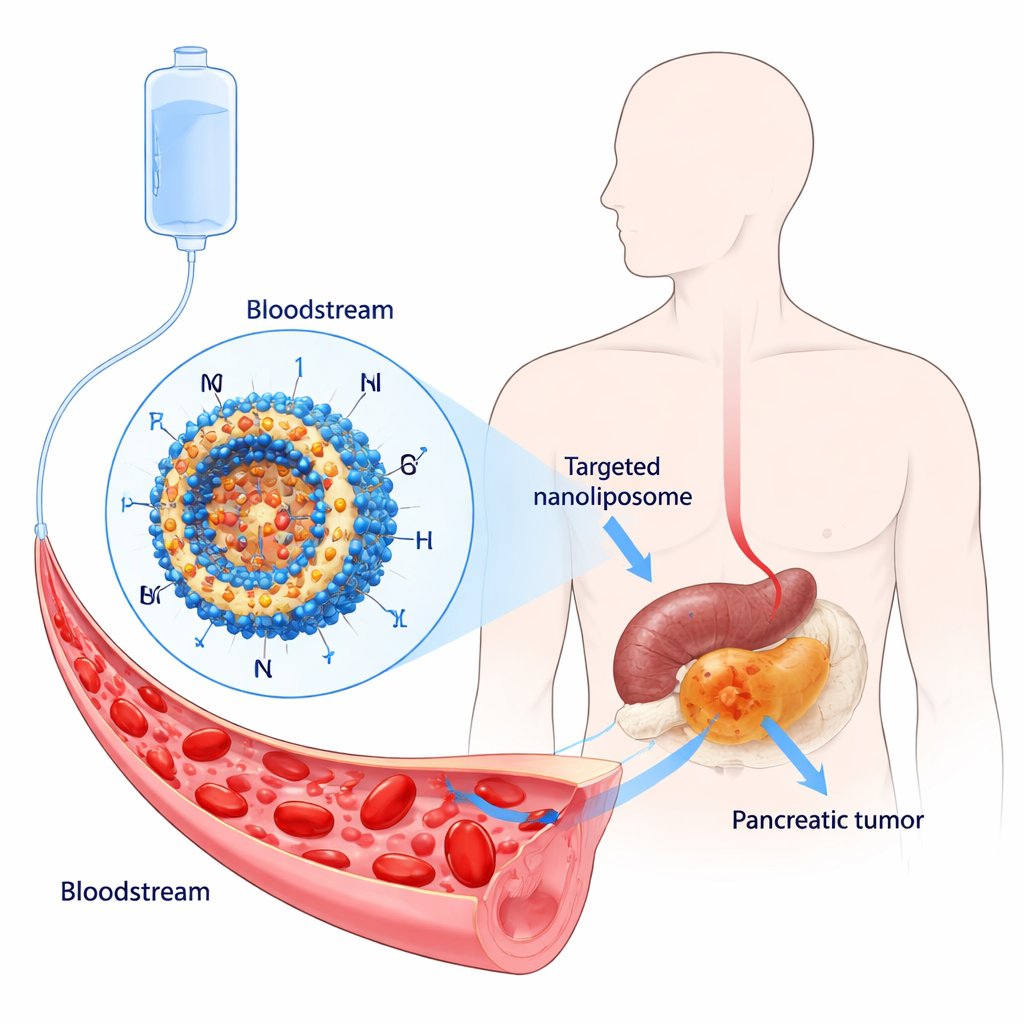
Zespół opracował dwuwarstwowy system dostarczania. Najpierw stworzyli długocirkulujące liposomy, powlekając ich powierzchnię poli(etylenoglikolem)em (PEG), elastycznym, hydrofilowym polimerem, który pomaga cząstkom unikać komórek układu odpornościowego i pozostawać dłużej we krwi. Następnie dodali krótki peptyd CKAAKN, który działa jak znacznik kierujący do raka trzustki. Peptyd ten naśladuje fragment szlaku sygnalizacyjnego Wnt, który jest nieprawidłowo aktywny w wielu guzach trzustki, co pozwala zmodyfikowanym liposomom (nazwanym ORI@CPD-Lipo) przyczepiać się do komórek nowotworowych prezentujących pasujące receptory. Końcowe cząstki miały około 100 nanometrów średnicy, zawierały dużą ilość oridoniny i uwalniały lek powoli przez wiele godzin zamiast natychmiast.
Jak cząstki celowane zachowują się w komórkach i organizmach
W testach na hodowlach komórkowych liposomy z oznakowaniem CKAAKN były pobierane znacznie wydajniej przez ludzkie komórki raka trzustki niż przez normalne komórki trzustki, szczególnie w pierwszych godzinach kontaktu. Gdy dodano nadmiar wolnego peptydu CKAAKN jako przynętę, komórki nowotworowe zaabsorbowały mniej cząstek, co potwierdza udział specyficznego etapu wiązania. Puste liposomy wykazywały niską toksyczność i nie uszkadzały erytrocytów, co sugeruje dobrą tolerancję. Po załadowaniu oridoniną, liposomy celowane zabijały komórki nowotworowe skuteczniej niż wolna oridonina lub liposomy bez ukierunkowania, a także silniej hamowały migrację komórek nowotworowych w teście „zadrapania”. U myszy z guzami trzustki fluorescencyjnie znakowane liposomy celowane kumulowały się w guzie do 48 godzin i gromadziły się tam bardziej niż liposomy nieukierunkowane, przy jednoczesnym oczekiwanym wydalaniu przez wątrobę i śledzionę.
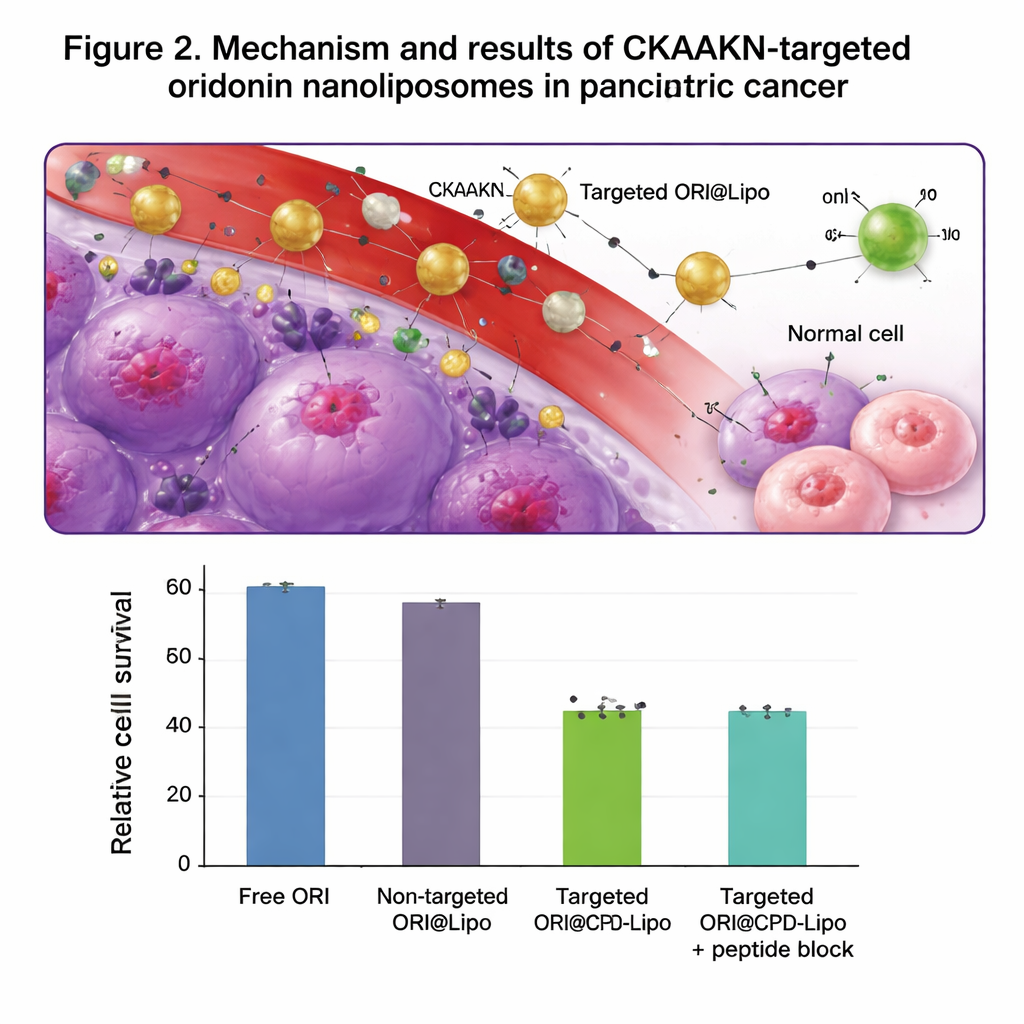
Co to może znaczyć dla przyszłych terapii
Podsumowując, wyniki pokazują, że połączenie tradycyjnego związku roślinnego z nowoczesnym, precyzyjnym nośnikiem może znacząco zwiększyć jego przeciwzapalną skuteczność w modelach laboratoryjnych. Nanoliposomy długocirkulujące i ozdobione CKAAKN kierują więcej oridoniny do komórek raka trzustki, ograniczając ekspozycję tkanek zdrowych, co wzmacnia śmierć komórek nowotworowych i zmniejsza ich migrację, która mogłaby prowadzić do przerzutów. Chociaż wyniki są nadal przedkliniczne i autorzy zauważają, że potrzebne są pełne badania terapeutyczne na zwierzętach i próby kliniczne, praca ta stanowi solidną podstawę dla celowanych podejść nanomedycyny wobec raka trzustki i sugeruje ogólną strategię przekształcania innych obiecujących naturalnych cząsteczek w praktyczne, poszukujące guza leki.
Cytowanie: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
Słowa kluczowe: rak trzustki, nanoliposomy, celowane dostarczanie leków, oridonina, peptyd kierujący do guza