Clear Sky Science · pl
Metadynamika ujawnia stabilizację konformacyjną pośredniczoną przez luteolinę przeciwko opornemu na awaprytynib PDGFRα D842V/G680R w GIST
Dlaczego to ma znaczenie dla leczenia raka
Leki celowane w onkologii potrafią działać niezwykle skutecznie — aż do momentu, gdy guzy wypracują sposoby ucieczki przed nimi. Ten artykuł bada, jak powszechne związek roślinny, luteolina, może pomóc przywrócić działanie ważnego leku stosowanego przeciwko niektórym guzom stromalnym przewodu pokarmowego (GIST). Dzięki zaawansowanym symulacjom komputerowym naukowcy pokazują, jak luteolina mogłaby ustabilizować zdeformowane białko w komórkach nowotworowych, tak by istniejący lek mógł znów się do niego przyłączyć, sugerując nowy sposób walki z opornością na leki bez konieczności całkowitego przeprojektowania terapii. 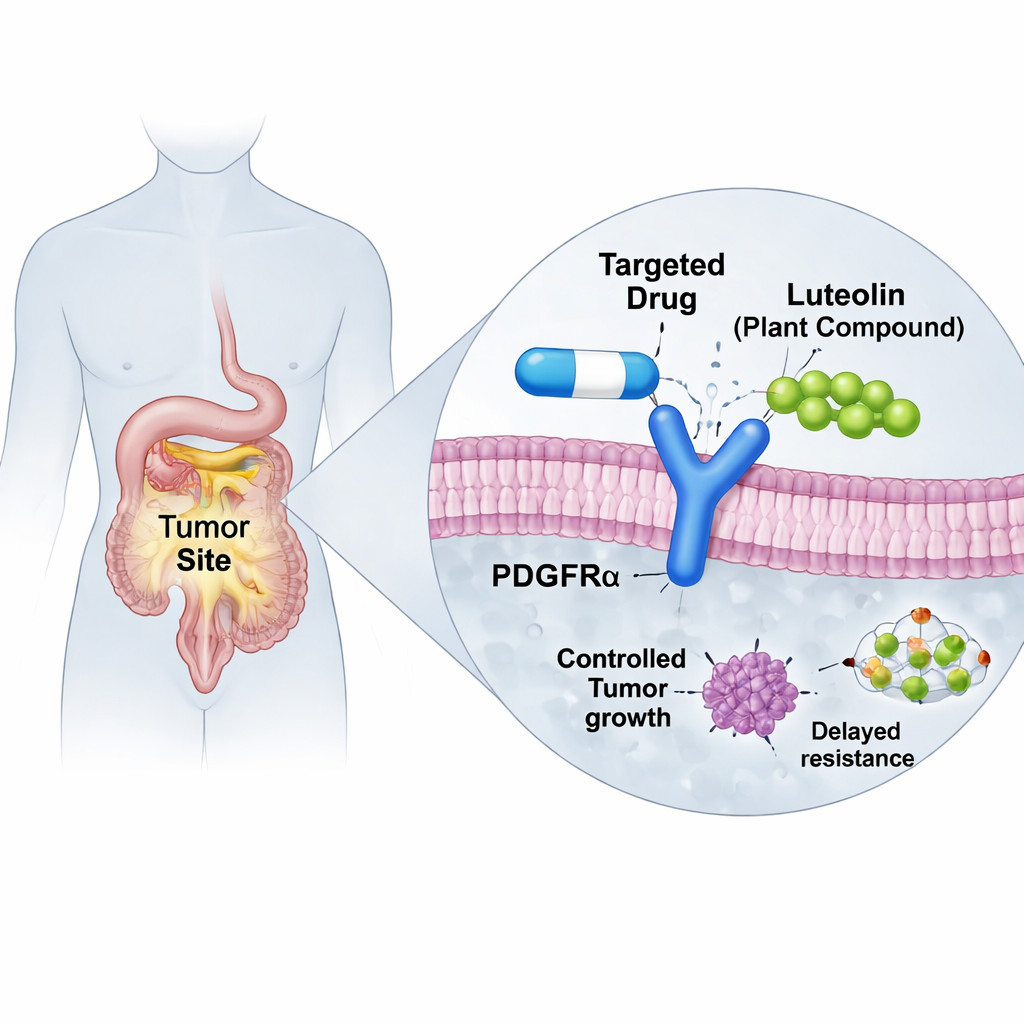
Problem guzów, które uczą się unikać leków
GIST często rozwijają się z powodu wadliwych „włączników” w białkach błonowych, znanych jako KIT lub PDGFRα, które generują stałe sygnały wzrostowe. Nowoczesne leki z grupy inhibitorów kinaz tyrozynowych zostały zaprojektowane, by wyłączać te przełączniki i zmieniły rokowania wielu pacjentów. Jednak częsta mutacja w PDGFRα, oznaczana jako D842V, sprawia, że starszy lek imatynib jest w dużej mierze nieskuteczny. Nowszy lek, awaprytynib, został stworzony specjalnie, by ujarzmić ten oporny mutant i wykazał imponującą skuteczność w badaniach klinicznych. Niestety guzy nadal potrafią się adaptować. U niektórych pacjentów pojawiają się dodatkowe zmiany w PDGFRα, takie jak wtórna mutacja G680R, które fizycznie blokują awaprytynib przed wygodnym dopasowaniem do kieszeni wiążącej, powodując wypadanie leku i narastanie oporności.
Roślinna cząsteczka o intrygującym kształcie
Produkty naturalne są bogatym źródłem pomysłów na leki, a flawonoidy — barwne związki występujące w wielu owocach, warzywach i roślinach leczniczych — są znane z interakcji z białkami kontrolującymi wzrost w komórkach. Luteolina, jeden z tych flawonoidów występujący w śródziemnomorskim krzewie Retama monosperma, była już badana pod kątem właściwości przeciwnowotworowych i przeciwzapalnych i wydaje się bezpieczna w dawkach osiągalnych przez suplementy doustne. Na podstawie wcześniejszych badań przesiewowych autorzy podejrzewali, że luteolina może wiązać się z PDGFRα w miejscu bliskim, lecz nie nakładającym się z typową więżącą kieszenią leku. Gdyby to potwierdzić, luteolina mogłaby działać jak subtelne wzmocnienie, popchnąć białko do kształtu, który ponownie zaakceptuje awaprytynib.
Symulacja cząsteczkowego partnerstwa
Aby przetestować ten pomysł in silico, zespół zbudował szczegółowe trójwymiarowe modele komputerowe opornego białka PDGFRα niosącego mutacje D842V i G680R. Symulowali zachowanie awaprytynibu samodzielnie oraz w obecności luteoliny w pobliżu, śledząc ruchy atomów przez setki nanosekund — miliardowe części sekundy w czasie rzeczywistym. Gdy tylko awaprytynib był związany sam, lek stopniowo wypływał z kieszeni, ponieważ masywna zmiana G680R go odpychała, aż w końcu całkowicie oddzielał się od białka. W przeciwieństwie do tego, gdy luteolina była również związana w oddzielnym miejscu „allosterycznym” obok kluczowej helisy, awaprytynib pozostawał w dużej mierze na swoim miejscu. Całe białko wykazywało mniejsze ugięcia, kluczowe segmenty strukturalne utrzymywały kształt, a istotne kontakty między lekiem a białkiem utrzymywały się znacznie dłużej. 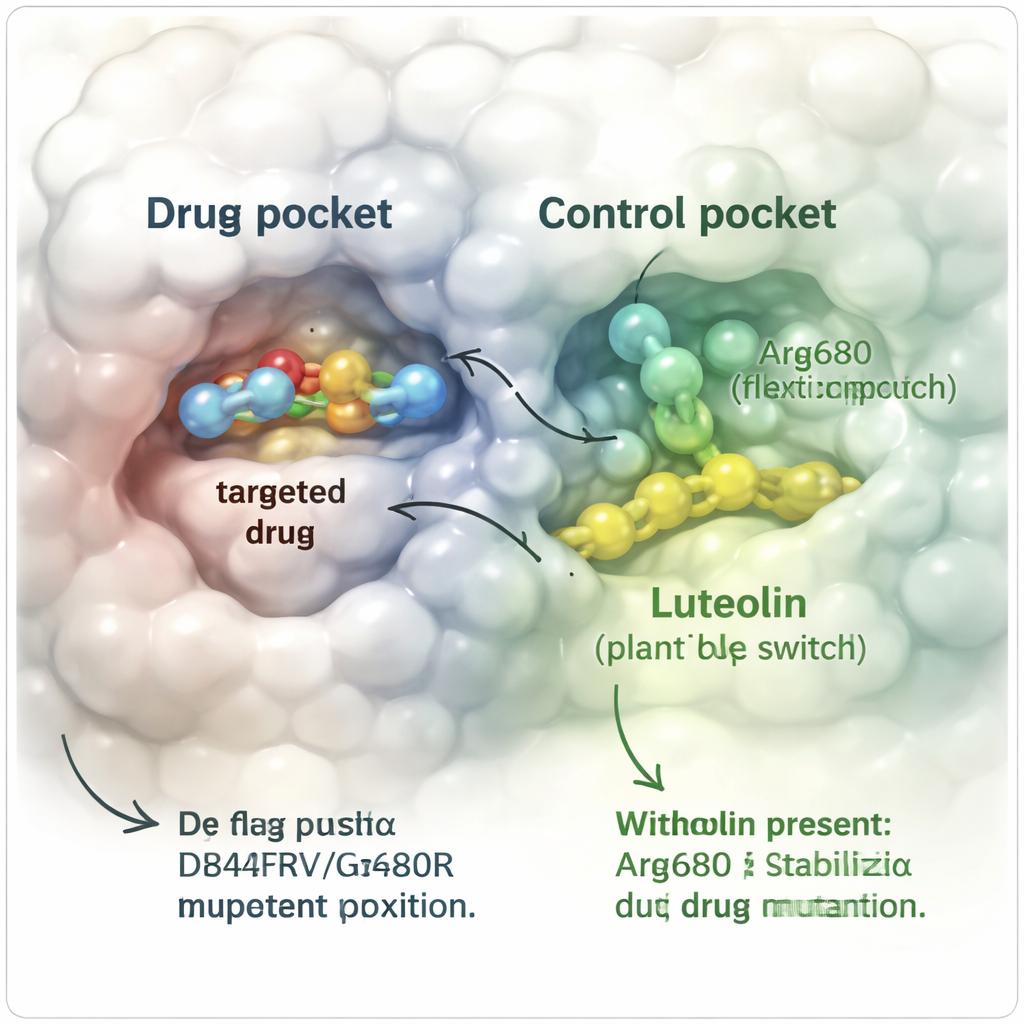
Przytrzymanie zwodniczego przełącznika molekularnego
Standardowe symulacje nadal pomijają rzadkie, ale istotne zmiany kształtu, więc badacze zastosowali ulepszone podejście zwane metadynamiką, aby pełniej zbadać, jak białko może się skręcać i zginać. Skoncentrowali się na zachowaniu zmienionego aminokwasu Arg680, który działa jak małe elastyczne ramię w pobliżu kieszeni leku. Bez luteoliny ramię to przemieszczało się przez wiele pozycji i lek łatwo się wymykał, z relatywnie niskimi barierami energetycznymi ucieczki. Gdy luteolina była obecna, Arg680 był utrzymywany w określonej orientacji, która przestała kolidować z lekiem. Krajobraz energetyczny przesunął się: układ preferował konformacje, w których awaprytynib pozostawał związany, a energetyczne „wzgórze”, które lek musiałby pokonać, by uciec, wzrosło o kilka kilokalorii, co znacząco zmniejszyło prawdopodobieństwo dysocjacji.
Co to może znaczyć dla pacjentów
Mówiąc prosto, badanie sugeruje, że luteolina może działać jak molekularna szyna, stabilizując zniekształcone białko nowotworowe, tak by istniejąca pigułka celowana mogła znów się go chwycić. Zamiast projektować zupełnie nowy lek dla każdej mutacji odpornościowej, parowanie aktualnego leku z ostro dobranym związkiem pomocniczym mogłoby przywrócić jego skuteczność. Praca opiera się na potężnych, lecz wyłącznie obliczeniowych metodach, dlatego potrzebne są badania laboratoryjne i na zwierzętach, aby potwierdzić, czy luteolina lub powiązana cząsteczka o lepszych właściwościach farmakologicznych rzeczywiście wzmocni awaprytynib w systemach żywych. Niemniej koncepcja używania małych allosterycznych pomocników do ponownego ustabilizowania opornych celów nowotworowych może otworzyć nową drogę przedłużania skuteczności dzisiejszych terapii precyzyjnych.
Cytowanie: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
Słowa kluczowe: oporność na leki, guz stromalny przewodu pokarmowego, inhibitory kinaz tyrozynowych, luteolina, modulacja allosteryczna